1. 领域背景与文献引入
文献英文标题:Revolutionizing oncology: the role of Artificial Intelligence (AI) as an antibody design, and optimization tools;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤学、抗体工程与人工智能交叉领域
抗体疗法自1975年单克隆抗体技术问世以来,已成为肿瘤精准治疗的核心手段之一。领域共识:目前全球已有超过160种抗体疗法获批上市,2028年市场规模预计将达4790亿美元。从早期的鼠源单克隆抗体,到如今的人源化单克隆抗体、抗体药物偶联物(ADC)、双特异性抗体、嵌合抗原受体T细胞(CAR-T细胞)等,抗体疗法的精准性与疗效不断提升,但仍面临诸多核心挑战:肿瘤的异质性、耐药性、免疫抑制微环境导致治疗响应率有限;传统抗体设计依赖实验筛选,周期长、成本高,难以覆盖庞大的序列空间,且对抗体的可开发性(如溶解度、聚集性、免疫原性)优化效率低下。
人工智能(AI)技术凭借其强大的大数据分析、结构预测与生成能力,为突破传统抗体设计的局限提供了新的解决方案。本文献旨在系统性综述AI在肿瘤抗体设计与优化中的最新进展,涵盖机器学习、深度学习、生成式AI等技术在抗体序列设计、结构预测、可开发性优化、抗原-抗体相互作用分析等环节的应用,为推动AI驱动的肿瘤抗体疗法发展提供全面的学术参考,填补了该领域缺乏系统性前沿综述的研究空白。
2. 文献综述解析
本文献采用“抗体疗法发展历程-传统方法局限-AI技术应用-挑战与前景”的核心评述逻辑,按抗体疗法类型(单克隆抗体、抗体药物偶联物、双特异性抗体等)与AI技术维度(机器学习、深度学习、生成式AI、大语言模型等)对现有研究进行分类整合,全面梳理了AI在肿瘤抗体设计领域的应用现状与前沿方向。
现有研究的关键结论显示,各类抗体疗法在多种肿瘤治疗中展现出显著疗效,但普遍存在免疫原性、溶解度差、易聚集、耐药性等问题;AI技术能够通过预测抗体序列与结构、优化可开发性、加速抗原-抗体相互作用分析,有效提升抗体设计的效率与质量。技术方法层面,机器学习模型(如支持向量机、随机森林)可用于抗体可开发性的早期预测,减少实验筛选成本;深度学习模型(如AlphaFold、IgFold)实现了高精度的抗体结构预测,为抗体设计提供了结构基础;生成式AI(如生成对抗网络、扩散模型)能够从头设计具有高亲和力的抗体序列,拓展了抗体的多样性。但现有研究也存在局限性:AI模型依赖高质量的实验数据,数据稀缺或偏差会影响模型性能;模型的可解释性不足,难以完全理解AI设计的抗体的作用机制;AI设计的抗体仍需大量实验验证,临床转化成本较高。
与现有研究多聚焦于单一AI技术或单一抗体设计环节不同,本文献的创新价值在于首次系统性整合了从传统机器学习到前沿大语言模型、扩散模型等多种AI技术在抗体设计全流程的应用,涵盖了可开发性优化、结构预测、表位识别、抗原-抗体相互作用分析等多个关键环节,并深入讨论了AI在肿瘤抗体疗法应用中的挑战与未来前景,为该领域的研究提供了全面的学术框架和方向指引。
3. 研究思路总结与详细解析
本文献为系统性综述,研究目标是全面梳理AI在肿瘤抗体设计与优化中的应用进展、技术优势、现存挑战及未来前景;核心科学问题是如何利用AI技术突破传统抗体设计的局限,提升肿瘤抗体疗法的疗效与可开发性;技术路线遵循“背景引入-现状综述-挑战分析-前景展望”的逻辑闭环,通过整合大量前沿研究成果,构建了AI驱动肿瘤抗体设计的完整学术图景。
3.1 抗体疗法发展历程与局限性综述
实验目的:系统回顾抗体疗法的发展阶段,明确传统抗体疗法的临床应用价值与核心局限。
方法细节:通过文献调研,梳理从单克隆抗体到嵌合抗原受体T细胞疗法等不同类型抗体疗法的发展时间线、代表药物、临床应用及局限性。
结果解读:文献指出,自1980年代首个单克隆抗体获批以来,全球已有162种抗体疗法获批,其中单克隆抗体如利妥昔单抗、曲妥珠单抗,抗体药物偶联物如维布妥昔单抗、T-DM1,双特异性抗体如blinatumomab,嵌合抗原受体T细胞疗法如tisagenlecleucel等已在临床广泛应用。然而,这些疗法普遍面临抗原异质性、免疫逃逸、免疫原性、耐药性等问题,传统抗体设计方法难以高效解决这些挑战。
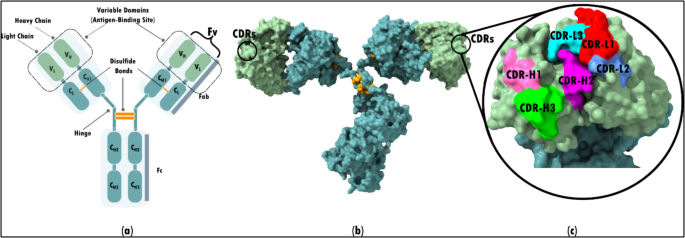
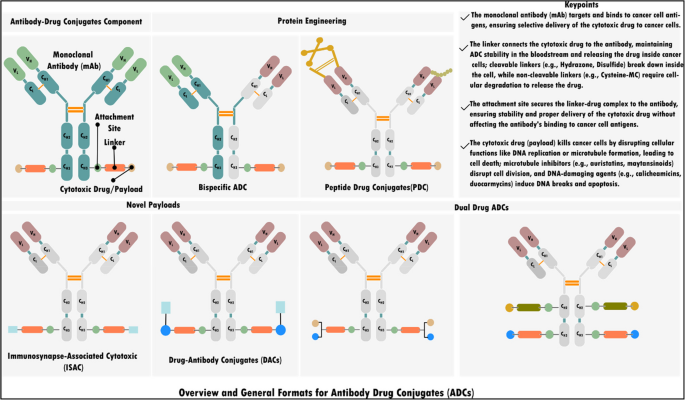
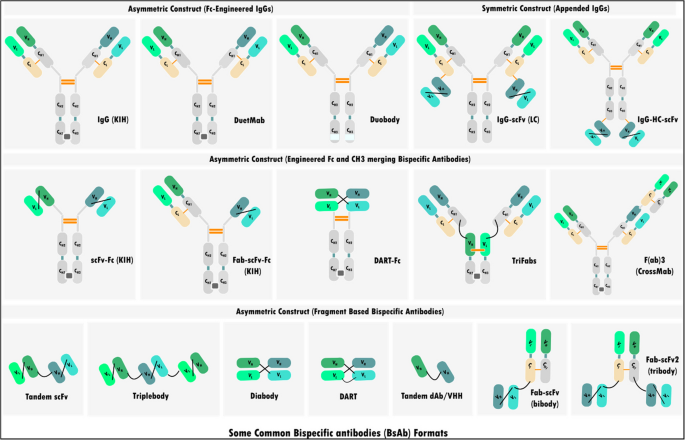
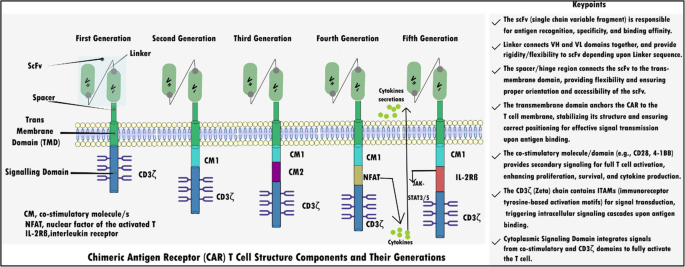
产品关联:文献未提及具体实验产品,领域常规使用临床病例数据库、药物审批数据库(如FDA、EMA数据库)等资源。
3.2 AI在抗体可开发性优化中的应用
实验目的:综述AI技术在抗体可开发性(包括溶解度、聚集性、粘度、免疫原性等)优化中的应用进展。
方法细节:整合现有研究中机器学习、深度学习模型在抗体可开发性预测与优化中的应用案例,分析不同模型的性能与优势。
结果解读:现有研究表明,支持向量机、随机森林、XGBoost等机器学习模型可通过分析抗体序列与理化性质,实现对抗体溶解度、聚集性、粘度等可开发性指标的早期预测,准确率可达74%以上;深度学习模型如ESM-1b、AntiBERTa可通过预训练语言模型,更精准地预测抗体的免疫原性,为降低抗体免疫原性提供设计依据。例如,SOLpro、PaRSnIP等工具可预测抗体溶解度,Aggrescan3D可识别聚集-prone区域并指导突变优化。
产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析软件(如Python、R语言工具包)、高通量筛选平台等。
3.3 AI在抗体结构与表位预测中的应用
实验目的:总结AI技术在抗体结构预测、B细胞表位与抗体互补决定区(CDR)预测中的应用。
方法细节:梳理AlphaFold、IgFold、DeepAb等AI工具在抗体结构预测中的性能,以及BepiPred、DiscoTope等工具在表位预测中的应用。
结果解读:AlphaFold2/3实现了高精度的蛋白质结构预测,包括抗体的可变区与互补决定区结构;IgFold、ImmuneBuilder等工具针对抗体结构进行优化,预测速度更快,可实现大规模抗体结构预测;表位预测工具如BepiPred、DiscoTope可通过序列或结构分析,预测抗原上的B细胞表位,为抗体设计提供靶点。例如,DeepH3模型对CDR-H3环结构的预测准确率较传统方法提升32.1%,平均RMSD为2.2±1.1 Å。
产品关联:文献未提及具体实验产品,领域常规使用蛋白质结构数据库(如PDB)、结构预测软件(如AlphaFold、Rosetta)等。
3.4 AI在抗原-抗体相互作用分析中的应用
实验目的:综述AI技术在抗原-抗体相互作用预测、亲和力优化中的应用。
方法细节:整合现有研究中AI模型在抗原-抗体结合界面预测、亲和力预测、亲和力成熟中的应用案例。
结果解读:AI模型可通过分析抗体与抗原的序列、结构信息,预测两者的结合界面与亲和力,例如,mCSM-AB2模型可预测突变对抗体-抗原结合亲和力的影响,Pearson相关系数在训练集和盲测中分别达0.73和0.77;生成式AI如生成对抗网络、扩散模型可从头设计具有高亲和力的抗体互补决定区序列,部分模型设计的抗体亲和力可达纳摩尔级,与临床药物相当。
产品关联:文献未提及具体实验产品,领域常规使用表面等离子体共振(SPR)、生物层干涉技术(BLI)等实验仪器验证亲和力,使用分子对接软件(如AutoDock、RosettaDock)进行相互作用分析。
3.5 前沿AI技术在抗体设计中的应用
实验目的:探讨大语言模型、扩散模型等前沿AI技术在抗体设计中的最新进展。
方法细节:梳理AntiBERTa、IgLM、AbDiffuser等前沿AI工具的原理与应用案例。
结果解读:大语言模型如AntiBERTa、IgLM通过预训练大量抗体序列,可实现抗体序列生成、表位预测、结构预测等多种任务;扩散模型如AbDiffuser可实现抗体3D结构与序列的协同生成,实验验证显示其设计的HER2抗体中57.1%具有强结合特性。这些前沿技术进一步拓展了抗体设计的可能性,提升了设计的效率与质量。
产品关联:文献未提及具体实验产品,领域常规使用预训练语言模型框架(如Hugging Face Transformers)、深度学习框架(如PyTorch、TensorFlow)等。
3.6 AI驱动的抗体药物发现平台与临床转化
实验目的:综述AI驱动的抗体药物发现平台及临床转化进展。
方法细节:梳理BenevolentAI、Exscientia、AbCellera等企业的AI平台在抗体药物发现中的应用,以及AI设计的抗体进入临床的案例。
结果解读:AI驱动的药物发现平台可加速抗体从设计到临床的转化,例如,BenevolentAI利用AI重新定位巴瑞替尼用于COVID-19治疗,显著降低住院患者死亡率;AbCellera开发的bamlanivimab进入COVID-19治疗的II期临床试验;多个AI设计的肿瘤抗体如AU-007、ADG-106等已进入I/II期临床试验,展现出良好的临床前景。

产品关联:文献未提及具体实验产品,领域常规使用AI药物发现平台(如BenevolentAI、Exscientia)、临床研究数据库等。
3.7 挑战与未来前景分析
实验目的:分析AI在肿瘤抗体设计应用中的现存挑战,并展望未来发展方向。
方法细节:整合现有研究中关于AI应用的局限性讨论,结合技术发展趋势提出未来方向。
结果解读:当前AI在抗体设计中的应用面临数据质量与多样性不足、模型可解释性差、实验验证成本高、多目标优化难度大等挑战;未来发展方向包括整合物理建模与AI、多组学数据融合、可解释AI、自动化实验与AI的闭环结合等,以提升AI设计抗体的临床转化效率与成功率。
产品关联:文献未提及具体实验产品,领域常规使用实验验证平台(如细胞培养、动物模型)、自动化实验设备等。
4. Biomarker研究及发现成果
本文献为系统性综述,未报道原创性的Biomarker发现,但全面综述了AI在肿瘤抗体疗法相关Biomarker研究中的应用,包括免疫检查点抑制剂响应Biomarker、抗体疗法耐药Biomarker的预测与筛选,以及AI辅助Biomarker驱动的精准抗体设计。
Biomarker定位方面,现有研究中,肿瘤突变负荷、PD-L1表达水平、微卫星不稳定性等是免疫检查点抑制剂的经典响应Biomarker;AI技术可通过分析多组学数据(基因组、转录组、蛋白质组),预测患者对抗体疗法的响应性与耐药风险,例如,AI模型可通过分析肿瘤组织的基因表达数据,预测抗HER2疗法的耐药性,为患者筛选更合适的治疗方案。
研究过程中,AI辅助Biomarker研究主要通过整合临床数据、多组学数据与抗体疗法的疗效数据,构建机器学习模型进行预测。例如,部分研究利用AI模型分析PD-L1表达、肿瘤突变负荷等数据,预测免疫检查点抑制剂的响应率,AUC可达0.8以上;AI还可通过分析抗体与抗原的相互作用,预测抗体的脱靶效应,为降低抗体毒性提供Biomarker依据。
核心成果提炼显示,AI技术提升了Biomarker筛选的效率与准确性,能够发现传统方法难以识别的新型Biomarker,例如,通过AI分析抗体序列与免疫原性的关系,可预测抗体的免疫原性Biomarker,为降低抗体免疫原性提供设计靶点;AI驱动的Biomarker研究还可实现精准的患者分层,为个性化抗体疗法提供支持。目前,AI辅助Biomarker研究仍面临数据异质性、模型可解释性等挑战,未来需进一步整合多源数据与实验验证,提升Biomarker的临床应用价值。
