1. 领域背景与文献引入
文献英文标题:Androgen receptor splice variant 7 detected by immunohistochemical is an independent poor prognostic marker in men receiving adjuvant androgen-deprivation therapy after radical prostatectomy;发表期刊:Biomarker Research;影响因子:未公开;研究领域:前列腺癌预后生物标志物研究
前列腺癌是全球男性发病率第二、死亡率第五的恶性肿瘤,2018年全球新发病例约130万,死亡病例35.9万,在中国也是男性常见的高致死性恶性肿瘤之一。根治性前列腺切除术是局限期前列腺癌的一线根治性治疗手段,但高危患者(如Gleason评分≥8、术前PSA≥20ng/mL、局部进展期或手术切缘阳性)术后易出现生化复发或远处转移,辅助雄激素剥夺治疗(AHT)是目前临床常用的辅助治疗方式,旨在通过抑制雄激素信号通路降低复发风险。
现有研究显示,AHT能延长部分高危患者的无进展生存期,但对总生存期的获益存在争议,且部分患者会出现治疗耐药并最终进展为去势抵抗性前列腺癌。雄激素受体(AR)剪接变体尤其是AR-V7是近年来的研究热点,该变体缺乏AR的C端配体结合域,可不依赖雄激素激活下游靶基因,导致雄激素剥夺治疗耐药。已有研究证实,AR-V7在去势抵抗性前列腺癌患者中与更差的预后相关,在激素敏感性前列腺癌患者中也被发现与治疗反应不佳有关,但针对根治性前列腺切除术后接受AHT的特定人群,AR-V7的预后价值尚未得到明确验证,不同研究中AR-V7的阳性率差异较大,检测方法的标准化也有待完善,这一研究空白促使本文开展针对性的回顾性队列研究。
2. 文献综述解析
本文综述部分围绕前列腺癌辅助治疗现状、AR-V7的结构功能及现有研究局限性展开,核心评述逻辑为:先梳理前列腺癌术后辅助治疗的应用价值与不足,再总结AR-V7的生物学特性及在前列腺癌中的研究进展,最后聚焦于术后接受AHT的特定人群,指出该领域的研究缺失,明确本文的研究必要性。
作者首先回顾了前列腺癌的治疗格局,指出根治性前列腺切除术联合AHT是高危局限期患者的标准治疗方案之一,但部分研究显示AHT对总生存期的获益不显著,且患者的预后差异较大,缺乏有效的预后分层标志物。随后,作者总结了AR-V7的结构与功能:AR-V7是AR的异常剪接变体,保留了N端转录激活域但缺失C端配体结合域,可不依赖雄激素持续激活下游雄激素应答基因,驱动前列腺癌的进展和耐药。现有研究表明,AR-V7在去势抵抗性前列腺癌患者中阳性率较高,且与对恩杂鲁胺、阿比特龙等新型内分泌治疗的耐药性相关,在激素敏感性前列腺癌患者中,AR-V7阳性也与更差的预后相关,但这些研究多未限定患者的治疗方式,或未聚焦于术后接受AHT的人群。
此外,作者还指出不同研究中AR-V7的阳性率差异显著(1.6%-91.8%),主要与检测抗体、人群选择、肿瘤分期等因素有关,而采用经过验证的抗体是确保检测结果可靠的关键。现有研究的核心局限性在于缺乏针对术后接受AHT的高危前列腺癌患者的大样本研究,无法明确AR-V7在该特定人群中的独立预后价值,本文正是针对这一空白,采用经过验证的免疫组化(IHC)抗体,开展回顾性队列研究以填补该领域的研究缺口。
3. 研究思路总结与详细解析
本文的研究目标是明确免疫组化检测的AR-V7表达在根治性前列腺切除术后接受AHT的前列腺癌患者中的预后价值,核心科学问题为AR-V7是否可作为该人群的独立不良预后标志物,技术路线遵循“回顾性样本收集→生物标志物检测→临床病理特征分析→生存预后分析→亚组验证”的闭环逻辑,通过严谨的统计学分析验证研究假设。
3.1 临床样本收集与入组标准
实验目的为获取符合研究要求的术后AHT患者的临床病理数据与组织样本,确保研究人群的同质性。方法细节为回顾性收集2010-2017年华中科技大学同济医学院附属同济医院110例接受根治性前列腺切除术+扩大盆腔淋巴结清扫(ePLND)后接受AHT的前列腺癌患者,入组标准包括:年龄≥18岁、病理确诊为前列腺腺癌、高危(Gleason评分≥8或术前PSA≥20ng/mL)或局部进展期(pT3/pT4、N0M0或任何T、N1M0)或手术切缘阳性(R1)、术后立即接受AHT,排除接受其他辅助抗癌治疗(如放疗、化疗)的患者,所有患者均签署知情同意书。实验所用关键产品:Abcam的AR-V7单克隆抗体(货号ab198394,1:150稀释)、Abcam的全长AR多克隆抗体(货号ab133273,1:100稀释)、Leica Biosystems的Bond Polymer Refine检测系统。结果解读显示,共入组110例患者,其中21例(19.1%)为AR-V7阳性,89例(80.9%)为AR-V7阴性,两组患者在年龄、Gleason评分、术前PSA、TN分期、前列腺体积、手术切缘状态等基线特征上无显著统计学差异(P值均>0.05),确保了后续生存分析的可比性。
3.2 AR-V7免疫组化检测与结果判读
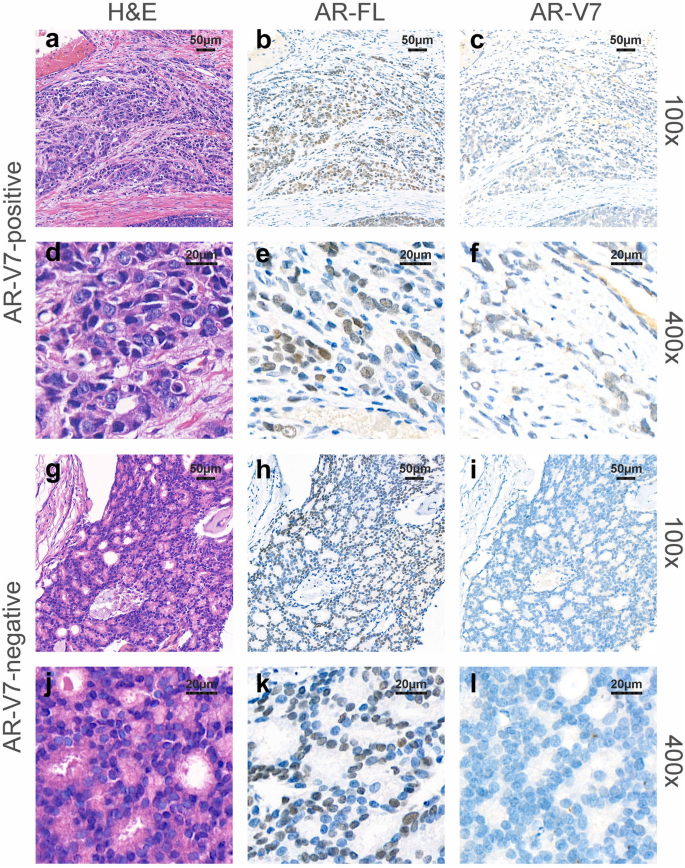
实验目的为准确、可靠地检测前列腺癌组织中AR-V7的表达水平,避免检测方法差异导致的结果偏差。方法细节为采用Leica的Bond Polymer Refine检测系统对手术标本进行免疫组化染色,AR-V7抗体选用经过多项研究验证的Abcam ab198394(1:150稀释),同时检测全长AR(AR-FL)的表达作为参照,以磷酸盐缓冲液替代一抗作为阴性对照。采用免疫反应评分(IRS)评估AR-V7表达水平,IRS为染色强度(0=阴性、1=弱阳性、2=中等阳性、3=强阳性)与阳性细胞比例(0=<1%、1=1%-10%、2=11%-50%、3=51%-80%、4=>81%)的乘积,IRS<2定义为阴性,IRS≥2定义为阳性,所有切片由两名不知情的资深病理医师独立判读,若存在分歧则由第三名医师参与评估并取平均评分。结果解读显示,代表性染色图片清晰展示了AR-V7阳性与阴性样本的差异(图1),本文中AR-V7的阳性率为19.1%(n=110),处于现有研究报道的合理范围内,采用的抗体已被证实适用于前列腺癌组织的免疫组化检测,确保了结果的可靠性。
3.3 生存预后分析与亚组验证
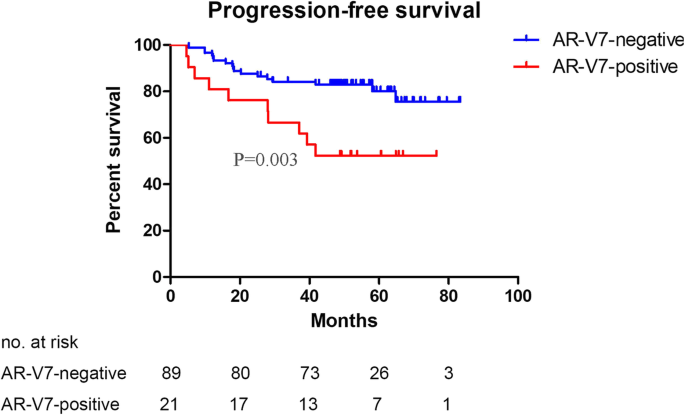
实验目的为明确AR-V7表达与患者生存结局的关联,并验证其独立预后价值。方法细节为采用Kaplan-Meier法绘制无进展生存期(PFS)、总生存期(OS)、癌症特异性生存期(CSS)的生存曲线,通过log-rank检验比较AR-V7阳性与阴性组的差异;采用单因素和多因素Cox比例风险回归模型分析AR-V7及其他临床病理因素对生存结局的影响,多因素分析调整了年龄、TN分期、Gleason评分、术前总PSA等混杂因素;进一步将患者分为局限期和局部进展期亚组,分析AR-V7在不同亚组中的预后价值。结果解读显示,AR-V7阳性患者的PFS显著短于阴性患者(HR=4.26,95%CI 1.55-11.68,P=0.003),AR-V7阴性组的中位PFS未达到,而阳性组的中位PFS为58.6个月,两组5年PFS率分别为80.1%和52.4%(P=0.004)(图2);多因素Cox回归分析显示,AR-V7是PFS的独立危险因素(HR=3.76,95%CI 1.63-8.70,P=0.002)。
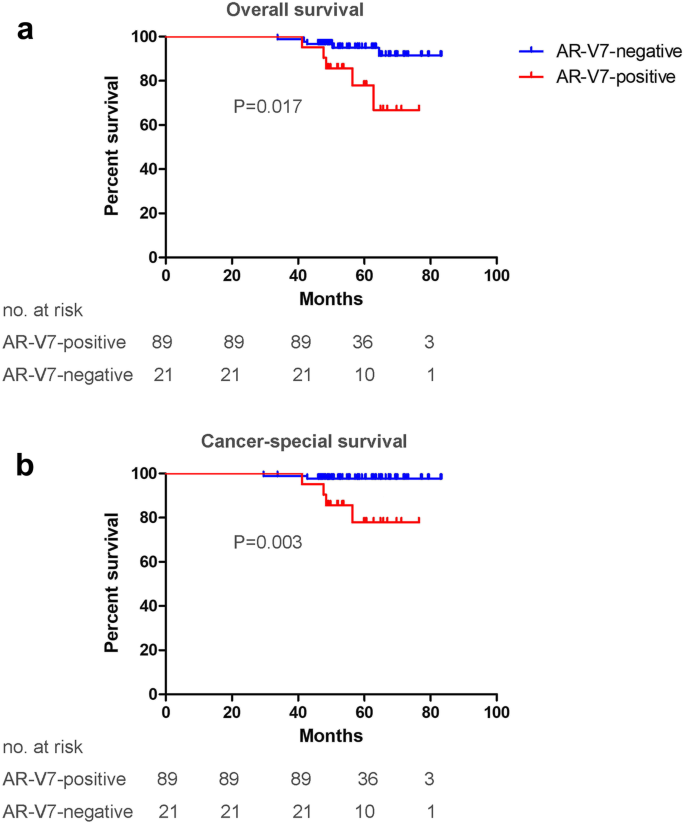
在OS和CSS方面,AR-V7阳性患者的OS(HR=6.61,95%CI 1.40-31.20,P=0.017)和CSS(HR=22.47,95%CI 2.91-173.4,P=0.003)均显著短于阴性患者(图3);多因素分析显示AR-V7是OS(HR=4.81,95%CI 1.28-17.86,P=0.020)和CSS(HR=9.17,95%CI 1.48-55.56,P=0.017)的独立危险因素。
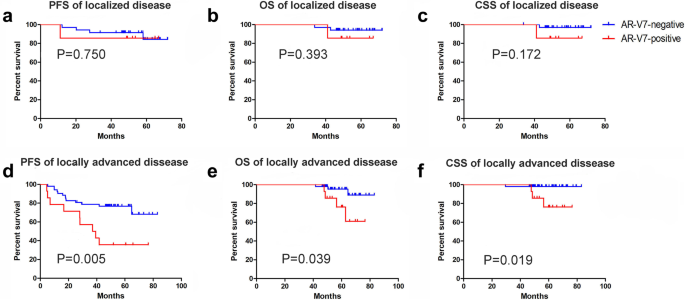
进一步亚组分析显示,在局部进展期患者中,AR-V7阳性与更短的PFS、OS、CSS显著相关,而在局限期患者中,两组的生存结局差异无统计学意义(图4),提示AR-V7的预后价值在局部进展期患者中更为显著。
4. Biomarker研究及发现成果解析
本文聚焦的Biomarker为雄激素受体剪接变体7(AR-V7),属于蛋白类肿瘤预后标志物,筛选与验证逻辑为:基于临床回顾性队列→免疫组化检测组织中AR-V7表达→生存分析验证与预后的关联→多因素回归确认独立预后价值→亚组分析进一步验证特异性,形成了完整的验证链条。
该Biomarker的来源为根治性前列腺切除术获取的前列腺癌组织标本,验证方法为免疫组化染色,采用经过多项研究验证的Abcam ab198394抗体,确保检测的特异性和可靠性。研究中,AR-V7的阳性率为19.1%(n=110),与现有针对激素敏感性前列腺癌患者的研究结果一致。生存分析数据显示,AR-V7阳性患者的无进展生存期风险比(HR)为4.26(95%CI 1.55-11.68,P=0.003),总生存期HR为6.61(95%CI 1.40-31.20,P=0.017),癌症特异性生存期HR为22.47(95%CI 2.91-173.4,P=0.003);多因素回归分析调整混杂因素后,AR-V7仍为无进展生存期(HR=3.76,95%CI 1.63-8.70,P=0.002)、总生存期(HR=4.81,95%CI 1.28-17.86,P=0.020)和癌症特异性生存期(HR=9.17,95%CI 1.48-55.56,P=0.017)的独立危险因素,显示出良好的特异性和预后价值。
核心成果方面,本文首次明确在根治性前列腺切除术后接受AHT的高危前列腺癌患者中,免疫组化检测的AR-V7是独立的不良预后标志物,尤其是在局部进展期患者中,AR-V7阳性与显著更差的生存结局相关。这一发现的创新性在于,针对术后接受AHT的特定人群填补了AR-V7预后价值研究的空白,为该人群的预后分层提供了可靠的生物标志物,有助于临床医师制定个体化的随访和治疗方案,同时也为AR-V7阳性患者的新型治疗策略(如紫杉类化疗、AR-V7靶向药物)提供了理论依据。
