1. 领域背景与文献引入
文献英文标题:Early kinetics of serum amyloid A predict clinical benefit to first-line chemoimmunotherapy and immunotherapy in advanced non-small cell lung cancer: a retrospective analysis;发表期刊:Biomarker Research;影响因子:未公开;研究领域:晚期非小细胞肺癌免疫治疗与化疗免疫治疗的生物标志物研究
领域共识:晚期非小细胞肺癌(NSCLC)是全球发病率和死亡率最高的恶性肿瘤之一,2010年后以程序性死亡受体1(PD-1)/程序性死亡受体配体1(PD-L1)为靶点的免疫检查点抑制剂(ICIs)的出现,成为晚期NSCLC治疗的关键突破节点。目前,ICIs单药或联合铂类化疗已成为无驱动基因突变晚期NSCLC的标准一线治疗方案,但仅约20%-30%的患者能获得长期临床获益,大部分患者存在原发或继发耐药。当前领域研究热点聚焦于开发精准的疗效预测生物标志物,以筛选潜在获益患者、优化治疗策略,但现有生物标志物仍存在诸多局限。组织来源的PD-L1表达、肿瘤突变负荷(TMB)是临床常用的预测指标,但受肿瘤异质性、有创活检的限制,难以动态反映治疗过程中的免疫应答变化;血液来源的循环肿瘤DNA(ctDNA)、中性粒细胞-淋巴细胞比值(NLR)等标志物虽具有无创优势,但ctDNA检测成本高、技术复杂度高,NLR等静态炎症指标的预测特异性不足。此外,血清淀粉样蛋白A(SAA)作为炎症相关的急性期蛋白,其静态水平在免疫单药治疗中的预测价值已被报道,但在化疗免疫治疗中的动态动力学模式对疗效的预测作用尚未明确,这一空白限制了临床对化疗免疫治疗患者的动态监测与疗效预判。
针对这一研究空白,本研究旨在探讨SAA早期动力学模式(flare应答、持续应答、无应答)对晚期NSCLC一线化疗免疫治疗及免疫单药治疗临床结局的预测价值,为临床提供一种无创、低成本、可动态监测的疗效预测生物标志物,以弥补现有标志物的不足。
2. 文献综述解析
本文献综述部分以生物标志物的类型(组织vs血液)、检测特性(静态vs动态)为分类维度,系统梳理了晚期NSCLC免疫治疗疗效预测生物标志物的研究现状,明确了现有研究的优势与局限,并针对性提出本研究的创新方向。
现有研究中,组织来源的PD-L1表达、TMB因能直接反映肿瘤免疫原性,被广泛用于筛选ICIs获益患者,但这类标志物存在明显局限性,如肿瘤异质性导致的检测结果偏差,以及有创活检带来的患者依从性问题。血液来源的生物标志物因无创、可动态监测的优势成为研究热点,其中NLR、乳酸脱氢酶(LDH)等静态炎症指标被证实与免疫治疗疗效相关,但预测特异性不足;ctDNA能反映肿瘤负荷变化,但高成本与技术复杂度限制了其临床普及。针对SAA的研究仅聚焦于静态水平在免疫单药中的预测价值,尚未涉及化疗免疫治疗中的动态动力学模式,而化疗免疫治疗过程中炎症反应的动态变化更为复杂,现有研究无法为这类患者提供有效的动态监测指标。
本研究的核心创新在于首次将SAA的早期动力学模式(flare应答,即先升高后降至基线以下的变化)应用于晚期NSCLC的一线化疗免疫治疗及免疫单药治疗的疗效预测,弥补了SAA动态变化在化疗免疫治疗中研究的空白。与现有静态生物标志物相比,SAA动力学模式能更精准地反映治疗过程中系统性炎症与抗肿瘤免疫应答的动态交互作用,且作为低成本的常规检测指标,具有更高的临床可及性,为晚期NSCLC患者的疗效预判与动态监测提供了新的选择。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确SAA早期动力学模式对晚期NSCLC一线化疗免疫治疗及免疫单药治疗临床结局的预测价值,核心科学问题是SAA动态变化是否能反映抗肿瘤免疫应答的激活状态,进而预测患者的生存获益,技术路线遵循“回顾性患者入组→SAA动力学分组→生存结局分析→独立预后价值验证”的逻辑闭环,通过临床数据的回顾性分析验证研究假设。
3.1 研究对象筛选与分组
实验目的:确定符合入组标准的晚期NSCLC患者,并基于治疗早期的SAA动力学模式完成分组,为后续生存分析奠定基础。方法细节:回顾性纳入2016年8月至2024年12月期间,中山大学肿瘤防治中心接受一线PD-(L)1抑制剂单药或联合铂类化疗的242例无驱动基因突变的晚期NSCLC患者;在治疗开始后的12周内定期采集患者血清样本,检测SAA水平,并参考Fukuda等提出的flare应答定义,将患者分为flare应答组(SAA先升高后降至基线以下)、持续应答组(SAA持续下降)、无应答组(SAA无下降或持续升高)。结果解读:各组患者的基线特征差异在表1中呈现(文献未明确具体差异数据),图1展示了化疗免疫治疗组与免疫单药组中SAA水平随时间的变化趋势,两组中均清晰呈现三种不同的动力学模式,为后续分组分析提供了依据。
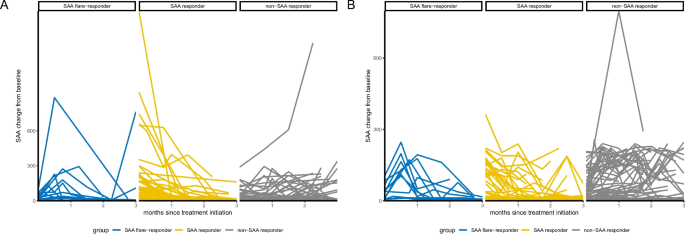
产品关联:文献未提及具体实验产品,领域常规使用免疫比浊法或酶联免疫吸附实验(ELISA)检测血清SAA水平。
3.2 生存结局分析与预后价值验证
实验目的:验证SAA早期动力学模式对患者无进展生存期(PFS)与总生存期(OS)的预测价值,并明确其是否为独立预后因素。方法细节:采用Kaplan-Meier法绘制不同SAA动力学组的生存曲线,通过Log-rank检验比较组间生存差异;进一步采用单因素与多因素Cox回归分析,调整年龄、性别、东部肿瘤协作组体能状态评分(ECOG PS)等潜在混杂因素,验证SAA早期动力学模式的独立预后价值。结果解读:在化疗免疫治疗组中,flare应答者的中位PFS为29.8个月(95%置信区间(CI):9.95-49.65),显著长于无应答者的7.4个月(95%CI:4.67-10.13),风险比(HR)=0.31(95%CI:0.15-0.64,P<0.01);在免疫单药组中,flare应答者的中位PFS为19.9个月,显著长于无应答者的2.1个月(HR=0.31,P<0.01)。图2展示了两组患者基于SAA早期动力学的PFS与OS曲线,直观呈现了组间的生存差异。多因素Cox回归分析显示,在调整所有潜在混杂因素后,SAA早期动力学模式仍是两组患者PFS与OS的独立预后因素(表2),证实了其预测价值的独立性。
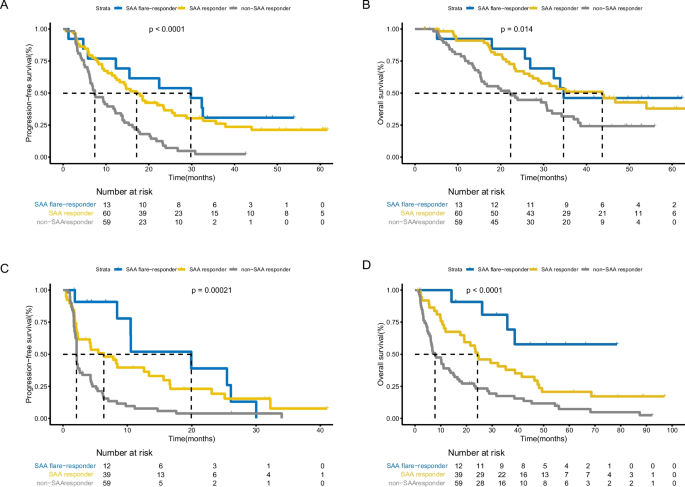
产品关联:文献未提及具体实验产品,领域常规使用SPSS、R等统计分析软件进行生存曲线绘制与Cox回归分析。
4. Biomarker研究及发现成果解析
本文献涉及的Biomarker为血清淀粉样蛋白A(SAA)的早期动力学模式,包括flare应答、持续应答、无应答三种类型,通过“回顾性临床数据筛选→生存分析验证→多因素回归确认”的完整逻辑链条,证实了其作为晚期NSCLC一线化疗免疫治疗及免疫单药治疗疗效预测标志物的价值。
该Biomarker的来源为患者治疗期间的外周血血清样本,筛选逻辑基于Fukuda等在转移性肾细胞癌中提出的flare应答模式,结合晚期NSCLC免疫治疗中的炎症应答特点,将SAA早期动力学模式分为三类;验证方法为定期检测治疗12周内的SAA水平,结合患者的PFS、OS及客观缓解率(ORR)数据进行生存分析与组间比较。特异性与敏感性数据方面,化疗免疫治疗组中flare应答者的ORR为46%(6/13),显著高于无应答者的34%(20/59,P=0.01);免疫单药组中flare应答者的ORR为25%(3/12),高于无应答者的7%(4/59,P=0.07),提示flare应答模式与更高的客观缓解率相关。
本研究的核心成果在于证实SAA早期动力学模式是晚期NSCLC一线化疗免疫治疗及免疫单药治疗的独立预后因素,其中flare应答模式与显著延长的PFS相关(化疗免疫治疗组HR=0.31,P<0.01;免疫单药组HR=0.31,P<0.01)。该Biomarker的创新性在于首次将SAA的动态动力学模式应用于化疗免疫治疗的疗效预测,弥补了现有静态生物标志物无法动态反映免疫应答变化的不足;同时,SAA作为常规检测指标,具有低成本、无创、可重复检测的优势,临床可及性高。统计学结果显示,所有生存分析的组间差异P值均<0.01,样本量n=242(化疗免疫治疗组n=132,免疫单药组n=110),证实了研究结果的可靠性。此外,推测:SAA早期动力学模式反映了治疗过程中系统性炎症与抗肿瘤免疫应答的动态交互作用,flare应答模式可能提示早期免疫激活,为进一步的机制研究提供了方向,但仍需前瞻性研究与基础实验验证其生物学机制。
