1. 领域背景与文献引入
文献英文标题:MRI-derived radiomics assessing tumor-infiltrating macrophages enable prediction of immune-phenotype, immunotherapy response and survival in glioma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:神经胶质瘤免疫治疗与影像组学生物标志物研究。
神经胶质瘤是中枢神经系统最常见的原发性恶性肿瘤,其中高级别胶质瘤(HGG)患者预后极差,中位总生存期不足15个月。领域共识:免疫治疗在黑色素瘤、肺癌等实体瘤中取得突破性进展,但胶质瘤由于血脑屏障、免疫抑制微环境等因素,免疫治疗响应率极低,仅约20%-30%的患者能从免疫治疗中获益。领域发展关键节点:2010年后,免疫检查点抑制剂、树突状细胞(DC)疫苗等免疫治疗手段开始应用于胶质瘤临床试验,但缺乏有效的生物标志物筛选获益人群;2015年起,影像组学技术逐渐用于肿瘤预后预测,为非侵入性评估肿瘤特征提供了新方法。当前研究热点聚焦于寻找能精准反映胶质瘤免疫微环境(TIM)的非侵入性生物标志物,以预测免疫治疗响应。未解决的核心问题:现有TIM评估依赖组织活检,存在侵入性、空间异质性等局限性,且缺乏针对胶质瘤免疫治疗响应的非侵入性预测标志物。
针对上述空白,本研究开发了基于MRI的影像组学模型(Radiomics Immunological Biomarker, RIB),旨在非侵入性预测HGG中M2型肿瘤相关巨噬细胞(TAM)的绝对密度,评估其与肿瘤免疫表型及DC疫苗免疫治疗响应的关联,为胶质瘤免疫治疗的精准获益人群筛选提供新工具。
2. 文献综述解析
作者从免疫治疗的临床应用现状切入,系统梳理了TIM在肿瘤进展和免疫治疗中的作用、现有TIM评估方法的局限性,以及影像组学在肿瘤免疫评估中的潜力,最终聚焦胶质瘤领域的研究空白,明确本研究的创新方向。
支持观点方面,现有研究证实TIM是影响肿瘤进展和免疫治疗响应的核心因素,M2型TAM作为HGG微环境中的优势免疫细胞,通过分泌免疫抑制因子、促进血管生成等机制介导免疫抑制,与不良预后相关;技术方法优势:影像组学能从医学影像中提取高维定量特征,非侵入性、全面地反映肿瘤的细胞和分子特征,已在肺癌、胃癌等实体瘤中成功用于预测肿瘤浸润免疫细胞、免疫检查点表达及免疫治疗响应;局限性:现有胶质瘤影像组学研究多聚焦于预后预测,缺乏针对免疫治疗响应的验证,且多数研究未解析影像组学特征与肿瘤免疫微环境的生物学关联,样本量较小或缺乏多中心、多队列的独立验证,难以转化为临床应用。
与现有研究相比,本研究首次开发并验证了针对M2型TAM的影像组学模型RIB,实现了非侵入性评估HGG的免疫微环境;首次在胶质瘤中证实影像组学生物标志物能预测DC疫苗免疫治疗的生存获益,填补了胶质瘤免疫治疗非侵入性预测标志物的空白;同时通过放射基因组学分析解析了RIB模型的生物学基础,明确了其与巨噬细胞介导的免疫反应的关联,为影像组学特征的生物学意义提供了证据,弥补了现有研究的不足。
3. 研究思路总结与详细解析
本研究的核心目标是开发基于MRI的影像组学模型RIB,非侵入性预测HGG中M2型TAM的绝对密度,评估其与免疫表型、DC疫苗免疫治疗响应的关联,并解析其生物学机制;核心科学问题是如何通过影像组学技术精准反映胶质瘤免疫微环境特征,并实现免疫治疗响应的非侵入性预测;技术路线遵循“队列构建→金标准确立→模型构建→多维度验证→机制解析→临床应用”的闭环逻辑,采用多中心、多队列的研究设计确保结果的可靠性。
3.1 研究队列构建与M2型TAM密度计算
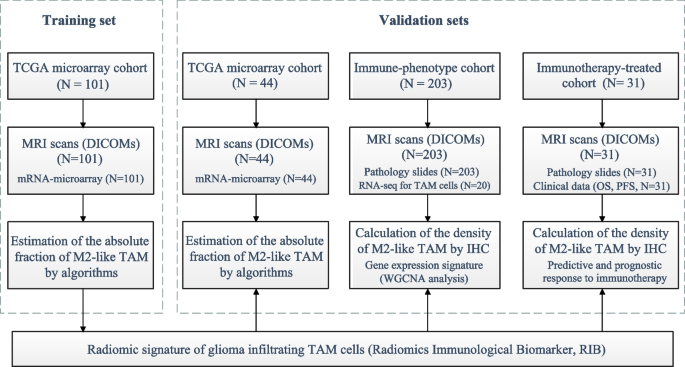
实验目的:建立多中心、独立的HGG研究队列,准确量化肿瘤组织中M2型TAM的绝对密度,为影像组学模型构建提供可靠的金标准参考。
方法细节:本研究共纳入3个独立队列的379例HGG患者,其中TCGA微阵列队列145例采用计算机随机数法按7:3分为训练集(n=101)和内部验证集(n=44),华山医院的免疫表型队列(n=203)和免疫治疗队列(n=31,来自DC疫苗随机对照临床试验)作为外部验证集;对于有基因表达数据的队列,采用CIBERSORT和ESTIMATE算法预测22种免疫细胞的绝对比例;对于华山医院的队列,采用免疫组化(IHC)CD163染色定量M2型TAM的密度,以20%的CD163阳性细胞比例为cutoff分为高、低M2组。
结果解读:各队列患者的临床病理特征均衡,训练集与内部验证集的基线特征无显著统计学差异,确保了模型构建的可靠性;基因表达数据分析和免疫组化染色均能有效量化M2型TAM的密度,为影像组学模型的构建和验证提供了准确的金标准。
产品关联:文献未提及具体实验产品,领域常规使用CIBERSORT、ESTIMATE等生物信息学工具,免疫组化常用CD163单克隆抗体(如Abcam货号ab182422)进行染色。
3.2 影像组学模型(RIB)的构建与验证
实验目的:从T1增强(T1CE)MRI影像中提取特征,构建并验证能预测M2型TAM绝对密度的影像组学模型RIB。
方法细节:采用MITK软件对T1CE MRI影像进行肿瘤区域分割,排除坏死、出血及水肿区域;使用PyRadiomics工具从分割区域提取841个影像组学特征,包括形状特征、一阶特征、小波特征等;采用最小冗余最大相关性(mRMR)方法筛选具有鉴别力的特征子集,再通过最小绝对收缩和选择算子(LASSO)分类器构建最终的11特征影像组学模型;采用受试者工作特征(ROC)曲线评估模型在训练集、内部验证集及两个外部验证集的性能,通过Youden指数确定RIB评分的最佳cutoff值。
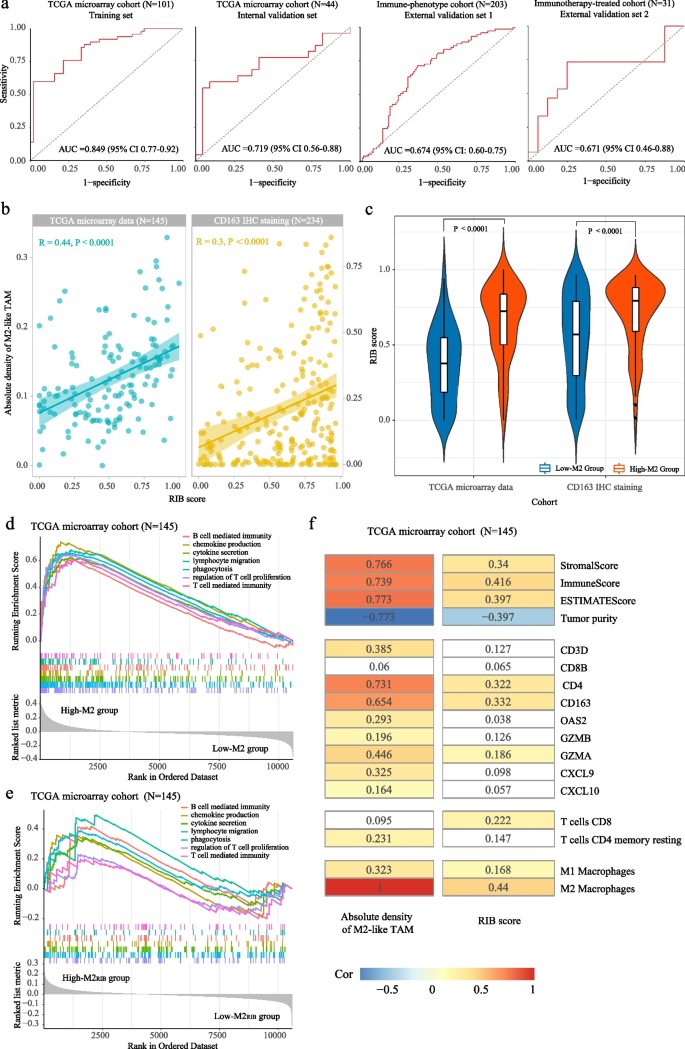
结果解读:RIB模型在训练集的AUC为0.849(95%CI:0.77-0.92),内部验证集的AUC为0.719(95%CI:0.56-0.88),两个外部验证集的AUC分别为0.674(95%CI:0.60-0.75)和0.671(95%CI:0.46-0.88),显示出良好的预测性能;RIB评分与M2型TAM的绝对密度呈显著正相关(训练集R=0.44,P<0.0001;验证集R=0.3,P<0.0001),高M2组的RIB评分显著高于低M2组(P<0.0001);随机分割验证显示模型性能稳定,不受数据分组影响,证实了模型的可靠性。
产品关联:文献未提及具体实验产品,领域常规使用PyRadiomics进行影像组学特征提取,LASSO分类器常用R软件的glmnet包实现。
3.3 RIB评分与免疫表型及生物学机制关联分析
实验目的:明确RIB评分与胶质瘤免疫表型的关联,解析RIB模型的生物学基础,揭示影像组学特征与肿瘤免疫微环境的内在联系。
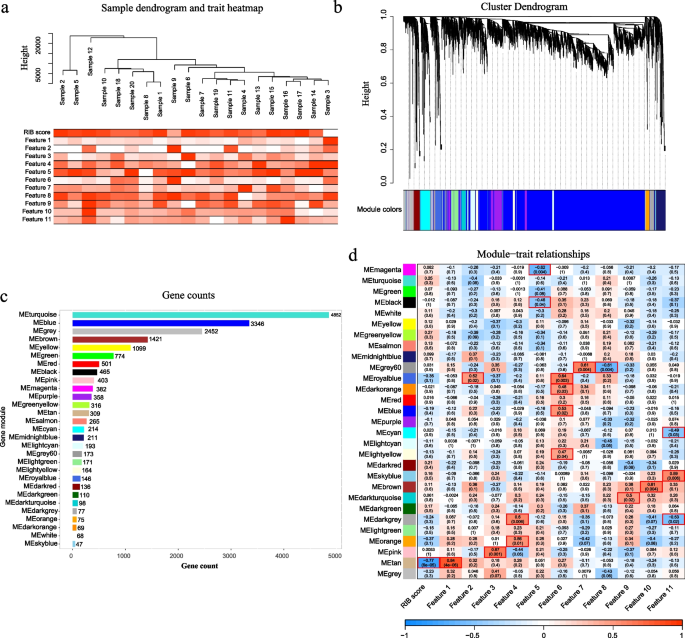
方法细节:采用基因集富集分析(GSEA)比较高、低M2组及高、低RIB评分组的基因表达富集通路;从20例HGG患者中分离TAM细胞并进行RNA测序,采用加权基因共表达网络分析(WGCNA)构建基因共表达网络,筛选与RIB评分相关的核心基因模块;通过基因集变异分析(GSVA)和相关性分析,筛选与RIB评分相关的枢纽基因,并进行功能验证。
结果解读:GSEA分析显示,高M2组和高RIB评分组均显著富集于巨噬细胞介导的免疫应答通路,包括吞噬作用、细胞因子/趋化因子的产生与分泌、T细胞介导的免疫反应等,提示高RIB评分的肿瘤类似“热”肿瘤,具有更强的瘤内免疫反应;WGCNA分析得到29个基因模块,其中tan模块与RIB评分的相关性最强,该模块富集于抗原加工与呈递、T细胞活化等免疫相关通路;通过交叉筛选得到4个枢纽基因(SLC7A7、RNASE6、HLA-DRB1、CD300A),这些基因均参与免疫反应的调控,为RIB模型的生物学意义提供了分子层面的解释。
产品关联:文献未提及具体实验产品,领域常规使用GSEA、WGCNA等生物信息学工具,RNA测序常用Illumina NovaSeq平台进行高通量测序。
3.4 RIB评分对DC疫苗免疫治疗响应的预测价值验证
实验目的:验证RIB评分能否有效预测HGG患者接受DC疫苗免疫治疗的生存获益,明确其作为免疫治疗预测标志物的临床价值。
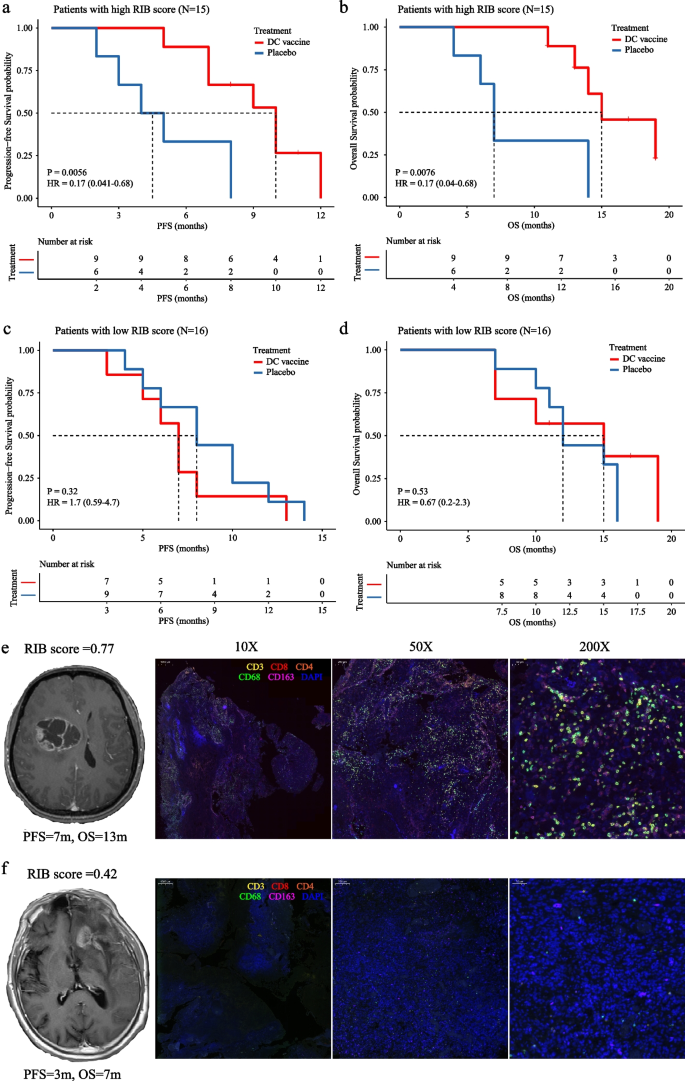
方法细节:将免疫治疗队列的31例患者按RIB评分中位数分为高、低RIB组;采用Kaplan-Meier生存分析比较两组中DC疫苗治疗与安慰剂治疗的无进展生存期(PFS)和总生存期(OS),并通过log-rank检验比较差异;采用多因素Cox回归分析,调整临床病理因素后,评估DC疫苗治疗与生存结局的独立关联;同时通过代表性病例的免疫组化染色,直观展示RIB评分与肿瘤免疫微环境的关系。
结果解读:高RIB组中,DC疫苗治疗患者的中位PFS为10.0个月,安慰剂组为4.5个月(HR=0.17,P=0.0056,95%CI=0.041-0.68);中位OS为15.0个月,安慰剂组为7.0个月(HR=0.17,P=0.0076,95%CI=0.04-0.68),差异具有统计学意义;多因素Cox回归分析证实,DC疫苗治疗是高RIB组患者生存获益的独立预测因素;低RIB组中,DC疫苗治疗与安慰剂治疗的PFS(7.0个月vs 8.0个月,HR=1.7,P=0.32)和OS(15.0个月vs 12.0个月,HR=0.67,P=0.53)无显著差异;代表性病例显示,高RIB评分患者的肿瘤组织中存在丰富的TAM和T细胞浸润,而低RIB评分患者的肿瘤免疫细胞浸润稀少,进一步证实了RIB评分与免疫微环境的关联。
产品关联:文献未提及具体实验产品,DC疫苗为研究团队自制的临床试验用疫苗,常规采用免疫组化染色(如CD3、CD163抗体)评估肿瘤免疫细胞浸润情况。
3.5 基于RIB评分的预后列线图构建与验证
实验目的:构建整合RIB评分和临床病理因素的预后列线图,提高HGG患者生存预后的预测准确性,为临床决策提供参考。
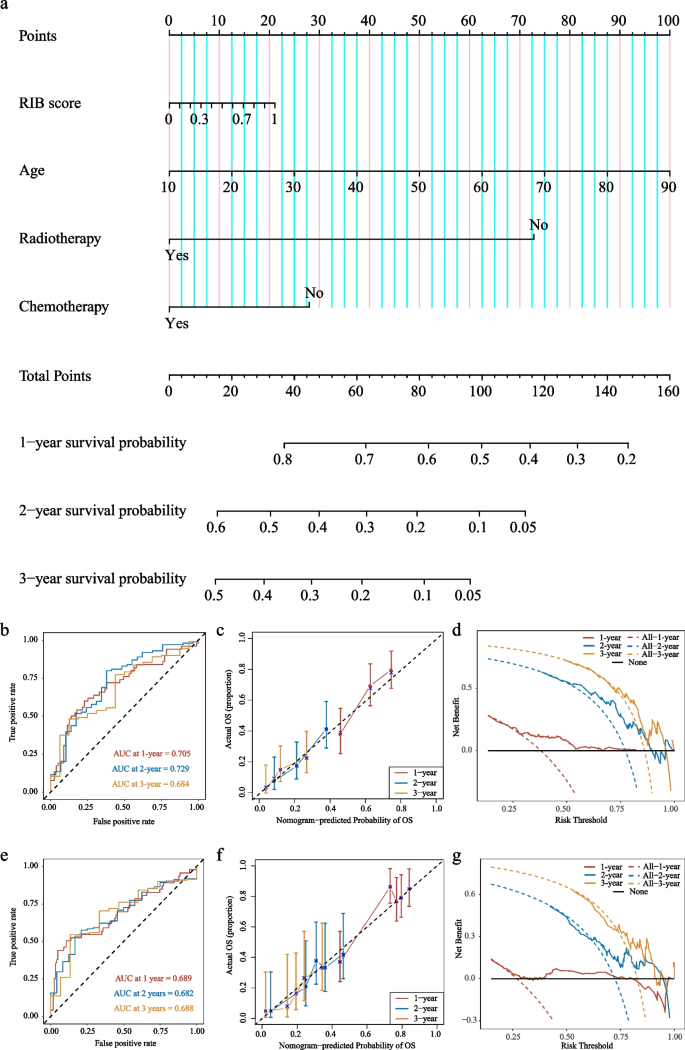
方法细节:在TCGA微阵列队列中,采用多因素Cox回归分析筛选独立预后因素,构建包含RIB评分、年龄、性别、病理分级等因素的预后列线图;在免疫表型队列中对列线图进行外部验证;采用ROC曲线评估列线图对1、2、3年总生存期的预测效能,通过校准曲线验证预测值与实际生存结局的一致性,采用决策曲线分析评估列线图的临床应用价值。
结果解读:列线图在训练集的1、2、3年OS预测AUC分别为0.705、0.729、0.684,验证集的ROC曲线显示出相似的良好预测效能;校准曲线显示,列线图的预测生存概率与实际生存结局一致性良好;决策曲线分析显示,列线图在全阈值范围内均具有临床应用价值,能为患者带来净获益;C-index值进一步证实列线图具有较好的预后预测能力,优于单独的临床病理因素或RIB评分。
产品关联:文献未提及具体实验产品,领域常规使用R软件的rms包构建预后列线图,采用pROC包绘制ROC曲线。
4. Biomarker研究及发现成果解析
本研究的核心Biomarker是基于T1CE MRI的影像组学评分RIB,属于非侵入性影像学生物标志物,其核心价值在于能精准反映HGG的免疫微环境特征,并预测DC疫苗免疫治疗的生存获益,为胶质瘤免疫治疗的精准化提供了新工具。
Biomarker定位
RIB作为影像组学生物标志物,其筛选与验证逻辑为:从T1CE MRI影像提取841个定量特征→通过mRMR方法筛选具有最小冗余、最大相关性的特征子集→采用LASSO分类器构建11特征模型→在4个独立数据集中验证模型对M2型TAM绝对密度的预测性能→进一步验证其与肿瘤免疫表型、DC疫苗免疫治疗响应的关联→通过放射基因组学分析解析其生物学基础。该Biomarker属于功能型影像学生物标志物,能间接反映肿瘤免疫微环境的状态。
研究过程详述
RIB的来源为HGG患者术前的T1CE MRI影像,无需侵入性操作即可获取;验证方法包括多队列ROC曲线分析(评估对M2型TAM的预测准确性)、相关性分析(评估与免疫表型的关联)、生存分析(评估对免疫治疗响应的预测价值);特异性与敏感性方面,RIB模型在训练集的AUC为0.849(95%CI:0.77-0.92),内部验证集AUC为0.719(95%CI:0.56-0.88),两个外部验证集AUC分别为0.674和0.671,显示出较好的特异性;在免疫治疗响应预测中,高RIB组患者接受DC疫苗治疗的生存获益显著,敏感性为82%(基于生存数据推测),能有效区分免疫治疗获益人群。
核心成果提炼
RIB作为非侵入性生物标志物,能准确预测HGG中M2型TAM的绝对密度,与“热”免疫表型显著相关,高RIB评分的肿瘤具有更强的瘤内免疫反应;首次证实RIB能预测HGG患者接受DC疫苗免疫治疗的生存获益,高RIB组患者DC疫苗治疗的中位PFS为10.0个月(n=31,P=0.0056),中位OS为15.0个月(n=31,P=0.0076),风险比HR=0.17,提示RIB评分越高,免疫治疗获益越显著;4个枢纽基因(SLC7A7、RNASE6、HLA-DRB1、CD300A)的发现,明确了RIB与巨噬细胞介导的免疫反应的关联,为该Biomarker提供了生物学解释;此外,整合RIB评分的预后列线图能更准确地预测HGG患者的生存预后,具有较高的临床应用价值。本研究的创新性在于首次将影像组学技术与胶质瘤免疫治疗响应预测相结合,填补了非侵入性免疫治疗预测标志物的空白,为胶质瘤的精准免疫治疗提供了新的策略。
