1. 领域背景与文献引入
文献英文标题:METTL3 facilitates immunosurveillance by inhibiting YTHDF2-mediated NLRC5 mRNA degradation in endometrial cancer;发表期刊:Biomarker Research;影响因子:未公开;研究领域:子宫内膜癌肿瘤免疫、RNA m6A修饰
子宫内膜癌是女性生殖系统常见的恶性肿瘤,其发生发展涉及流行病学风险因素与遗传因素的共同作用,近年来肿瘤细胞逃避免疫监视被证实是驱动肿瘤进展的核心机制之一,但具体分子调控通路仍未完全阐明。领域共识:N6-甲基腺苷(m6A)是人类mRNA最丰富的转录后化学修饰,可通过甲基转移酶、去甲基化酶及阅读器蛋白调控mRNA的稳定性、翻译与降解,在多种肿瘤的增殖、侵袭及免疫调控中发挥关键作用。此前研究已发现m6A修饰可通过调控靶基因表达影响子宫内膜癌的增殖能力,但m6A修饰在子宫内膜癌免疫应答中的具体调控机制仍不明确;针对甲基转移酶样3(METTL3)的研究仅揭示其通过AKT通路影响子宫内膜癌的增殖,未涉及免疫逃逸相关功能。因此,METTL3是否参与调控子宫内膜癌的免疫监视过程成为领域空白,本研究旨在明确METTL3在子宫内膜癌免疫应答中的作用及分子机制,为子宫内膜癌的免疫治疗提供新的潜在靶点。
2. 文献综述解析
作者围绕子宫内膜癌的免疫逃逸机制、m6A修饰在肿瘤中的调控功能、METTL3及NLRC5在肿瘤免疫中的作用三个维度对现有研究进行分类评述,系统梳理了领域内的研究进展与未解决问题。
现有研究已明确CD8+T细胞介导的细胞免疫是抗肿瘤免疫的核心力量,子宫内膜癌的免疫逃逸与CD8+T细胞浸润不足密切相关,但具体调控分子及通路仍需深入挖掘;m6A修饰作为mRNA的关键转录后修饰,其优势在于可精准调控靶基因的表达命运,局限性在于不同肿瘤中同一分子的功能可能存在差异,且多数研究未深入到免疫调控层面;针对METTL3的研究,此前仅发现其通过AKT通路影响子宫内膜癌的增殖能力,未涉及免疫相关功能;NLRC5作为先天免疫分子,可调控MHC I类分子介导的免疫应答,被证实是多种肿瘤免疫逃逸的靶点,但在子宫内膜癌中的调控机制尚未明确。
本研究的创新价值在于首次将METTL3与子宫内膜癌的免疫监视过程关联,通过临床样本、细胞模型及动物实验系统揭示了METTL3/YTHDF2/NLRC5轴调控CD8+T细胞介导的抗肿瘤免疫的分子机制,填补了m6A修饰在子宫内膜癌免疫应答中调控机制的空白,为子宫内膜癌的免疫治疗提供了新的潜在靶点,同时拓展了m6A修饰在肿瘤免疫调控中的研究范畴。
3. 研究思路总结与详细解析
本研究的核心目标是明确METTL3在子宫内膜癌免疫监视中的作用及分子机制,核心科学问题为METTL3如何通过m6A修饰调控子宫内膜癌的免疫应答,技术路线遵循“临床样本关联分析→细胞与动物模型功能验证→分子机制解析→结论总结”的闭环逻辑,层层递进验证METTL3/YTHDF2/NLRC5轴的调控作用。
3.1 临床样本队列分析METTL3的表达与临床意义
实验目的:明确METTL3在子宫内膜癌组织中的表达水平,及其与患者预后、CD8+T细胞浸润的相关性。方法细节:采用子宫内膜组织芯片队列,通过免疫组化(IHC)检测METTL3、CD8的表达水平;结合TCGA数据库分析METTL3在子宫内膜癌中的表达差异;采用Kaplan-Meier生存分析评估METTL3表达与患者预后的关系;通过Pearson相关性分析明确METTL3与CD8、NLRC5的表达关联。结果解读:免疫组化及TCGA数据库分析显示,子宫内膜癌组织中METTL3表达显著下调(n=3,P<0.01;TCGA队列P<0.0001);低METTL3表达与患者不良预后相关(组织芯片队列P=0.04,TCGA队列P<0.001);METTL3表达与CD8表达呈正相关(R=0.78,P<2.2e-16),与NLRC5表达也呈正相关(R=0.63,P=5.9e-12)。产品关联:文献未提及具体实验产品,领域常规使用免疫组化试剂盒、数据库分析工具等。
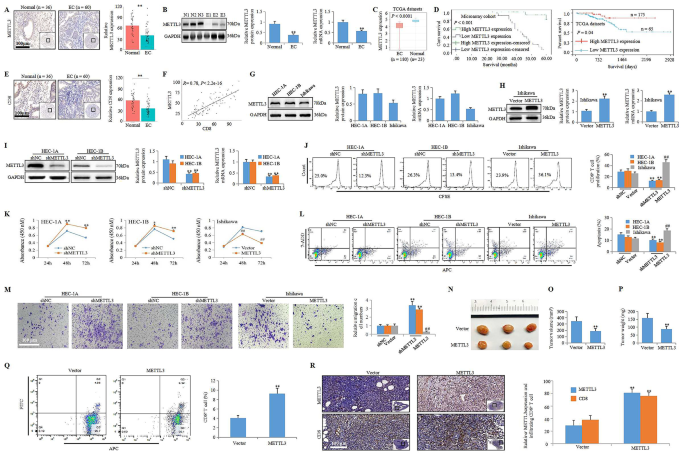
3.2 细胞共培养与动物模型验证METTL3的免疫调控功能
实验目的:验证METTL3对子宫内膜癌细胞增殖、迁移及CD8+T细胞免疫功能的调控作用。方法细节:构建METTL3过表达或敲低的子宫内膜癌细胞系(HEC-1A、HEC-1B、Ishikawa),建立CD8+T细胞-子宫内膜癌细胞共培养体系;采用细胞增殖实验、迁移实验、凋亡实验检测细胞功能;构建子宫内膜癌异种移植小鼠模型,检测METTL3过表达对肿瘤生长及CD8+T细胞浸润的影响。结果解读:在共培养体系中,METTL3过表达可抑制子宫内膜癌细胞增殖、迁移,促进CD8+T细胞增殖(CD8+T细胞增殖率显著升高,P<0.01),促进子宫内膜癌细胞凋亡(凋亡率升高,P<0.01);METTL3敲低则发挥相反作用。在动物模型中,METTL3过表达显著降低肿瘤体积及重量(P<0.01),增加外周血及肿瘤组织中CD8+T细胞比例(P<0.01)。产品关联:文献未提及具体实验产品,领域常规使用细胞转染试剂、细胞增殖检测试剂盒、流式细胞仪等。
3.3 分子机制研究:METTL3对NLRC5的m6A修饰调控
实验目的:明确METTL3调控子宫内膜癌免疫监视的靶基因及m6A修饰机制。方法细节:通过m6A数据库预测NLRC5 mRNA的m6A修饰位点;采用RNA免疫沉淀(RIP)、甲基化RNA免疫沉淀(MeRIP)实验验证METTL3与NLRC5 mRNA的结合及m6A修饰;通过mRNA稳定性实验检测METTL3对NLRC5 mRNA稳定性的影响;采用免疫组化、蛋白免疫印迹(WB)及qRT-PCR检测NLRC5的表达水平。结果解读:m6A数据库预测NLRC5 mRNA存在两个高置信度m6A修饰位点;MeRIP-PCR实验显示,METTL3敲低后NLRC5 mRNA的m6A修饰水平显著降低(P<0.01);RIP实验证实METTL3可直接结合NLRC5 mRNA(P<0.01);METTL3过表达可显著上调NLRC5的mRNA及蛋白表达水平(P<0.01),并延长NLRC5 mRNA的半衰期(P<0.01);METTL3敲低则导致NLRC5表达下调及mRNA稳定性降低。产品关联:文献未提及具体实验产品,领域常规使用RIP试剂盒、MeRIP试剂盒、蛋白免疫印迹相关试剂等。
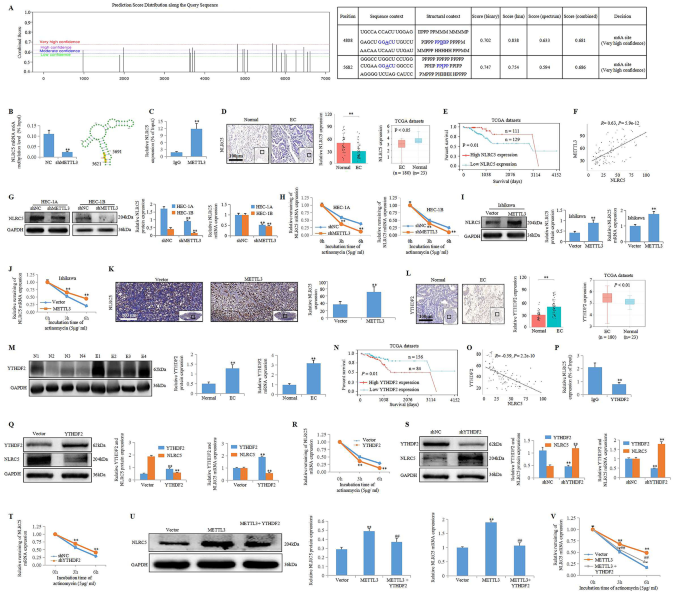
3.4 YTHDF2介导NLRC5降解的机制验证
实验目的:明确m6A阅读器蛋白YTHDF2在METTL3调控NLRC5表达中的作用。方法细节:通过临床样本及TCGA数据库分析YTHDF2的表达水平及与患者预后的关系;采用RIP实验验证YTHDF2与NLRC5 mRNA的结合;通过过表达或敲低YTHDF2,检测其对NLRC5表达及mRNA稳定性的影响;通过共转染实验验证METTL3与YTHDF2的协同作用。结果解读:临床样本及TCGA数据库显示,YTHDF2在子宫内膜癌组织中表达上调(P<0.01),高表达与患者不良预后相关(P=0.01);YTHDF2与NLRC5表达呈负相关(R=-0.59,P=2.2e-10);RIP实验证实YTHDF2可结合NLRC5 mRNA(P<0.01);YTHDF2过表达可下调NLRC5表达并降低其mRNA稳定性(P<0.01),敲低YTHDF2则发挥相反作用;共转染实验显示,YTHDF2过表达可逆转METTL3过表达对NLRC5的上调作用(P<0.01),证实METTL3通过抑制YTHDF2介导的NLRC5降解发挥功能。产品关联:文献未提及具体实验产品,领域常规使用细胞转染试剂、qRT-PCR试剂盒等。
4. Biomarker研究及发现成果
本研究鉴定出METTL3、YTHDF2、NLRC5三个可作为子宫内膜癌诊断及预后的潜在生物标志物,通过临床样本、细胞及动物实验系统验证了其表达特征、临床意义及调控逻辑,为子宫内膜癌的精准诊断及预后评估提供了新的分子靶点。
Biomarker定位:METTL3、YTHDF2、NLRC5均为分子生物标志物(mRNA/蛋白水平),筛选与验证逻辑为“临床样本芯片+TCGA数据库初步筛选→细胞模型验证表达调控关系→动物模型验证功能相关性”的完整链条。其中METTL3与NLRC5为抑癌相关标志物,其低表达提示子宫内膜癌进展风险升高;YTHDF2为促癌相关标志物,其高表达提示患者不良预后。
研究过程详述:Biomarker来源为临床子宫内膜癌组织样本及细胞系;验证方法包括免疫组化、qRT-PCR、蛋白免疫印迹、RNA免疫沉淀、甲基化RNA免疫沉淀等;特异性与敏感性数据方面,METTL3与CD8的表达相关性R=0.78(P<2.2e-16),与NLRC5的相关性R=0.63(P=5.9e-12),YTHDF2与NLRC5的负相关性R=-0.59(P=2.2e-10);预后评估显示,低METTL3表达患者的总生存期显著缩短(组织芯片队列P=0.04,TCGA队列P<0.001),低NLRC5表达患者预后不良(TCGA队列P=0.01),高YTHDF2表达患者预后不良(TCGA队列P=0.01)。
核心成果提炼:METTL3、YTHDF2、NLRC5可作为子宫内膜癌的潜在诊断及预后生物标志物,其中METTL3与NLRC5的低表达、YTHDF2的高表达提示患者不良预后;本研究首次揭示了METTL3通过m6A修饰抑制YTHDF2介导的NLRC5降解,进而促进CD8+T细胞介导的抗肿瘤免疫的功能关联,为子宫内膜癌的免疫治疗提供了新的靶点;统计学结果显示,各指标的相关性及预后分析均具有显著统计学意义(P值均<0.05),样本量涵盖临床组织芯片队列及TCGA大样本队列,结论具有较高的可靠性。
