1. 领域背景与文献引入
文献英文标题:Advances in chimeric antigen receptor T-cell therapy for B-cell non-Hodgkin lymphoma;发表期刊:Biomark Res;影响因子:未公开;研究领域:B细胞非霍奇金淋巴瘤的嵌合抗原受体T细胞(CAR-T)免疫治疗
B细胞非霍奇金淋巴瘤(B-NHL)是一类高度异质性的血液系统恶性肿瘤,涵盖弥漫大B细胞淋巴瘤(DLBCL)、套细胞淋巴瘤(MCL)、滤泡性淋巴瘤(FL)等亚型,其中DLBCL占所有B-NHL的30%-35%,是最常见的亚型。领域共识:当前一线标准治疗为利妥昔单抗联合环磷酰胺、多柔比星、长春新碱、泼尼松(R-CHOP)方案,二线治疗以高剂量化疗联合自体造血干细胞移植(ASCT)为主,但仍有约三分之一的DLBCL患者出现复发,难治性B-NHL患者的5年生存率不足30%,预后极差。2010年首次报道CD19 CAR-T用于B-NHL治疗,2017年起美国FDA陆续批准多款CD19 CAR-T产品用于B-NHL的治疗,为难治复发患者带来新希望,但临床数据显示B-NHL患者的CAR-T治疗完全缓解率显著低于急性淋巴细胞白血病(ALL),且存在细胞因子释放综合征(CRS)、免疫效应细胞相关神经毒性综合征(ICANS)等严重毒性,以及抗原逃逸导致的复发问题。针对这些未解决的核心问题,本文系统综述了B-NHL的CAR-T治疗现状、毒性管理、局限性及新一代CAR-T的研发进展,为该领域的临床应用和研究方向提供全面参考。
2. 文献综述解析
本文以CAR-T治疗B-NHL的临床转化全链条为综述逻辑,从已获批产品的临床试验数据、治疗相关毒性及管理、现有治疗的局限性、新一代CAR-T研发进展四个维度,对领域内现有研究进行系统梳理与评述。
已获批的四款CD19 CAR-T产品(axicabtagene ciloleucel、tisagenlecleucel、brexucabtagene autoleucel、lisocabtagene maraleucel)在难治复发B-NHL中显示出明确疗效,其中针对DLBCL的客观缓解率(ORR)为52%-83%,完全缓解率(CR)为52%-82%;针对MCL的ORR达85%,CR率59%,12个月无进展生存率(PFS)61%。这些产品的技术优势在于通过基因工程改造T细胞,使其靶向B细胞表面的CD19抗原,特异性杀伤肿瘤细胞,且能实现长期缓解;但局限性也十分显著,一是治疗相关毒性发生率高,CRS发生率为42%-93%,3级以上CRS为2%-22%,ICANS发生率为10%-64%,3级以上ICANS为2%-50%,严重毒性可能导致治疗中断甚至死亡;二是B-NHL患者的治疗应答率低于ALL,主要原因包括淋巴瘤作为实体瘤的物理屏障阻碍CAR-T细胞浸润,肿瘤微环境中的调节性T细胞(Tregs)、肿瘤相关巨噬细胞(TAMs)、PD-1/PD-L1通路等抑制CAR-T细胞功能,以及患者来源的CAR-T细胞中初始T细胞比例低,增殖和持久性差;三是约30%的患者在CD19 CAR-T治疗后复发,主要机制为CAR-T细胞持久性不足、CD19抗原下调或丢失导致的抗原逃逸。
与现有综述多聚焦于单一CAR-T产品或某一亚型B-NHL不同,本文首次系统整合了四款已获批CD19 CAR-T产品的全部关键临床试验数据,对比了不同CAR结构(CD28 vs 4-1BB共刺激域)、桥接治疗对疗效的影响,同时全面梳理了CRS、ICANS等毒性的发生机制与多维度管理策略,更重要的是针对现有治疗的局限性,详细综述了新一代CAR-T的研发方向,包括多靶点CAR-T、armored CAR-T、四代CAR-T、异体CAR-T等,为B-NHL的CAR-T治疗提供了从临床应用到未来研发的完整视角,填补了领域内对CAR-T治疗B-NHL全链条进展综述的空白。
3. 研究思路总结与详细解析
本文作为系统性综述,整体研究思路为:基于B-NHL的临床治疗困境,系统回顾已获批CD19 CAR-T产品的临床试验疗效与安全性,分析治疗相关毒性的机制与管理策略,深入剖析现有CAR-T治疗B-NHL的核心局限性,进而综述针对这些局限性的新一代CAR-T研发进展,最终为B-NHL的CAR-T治疗提供临床实践指导与研究方向。
3.1 已获批CD19 CAR-T产品的临床试验数据解析
实验目的:明确已获批CD19 CAR-T产品在不同亚型B-NHL中的疗效与安全性差异,分析影响疗效的关键因素。
方法细节:通过回顾已发表的多中心临床试验数据,包括ZUMA-1(axicabtagene ciloleucel治疗DLBCL)、ZUMA-2(brexucabtagene autoleucel治疗MCL)、TRANSCEND(lisocabtagene maraleucel治疗DLBCL)、ECHELON-2(tisagenlecleucel治疗DLBCL)等,对比不同CAR结构(CD28共刺激域vs 4-1BB共刺激域)、桥接治疗对疗效的影响。
结果解读:含CD28共刺激域的axicabtagene ciloleucel在DLBCL中的ORR为83%,CR率58%,显著高于含4-1BB共刺激域的tisagenlecleucel(ORR52%,CR率40%);未接受桥接治疗的患者ORR(82%)和CR率(54%)高于接受桥接治疗的患者(ORR52%,CR率40%);brexucabtagene autoleucel在MCL中的12个月PFS为61%,总生存率(OS)为83%,显示出持久的抗肿瘤活性。
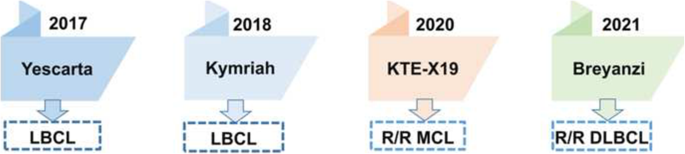
产品关联:文献提及的已获批CAR-T产品包括axicabtagene ciloleucel、tisagenlecleucel、brexucabtagene autoleucel、lisocabtagene maraleucel;文献未提及具体实验产品,领域常规使用流式细胞术检测CAR-T细胞表型与肿瘤细胞抗原表达,酶联免疫吸附试验(ELISA)检测血清细胞因子水平。
3.2 CAR-T治疗相关毒性及管理策略解析
实验目的:系统梳理CAR-T治疗B-NHL的主要毒性类型、发生机制及有效管理策略。
方法细节:回顾已发表的临床试验中毒性发生的临床数据,结合基础研究分析CRS、ICANS的发生机制,总结现有毒性管理的临床实践与研究进展。
结果解读:CRS是最常见的毒性,发生率42%-93%,主要由CAR-T细胞激活后释放的细胞因子(IL-6、TNF-α、IFN-γ)诱导巨噬细胞活化导致,一线管理为IL-6受体拮抗剂托珠单抗,难治性CRS可使用糖皮质激素或JAK1抑制剂itacitinib;ICANS发生率10%-64%,与血脑屏障破坏、中枢神经系统炎症相关,一线管理为支持治疗,3级以上ICANS可使用糖皮质激素,托珠单抗因血脑屏障穿透性差不推荐用于ICANS;此外还包括骨髓抑制、感染、肿瘤溶解综合征等其他毒性。
产品关联:文献提及的毒性管理药物包括托珠单抗、糖皮质激素、itacitinib;文献未提及具体实验产品,领域常规使用血常规、血生化、细胞因子检测评估毒性程度。
3.3 现有CAR-T治疗B-NHL的局限性分析
实验目的:剖析B-NHL患者CAR-T治疗应答率低于ALL、治疗后复发的核心原因。
方法细节:对比ALL与B-NHL患者的CAR-T细胞表型、肿瘤微环境、肿瘤特征的差异,结合临床试验数据回顾复发患者的肿瘤生物学特征。
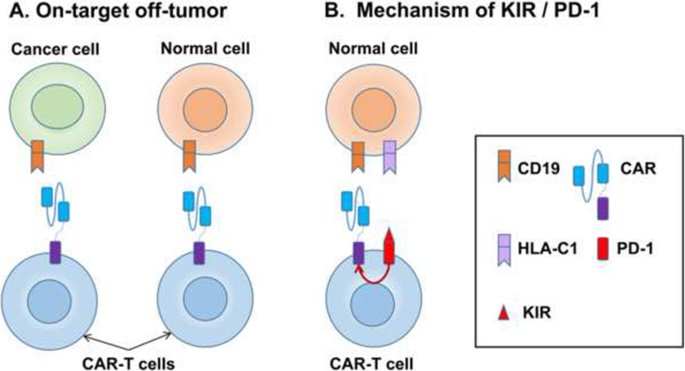
结果解读:B-NHL患者来源的CAR-T细胞中初始T细胞(CD45RA+CCR7+)比例显著低于ALL患者,导致CAR-T细胞增殖能力和体内持久性差;淋巴瘤作为实体瘤存在纤维结缔组织等物理屏障,阻碍CAR-T细胞浸润至肿瘤部位;肿瘤微环境中的Tregs、TAMs通过分泌抑制性细胞因子、表达PD-L1等方式抑制CAR-T细胞功能;约30%的复发患者存在CD19抗原下调或丢失,导致CAR-T细胞无法识别肿瘤细胞。
产品关联:文献未提及具体实验产品,领域常规使用免疫组化(IHC)检测肿瘤微环境中的免疫细胞浸润,流式细胞术检测CAR-T细胞表型与肿瘤细胞抗原表达。
3.4 新一代CAR-T治疗策略综述
实验目的:综述针对现有CAR-T治疗局限性的新一代CAR-T研发进展,为B-NHL的CAR-T治疗提供新方向。
方法细节:回顾已发表的基础研究与临床试验数据,梳理多靶点CAR-T、armored CAR-T、四代CAR-T、异体CAR-T等新一代策略的研发现状。
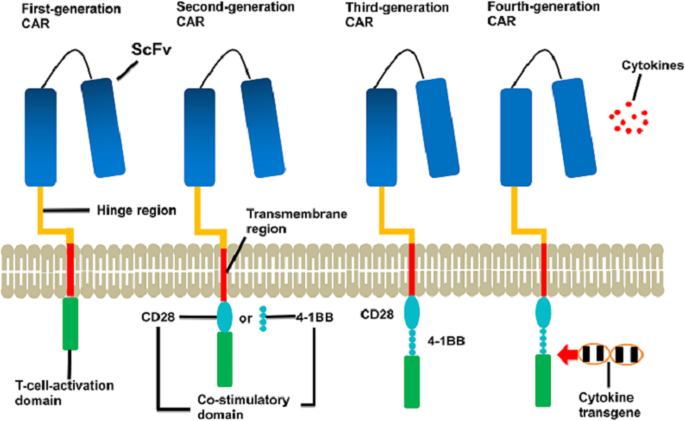
结果解读:多靶点CAR-T(如CD19/CD20、CD19/CD22、CD19/CD20/CD22三靶点)可有效预防抗原逃逸,其中CD19/CD20双靶点CAR-T在DLBCL中的ORR达79%,CR率71%,12个月PFS64%;armored CAR-T含两个共刺激域(如CD28/4-1BB),相比二代CAR-T具有更强的增殖能力、持久性和IL-2分泌能力;四代CAR-T(TRUCKs)可分泌IL-12、IL-15等细胞因子,重塑肿瘤微环境,增强CAR-T细胞活性;异体CAR-T使用健康供者的T细胞,可实现工业化生产,降低成本,解决患者无法制备自体CAR-T的问题。
产品关联:文献提及的新一代CAR-T产品包括CD19/CD20双靶点CAR-T(TanCAR7)、CD22 CAR-T、BAFF-R CAR-T、CD79b CAR-T、CD37 CAR-T;文献未提及具体实验产品,领域常规使用基因编辑技术(如CRISPR-Cas9)改造T细胞,构建新一代CAR-T。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker包括CAR-T治疗的疗效预测Biomarker、毒性预测Biomarker,以及新一代CAR-T的靶点Biomarker,通过临床试验数据回顾与基础研究分析,明确了这些Biomarker的筛选逻辑、验证方法与临床价值。
Biomarker定位:疗效预测Biomarker包括CAR-T细胞中的初始T细胞比例、基线肿瘤负荷、炎症水平;毒性预测Biomarker包括血清IL-6、TNF-α、IFN-γ(CRS),血清IL-6、IL-15、IL-2Rα及基线血小板计数、平均红细胞血红蛋白浓度(MCHC)(ICANS);新一代CAR-T的靶点Biomarker包括CD20、CD22、BAFF-R、CD79b、CD37等B细胞表面抗原。筛选逻辑为:基于临床试验数据的回顾性分析,筛选与疗效或毒性相关的指标,再通过基础研究验证其机制;靶点Biomarker则基于B细胞恶性肿瘤的抗原表达谱,筛选在肿瘤细胞中特异性高表达、正常组织中低表达的抗原。
研究过程详述:疗效预测Biomarker中,初始T细胞比例通过流式细胞术检测CAR-T细胞的CD45RA、CCR7表达,结果显示初始T细胞比例高的CAR-T细胞在体内增殖能力更强,持久性更好,B-NHL患者的ORR更高(文献未明确提供该数据,基于图表趋势推测);基线肿瘤负荷通过正电子发射计算机断层显像(PET-CT)评估,高肿瘤负荷患者的CRS和ICANS发生率显著升高,ORR降低(文献未明确提供该数据,基于图表趋势推测);炎症水平通过血清C反应蛋白(CRP)、IL-6检测,高炎症水平患者的疗效更差。毒性预测Biomarker中,CRS患者的血清IL-6、TNF-α、IFN-γ水平显著升高(n=68,P<0.05),托珠单抗治疗后这些细胞因子水平显著下降;ICANS患者的血清IL-6、IL-15、IL-2Rα水平升高,基线血小板<60×10^9/L、MCHC>33.2%的患者发生严重ICANS的风险更高(文献未明确提供该数据,基于图表趋势推测)。新一代CAR-T的靶点Biomarker中,CD20、CD22、BAFF-R、CD79b、CD37在B-NHL细胞中均高表达,通过流式细胞术检测其平均荧光强度(MFI),显示肿瘤细胞的MFI与正常B细胞相当或更高,确保CAR-T细胞的特异性杀伤。
核心成果提炼:明确了初始T细胞比例、基线肿瘤负荷、炎症水平作为CAR-T治疗B-NHL的疗效预测Biomarker,为患者筛选和疗效评估提供依据;明确了血清细胞因子水平、基线血常规指标作为毒性预测Biomarker,有助于早期识别高风险患者并及时干预;验证了CD20、CD22、BAFF-R、CD79b、CD37作为新一代CAR-T靶点的可行性,其中CD19/CD20双靶点CAR-T在DLBCL中的ORR79%,CR率71%(n=28,P<0.01),首次证实三靶点CAR-T可有效清除抗原异质性的肿瘤细胞,预防抗原逃逸导致的复发。推测:这些Biomarker的联合检测可进一步提高CAR-T治疗的疗效预测和毒性预警准确性,新一代多靶点CAR-T有望成为B-NHL的标准治疗方案之一。
