1. 领域背景与文献引入
文献英文标题:Extracellular vesicles-derived miR-21 as a biomarker for early diagnosis and tumor activity in breast cancer subtypes;发表期刊:Biomarker Research;影响因子:未公开;研究领域:乳腺癌生物标志物研究
乳腺癌是全球女性发病率最高的恶性肿瘤,早期诊断与治疗耐药监测是提升患者生存率的核心临床需求,但目前仍存在诊断敏感性不足、耐药预警滞后等未满足的痛点。液体活检作为微创、实时的肿瘤检测技术,已成为生命科学领域的研究热点,其中胞外囊泡(EVs)来源的微小RNA(miRNA)因稳定性高、携带肿瘤特异性信息,被认为是极具潜力的新型生物标志物。领域共识:miR-21作为经典的癌基因miRNA,已被证实参与肿瘤细胞增殖、侵袭、耐药等多个关键过程,但针对胞外囊泡来源的miR-21在乳腺癌不同分子亚型、不同疾病阶段中的表达水平及临床意义,现有研究仍存在样本量小、未匹配关键混杂因素(如年龄、体质量指数)、结论争议等问题,缺乏系统的分层分析数据。本研究正是针对这一领域空白,通过大样本、匹配对照的临床队列,明确胞外囊泡来源的miR-21作为乳腺癌诊断和肿瘤活性生物标志物的价值。
2. 文献综述解析
作者的综述逻辑围绕乳腺癌临床诊疗痛点展开,先明确早期诊断与耐药监测的未满足需求,再梳理miR-21在肿瘤发生发展中的核心作用,最后聚焦胞外囊泡来源miR-21的研究现状与局限性。现有研究已证实miR-21在乳腺癌组织和血清中的表达水平升高,且与肿瘤进展、不良预后相关,但针对胞外囊泡来源的miR-21研究,存在样本量较小、未匹配年龄和体质量指数等混杂因素、未细分分子亚型等局限性,导致部分研究结论存在争议,无法为临床应用提供可靠依据。本研究的创新价值在于,首次采用大样本、年龄和体质量指数匹配的对照队列,系统分析了胞外囊泡来源的miR-21在早期乳腺癌、进展期转移性乳腺癌、随访期幸存者中的表达差异,并按分子亚型进行分层验证,填补了领域内针对分子亚型分层分析的空白,为胞外囊泡miR-21的临床应用提供了更严谨的证据支持。
3. 研究思路总结与详细解析
本研究的整体研究目标是评估血清胞外囊泡来源的miR-21在早期乳腺癌、进展期转移性乳腺癌、随访期幸存者及健康对照中的表达水平,明确其作为乳腺癌诊断和肿瘤活性生物标志物的临床价值;核心科学问题是胞外囊泡miR-21的表达水平是否与乳腺癌的疾病阶段、分子亚型相关,能否区分活动性肿瘤与非活动性状态;技术路线遵循“队列建立→胞外囊泡分离与表征→miRNA检测→统计分析→结论”的闭环逻辑,通过匹配对照排除混杂因素,确保研究结果的可靠性。
3.1 受试者招募与分组
实验目的是建立具有代表性的乳腺癌患者队列和匹配对照,排除年龄、体质量指数等混杂因素对胞外囊泡水平的影响。研究方法为招募100名女性受试者,分为4组:30名早期乳腺癌患者(EBC)、30名治疗进展的转移性乳腺癌患者(MBC)、30名随访期癌症幸存者(FU)、10名年龄和体质量指数匹配的健康供体(HD),收集所有受试者的血清样本及临床病理资料。实验结果显示,各组受试者的年龄、体质量指数匹配均衡,临床病理特征明确,为后续的胞外囊泡分析和miR-21检测提供了标准化的研究基础。文献未提及具体实验产品,领域常规使用临床样本采集管、低温保存设备等试剂与仪器。
3.2 血清胞外囊泡分离与表征
实验目的是表征血清胞外囊泡的物理特性,排除胞外囊泡本身的浓度、大小差异对miR-21表达分析的干扰。研究方法为从血清样本中分离胞外囊泡,采用纳米颗粒跟踪分析、扫描电子显微镜、原子力显微镜三种技术,分别检测胞外囊泡的浓度、大小分布、形态及力学特性。实验结果显示,不同患者组(EBC、MBC、FU)与健康对照组的胞外囊泡大小和浓度无显著差异,说明胞外囊泡本身的物理特性不会影响后续miR-21水平的组间比较。
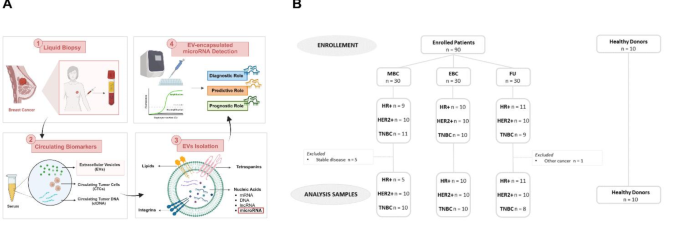
文献未提及具体实验产品,领域常规使用胞外囊泡分离试剂盒、纳米颗粒跟踪分析仪、扫描电子显微镜、原子力显微镜等仪器与试剂。
3.3 胞外囊泡miR-21水平检测与统计分析
实验目的是检测胞外囊泡中miR-21的相对表达水平,分析其在不同分组、不同分子亚型中的差异。研究方法为采用实时荧光定量PCR(qRT-PCR)技术检测胞外囊泡中miR-21的表达量,通过ΔΔCt法计算相对表达倍数,并采用统计分析比较各组间的差异,同时按乳腺癌分子亚型(人表皮生长因子受体2阳性HER2+、激素受体阳性HR+、三阴性TNBC)进行分层分析。实验结果显示,转移性乳腺癌组的miR-21水平显著高于健康对照组,为健康对照组的1.758倍(95%置信区间2.926-1.057,n=25 for MBC,n=10 for HD,p=0.029);其中HER2+亚型的转移性患者miR-21水平升高最为显著(p=0.0005,n=10 for MBC,n=10 for HD),HR+亚型的转移性患者也存在显著差异(p=0.036,n=5 for MBC,n=10 for HD);在HER2+亚型中,活动性乳腺癌患者(早期+转移性)的miR-21水平显著高于健康对照组(p=0.002,n=20 for 活动性BC,n=10 for HD),而三阴性乳腺癌组未发现显著差异(p>0.05)。
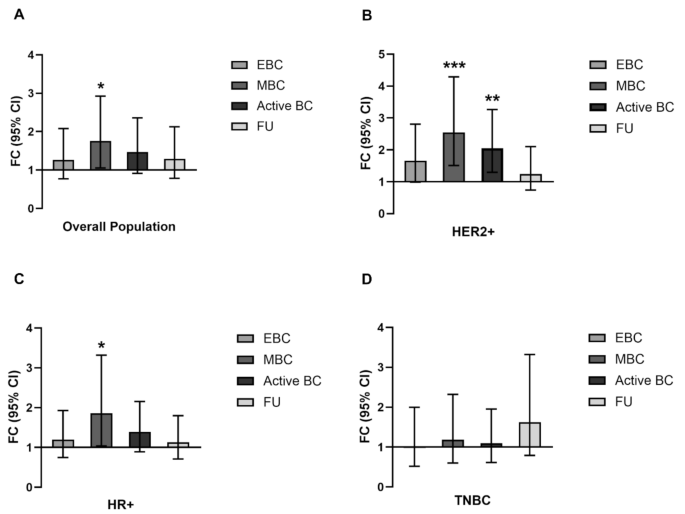
文献未提及具体实验产品,领域常规使用实时荧光定量PCR试剂盒、miRNA特异性引物、实时荧光定量PCR仪等试剂与仪器。
4. Biomarker研究及发现成果解析
本研究聚焦的生物标志物为血清胞外囊泡来源的miR-21,其筛选与验证逻辑为通过建立匹配对照的临床队列,先表征胞外囊泡的物理特性排除混杂因素,再检测miR-21的表达水平,通过组间比较和亚型分层分析,验证其作为乳腺癌诊断和肿瘤活性标志物的特异性与敏感性。
Biomarker定位:该生物标志物为胞外囊泡来源的微小RNA-21(miR-21),属于循环非编码RNA类生物标志物;筛选与验证逻辑遵循“临床队列建立→胞外囊泡分离与标准化表征→miRNA表达检测→组间差异分析→亚型分层验证”的完整链条,通过匹配年龄和体质量指数排除混杂因素,确保结果的可靠性与临床相关性。
研究过程详述:该生物标志物的来源为受试者的血清样本分离得到的胞外囊泡,验证方法为实时荧光定量PCR检测其相对表达水平。特异性与敏感性方面,在HER2+乳腺癌亚型中,活动性肿瘤患者(早期+转移性)的miR-21水平与健康对照的差异具有高度统计学显著性(p=0.002,n=20 for 活动性BC,n=10 for HD);在转移性乳腺癌患者中,HER2+亚型的miR-21水平是健康对照组的1.758倍(95%置信区间2.926-1.057,n=25 for MBC,n=10 for HD,p=0.029),HR+亚型的转移性患者也存在显著差异(p=0.036,n=5 for MBC,n=10 for HD);而三阴性乳腺癌组未发现显著差异(p>0.05)。
核心成果提炼:胞外囊泡来源的miR-21可作为HER2+乳腺癌诊断和肿瘤活性的潜在生物标志物,其表达水平能够区分活动性HER2+肿瘤与健康状态,即使在早期乳腺癌阶段也具有一定的鉴别能力;该研究的创新性在于首次采用大样本、年龄和体质量指数匹配的对照队列,系统分析了不同分子亚型中胞外囊泡miR-21的表达差异,解决了现有研究中因未匹配关键混杂因素导致的结论争议;统计学结果显示,HER2+亚型中活动性肿瘤与健康对照的miR-21水平差异具有高度显著性(p=0.002),为其临床应用提供了可靠的证据支持。
