1. 领域背景与文献引入
文献英文标题:The essential roles of FXR in diet and age influenced metabolic changes and liver disease development: a multi-omics study;发表期刊:Biomark Res;影响因子:未公开;研究领域:代谢性肝病(非酒精性脂肪性肝病、肝细胞癌)与法尼醇X受体(FXR)调控机制。
饮食和衰老是代谢性肝病的核心风险因素,非酒精性脂肪性肝炎(NASH)进展为肝细胞癌(HCC)是当前临床面临的重大难题,目前缺乏有效治疗药物,早期诊断标志物和精准治疗靶点的挖掘迫在眉睫。领域共识:肠道微生物-胆汁酸轴在代谢性肝病发生发展中发挥关键调控作用,FXR作为胆汁酸的核心核受体,其功能缺失与肝脏脂肪变性、炎症及肿瘤进展密切相关,但饮食、衰老与FXR三者交互调控的分子网络尚未完全阐明,也缺乏可用于早期诊断的特异性、多维度标志物。针对这一研究空白,本研究通过整合转录组、代谢组、微生物组多组学技术,系统解析饮食、衰老与FXR功能状态对代谢性肝病的协同调控机制,明确FXR的核心调控作用,筛选兼具诊断潜力与临床预后价值的分子标志物,为代谢性肝病的早期干预提供新的思路。
2. 文献综述解析
作者以“饮食-衰老-FXR-代谢性肝病”的调控轴为核心逻辑,从风险因素、核心调控分子、研究技术三个维度梳理领域现有研究:首先围绕饮食与衰老作为代谢性肝病的诱因,总结了NASH进展为HCC的临床病理特征及现有治疗困境;其次聚焦FXR调控胆汁酸代谢、肠道微生物的研究进展,分类阐述FXR在维持肝脏代谢稳态中的作用及功能缺失后的病理表型;最后概述多组学技术在肝病研究中的应用现状及局限性。
现有研究已证实,FXR敲除小鼠随年龄增长会自发进展为HCC,西式饮食(WD)可加速这一病理进程;肠道微生物通过代谢产物调控胆汁酸信号通路,益生菌、粪菌移植等干预手段可改善肝脏炎症及脂肪变性表型,但这些研究多聚焦单一因素的调控作用,缺乏对饮食、衰老、FXR三者交互作用的系统解析;部分临床前研究发现FXR靶点药物在NASH治疗中的潜力,但临床转化效果不佳,且缺乏对早期诊断标志物的系统筛选与临床验证。
本研究的创新价值在于,首次整合多组学数据构建饮食、衰老与FXR的协同调控网络,同时将小鼠模型数据与人类HCC数据库(TCGA)关联,筛选出跨物种、多维度的联合标志物,弥补了现有研究单一因素分析、缺乏临床转化关联的不足,为代谢性肝病的早期诊断和靶点治疗提供了更系统的理论依据。
3. 研究思路总结与详细解析
本研究的核心目标是明确FXR在饮食和衰老诱导的代谢性肝病中的关键调控作用,筛选潜在诊断标志物与治疗靶点;核心科学问题是饮食、衰老与FXR功能缺失如何通过调控肝脏转录组、代谢组及肠道微生物组的交互作用促进肝病进展;技术路线遵循“模型构建-多组学检测-数据整合-临床关联”的闭环逻辑,通过构建多因素干预的小鼠模型,整合多组学数据解析调控网络,最终验证FXR的功能及标志物的临床价值。
3.1 动物模型构建与病理表型验证
实验目的:构建饮食、年龄、FXR功能状态三因素干预的小鼠模型,验证不同组别的肝脏病理表型差异,为后续多组学分析提供基础。
方法细节:选用C57BL/6N背景的野生型(WT)和FXR敲除(KO)雄性小鼠,断奶后分别饲喂健康对照饮食(CD)或西式饮食(WD),在5、10、15月龄时处死小鼠,收集肝脏、血清、尿液、盲肠内容物样本;检测血清胆固醇、甘油三酯水平,结合已发表的肝脏病理数据(脂肪变性、NASH、肿瘤形成情况)进行表型分析。
结果解读:WD饲喂可诱导所有年龄阶段的WT和FXR KO小鼠出现时间依赖性肝脏脂肪变性;5月龄CD饲喂的FXR KO小鼠已出现脂肪变性,且随年龄增长病理程度加重,WD饲喂的FXR KO小鼠在10月龄进展为NASH,15月龄出现肝脏肿瘤;与CD饲喂的WT小鼠相比,WD饲喂的FXR KO小鼠在5月龄时血清胆固醇和甘油三酯水平已显著升高(文献未明确具体数值,基于图表趋势推测)。
产品关联:文献未提及具体实验产品,领域常规使用的试剂包括血清生化检测试剂盒、组织病理染色试剂等。
3.2 多组学数据采集与差异分析
实验目的:获取肝脏转录组、肝/血清/尿液代谢组、盲肠微生物组数据,解析不同干预因素对分子调控网络的影响。
方法细节:肝脏转录组采用TRIzol试剂提取RNA,进行RNA测序,通过Salmon、DESeq2工具进行差异表达基因(DEGs)分析;肝脏代谢组采用气相色谱-飞行时间质谱(GC-TOF-MS)检测,血清/尿液代谢组采用核磁共振(NMR)检测,通过MetaboAnalyst进行代谢物富集分析;盲肠微生物组进行群落结构分析,结合TCGA数据库的人类HCC转录组数据进行跨物种关联分析。
结果解读:转录组分析显示,WD对肝脏基因表达的调控依赖FXR功能,WT小鼠中WD诱导2250个DEGs,而FXR KO小鼠仅486个;年龄相关的DEGs在WT小鼠中为1908个,FXR KO小鼠中为470个,表明FXR参与调控年龄相关的基因表达变化。

代谢组分析显示,尿液代谢物可特异性区分不同饮食干预,血清代谢物可清晰区分不同年龄阶段,肝脏代谢物在WT小鼠中受饮食影响更显著。
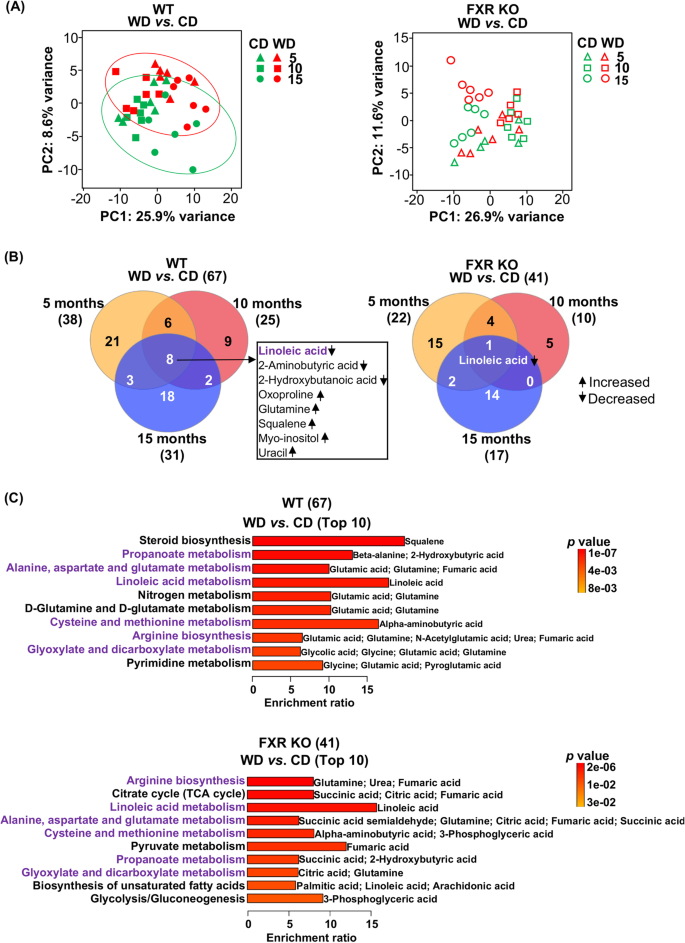
微生物组分析显示,WT小鼠中饮食对微生物群落的影响随年龄增长逐渐减弱,而FXR KO小鼠中饮食可显著区分微生物群落结构。
产品关联:实验所用关键产品:TRIzol试剂(Invitrogen,货号未提及)、Avance 600 MHz NMR光谱仪(Bruker)、RNA测序服务(Novogene Co., LTD)。
3.3 多组学整合与临床标志物筛选
实验目的:整合多组学数据,筛选与饮食、衰老、FXR调控相关且与人类HCC预后关联的分子标志物。
方法细节:通过Venn图分析筛选受饮食、年龄、FXR KO共同调控的转录本和代谢物;利用Spearman相关性分析构建肝脏转录本/代谢物与血清/尿液代谢物、肠道微生物的关联网络;结合TCGA数据库分析差异基因在人类HCC中的表达及与患者预后的关系。
结果解读:共筛选出654个受三因素共同调控的转录本,其中76个在人类HCC与健康肝脏中差异表达,18个上调基因(如PLEKHH1、TTC39A等)与HCC患者不良预后正相关(n=371,P<0.05),7个下调基因(如PCK1、TSC22D3等)与不良预后负相关;44个肝脏代谢物受三因素共同调控,部分代谢物与HCC预后相关基因及肠道微生物存在显著相关性;肠道微生物中拟杆菌属(Bacteroides)在FXR KO小鼠中显著富集,与不良预后基因正相关(n=6,P<0.05)。
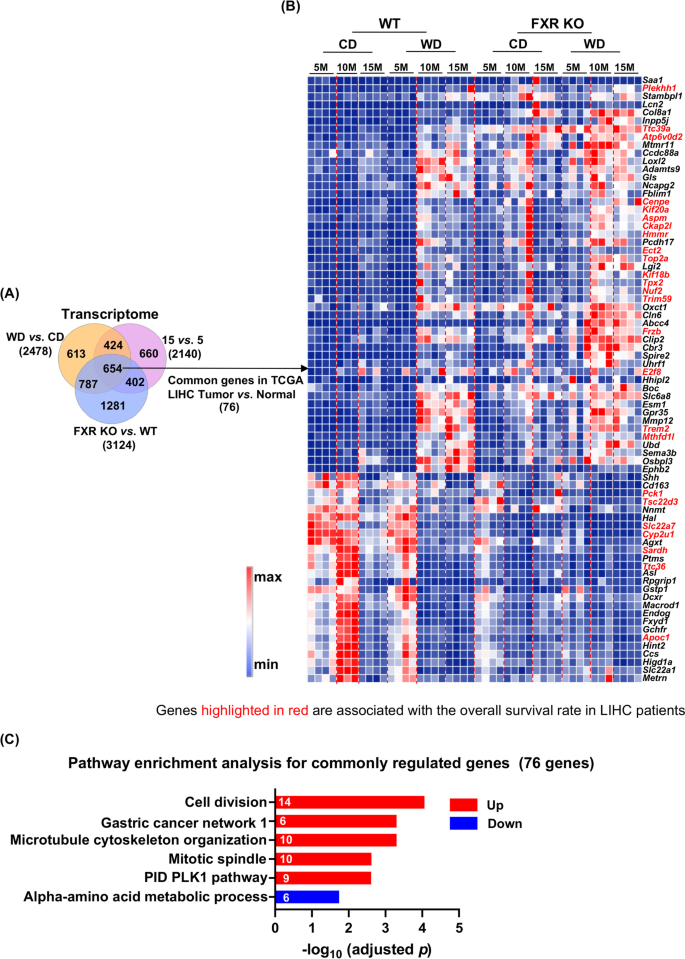
产品关联:文献未提及具体实验产品,领域常规使用的生物信息学工具包括Metascape、OncoLnc、R语言分析包等。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究涉及的Biomarker涵盖三类:转录组标志物(76个与人类HCC相关的差异基因)、代谢组标志物(肝脏/血清/尿液中的差异代谢物)、微生物组标志物(拟杆菌属等肠道微生物);筛选与验证逻辑为:首先基于小鼠多组学数据筛选受饮食、年龄、FXR共同调控的分子,再通过人类TCGA数据库验证其与HCC的表达关联,最后通过相关性分析验证其与临床预后的关系,形成“动物模型筛选-人类数据库验证-临床预后关联”的完整链条。
研究过程详述
转录组标志物来源于小鼠肝脏组织,通过RNA测序筛选差异基因,结合TCGA数据库验证显示,18个上调基因在人类HCC组织中高表达,与患者不良预后正相关(n=371,P<0.05),7个下调基因在HCC组织中低表达,与不良预后负相关;代谢组标志物中,尿液代谢物(如三甲胺TMA、氧化三甲胺TMAO)可特异性区分饮食干预,WD饲喂小鼠尿液中TMA、TMAO水平显著降低,血清代谢物(如丙氨酸、异亮氨酸)可区分年龄阶段,随年龄增长水平显著升高,肝脏代谢物(如尿嘧啶、氧代脯氨酸)在WD饲喂小鼠中水平升高,与NASH进展相关;微生物组标志物中,拟杆菌属在FXR KO小鼠中显著富集,与不良预后基因呈正相关(n=6,P<0.05)。
核心成果提炼
该Biomarker的功能关联与创新性体现在:18个上调转录组标志物参与细胞分裂、有丝分裂纺锤体形成等肿瘤发生通路,可作为HCC的预后标志物,风险比HR未明确(P<0.05);尿液代谢物TMA、TMAO可作为饮食诱导肝病的早期诊断标志物,具有非侵入性检测优势;拟杆菌属可作为FXR功能缺失及肝病进展的微生物标志物,为肠道微生物干预提供靶点。本研究首次系统整合多维度Biomarker,构建了“转录组-代谢组-微生物组”联合诊断体系,为代谢性肝病的早期诊断和预后评估提供了多维度的候选分子,相关数据均经过统计学验证,具有较高的临床转化潜力。
