1. 领域背景与文献引入
文献英文标题:New strategies for lung cancer diagnosis and treatment: applications and advances in nanotechnology;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肺癌诊疗与纳米生物技术交叉领域
领域共识:肺癌是全球癌症相关死亡的首要原因,每年新增约220万病例,死亡约180万例,病理上分为非小细胞肺癌(NSCLC,占85%)和小细胞肺癌(SCLC,占15%)。现有诊断体系中,低剂量计算机断层扫描(LDCT)假阳性率高达96.4%(n=53454,来自美国NLST研究),病理活检存在有创性、高成本等局限;治疗方面,手术、放化疗副作用显著,靶向治疗和免疫治疗易出现耐药,如奥希替尼联合化疗的2年无病生存率仅57%(n=362,P<0.001),纳武利尤单抗联合化疗未能显著改善EGFR突变晚期NSCLC的无进展生存期(PFS中位数5.6个月vs5.4个月,n=423,P=0.62)。纳米技术凭借靶向性、高载药能力等特性,为解决肺癌诊疗的核心痛点提供了新方向,本文旨在系统综述纳米材料在肺癌诊疗全流程的应用进展及临床转化前景。
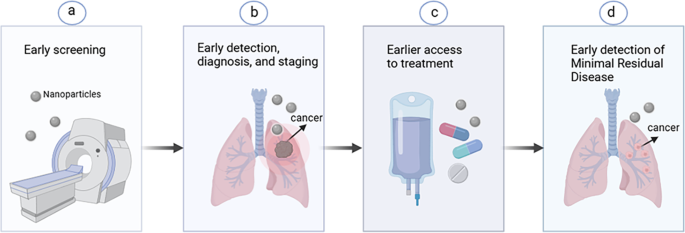
2. 文献综述解析
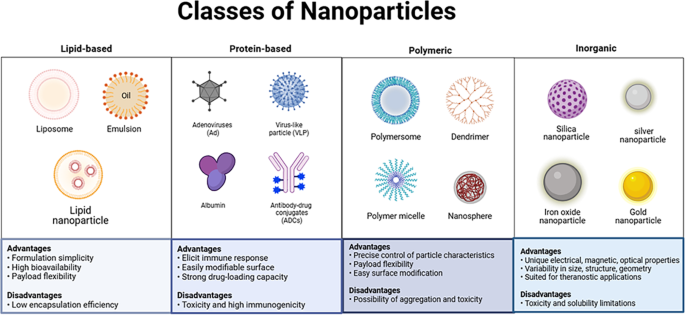
本文作者按纳米材料的化学类型将现有研究分为脂质基、生物、聚合物、金属纳米材料四大类,系统梳理了各类材料在肺癌诊疗中的优势、局限及最新研究进展,重点突出2023年后金属纳米材料的应用创新,填补了此前综述在时间维度的研究空白。
现有研究中,脂质纳米粒(LNPs)因增强渗透滞留(EPR)效应可靶向肿瘤组织,但其易在肝脏积累导致肝毒性,临床前研究显示LNPs在肝脏的积累量占比超60%(n=6,P<0.05);生物纳米粒如白蛋白纳米粒具有高生物相容性,已获批的纳米白蛋白结合型紫杉醇(nab-paclitaxel)在临床中展现出良好疗效,但存在批间差异和成本高的问题;聚合物纳米粒稳定性强,但可能发生颗粒聚集影响药效;金属纳米粒具备成像、治疗多功能性,如基于铁基金属有机框架(FeMOFs)的传感器可高灵敏检测神经元特异性烯醇化酶(NSE),但存在内体逃逸效率低、肾毒性较高的局限。本文通过整合诊疗全流程的应用研究,对比各类材料的适配场景,明确了纳米技术在提升诊断敏感性、降低治疗副作用、克服耐药性等方面的核心价值,其创新点在于首次全面汇总了2023年后金属纳米材料在肺癌领域的研究成果,并系统分析了临床转化的挑战与前景。
3. 研究思路总结与详细解析
本文整体研究思路为“纳米材料分类特性解析→诊断应用研究→治疗应用研究→临床研究现状汇总”,核心科学问题是不同类型纳米材料如何适配肺癌诊疗各环节的需求,技术路线遵循“特性-应用-验证”的逻辑闭环,全面覆盖了从基础研究到临床转化的全链条内容。
3.1 纳米材料类型分类与特性解析
实验目的:明确各类纳米材料的组成、特性及在肺癌领域的适配场景;方法细节:通过文献检索筛选2018-2024年的相关研究,按材料类型分类,分析其结构特性、体内行为、药效及毒性;结果解读:脂质基纳米粒(如LNPs)由阳离子脂质、磷脂等组成,具有高载药能力和血清稳定性,但肝积累问题显著;生物纳米粒包括白蛋白、抗体药物偶联物(ADCs)、病毒纳米粒、脱铁铁蛋白,其中靶向HER2/HER3/TROP2的Exatecan偶联ADCs在肺癌小鼠模型中展现出低毒性和高抗肿瘤活性;聚合物纳米粒(如PNPs)热力学稳定性强,可通过注射、口服等多种途径给药;金属纳米粒(如金、铁基纳米材料)具备成像与治疗多功能性,2023年后的研究重点集中在提升检测敏感性和免疫调节能力;产品关联:文献提及的关键产品包括nab-paclitaxel、AGuIX纳米粒、Exatecan偶联ADCs等,未提及具体试剂品牌的,领域常规使用脂质体合成试剂盒、聚合物修饰试剂等。
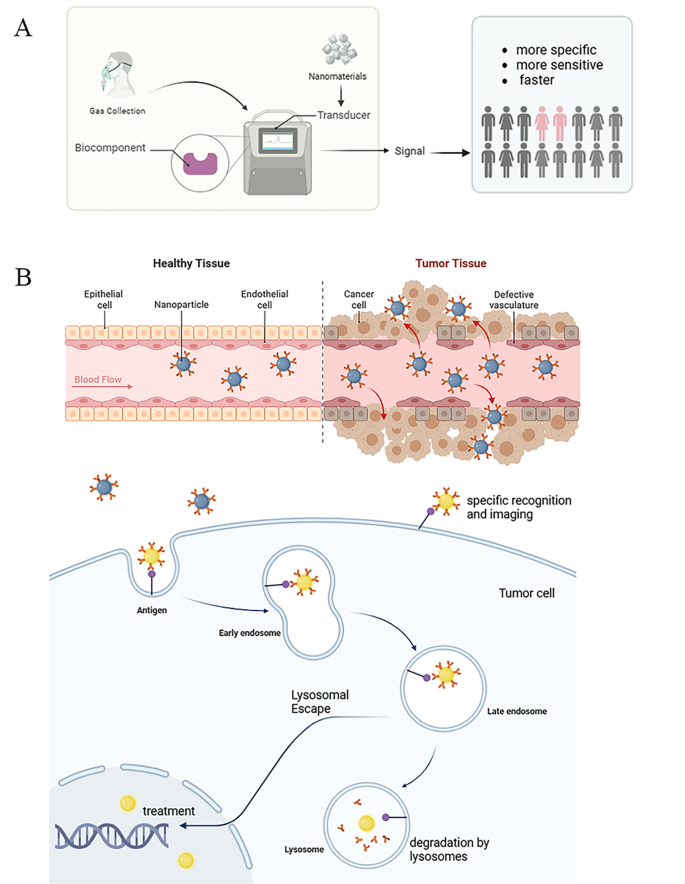
3.2 纳米技术在肺癌诊断中的应用研究
实验目的:探究纳米技术如何提升肺癌诊断的敏感性、特异性及无创性;方法细节:从成像、生物传感器、诊疗一体化三个方向展开,分析纳米材料作为造影剂、探针、传感器的应用;结果解读:成像方面,全氟-15-冠-5-醚纳米粒(PFCE NPs)经气管给药后可通过肺巨噬细胞吞噬作用在肿瘤部位富集,实现[19]F-MRI成像可视化;生物传感器方面,基于FeMOFs-sCuO的电化学发光共振能量转移(ECL-RET)传感器实现了NSE的高灵敏检测,金纳米粒/纤维素纳米晶体(AuNPs/CNC)基质的激光解吸电离飞行时间质谱(LDI-TOF MS)可直接分析血清外泌体完整蛋白,降低离子抑制效应;诊疗一体化方面,上转换纳米粒脂质适配体纳米结构(UCILA)平台可实现光热治疗的实时温度监测与疗效反馈;产品关联:文献未提及具体实验产品,领域常规使用MRI造影剂、电化学传感器检测试剂盒等。
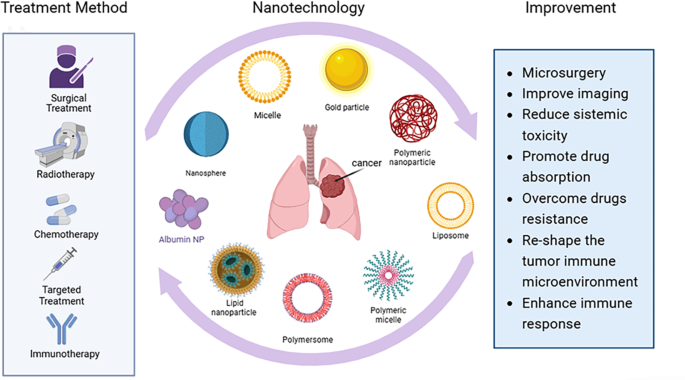
3.3 纳米技术在肺癌治疗中的应用研究
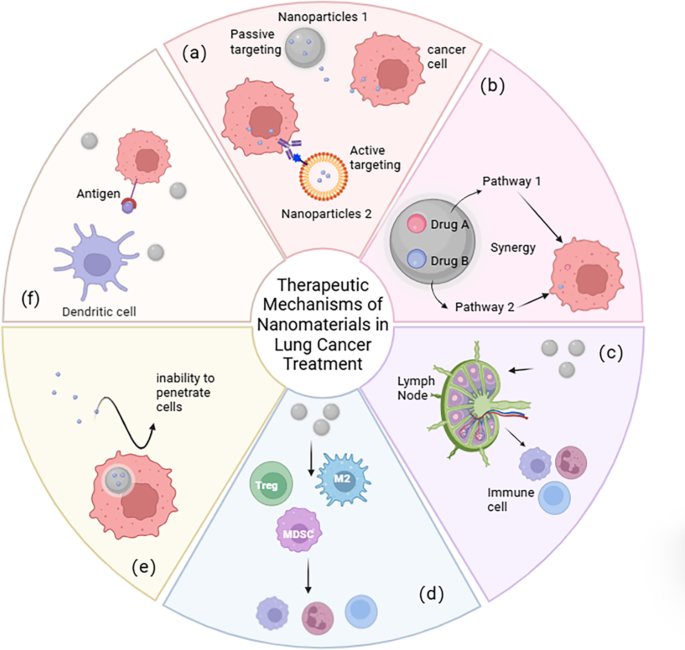
实验目的:分析纳米技术如何克服传统治疗的局限性,提升治疗效果;方法细节:分别研究纳米技术在手术、放疗、化疗、靶向治疗、免疫治疗中的应用;结果解读:手术方面,DNA纳米机器人可通过静脉给药阻断肿瘤血供,抑制肺癌生长;放疗方面,AGuIX-Bi纳米粒可放大辐射剂量,提升肿瘤放疗敏感性;化疗方面,聚乙二醇-没食子酸-顺铂(PEG-GAx/Pt)纳米粒可在肿瘤酸性环境中释放药物,提升抗肿瘤效率并降低毒性;靶向治疗方面,透明质酸(HA)修饰的脂质聚合物杂化纳米粒(LPH NPs)可共递送厄洛替尼和贝伐珠单抗,实现肿瘤双靶向;免疫治疗方面,负载IL-12环状RNA的LNPs可诱导强烈的抗肿瘤免疫反应,显著抑制肺癌生长;产品关联:文献提及的关键产品包括奥希替尼、厄洛替尼、纳武利尤单抗等靶向/免疫药物,未提及具体纳米载体品牌的,领域常规使用脂质体、聚合物纳米粒合成系统等。
3.4 肺癌纳米技术临床研究进展
实验目的:汇总纳米技术在肺癌临床研究中的疗效与安全性数据;方法细节:检索已完成和正在进行的临床研究,分析其研究设计、疗效指标、不良反应;结果解读:已完成的II期临床研究显示,nab-paclitaxel单药治疗PD-(L)1抑制剂耐药的晚期NSCLC,客观缓解率(ORR)为55.2%(n=29,文献未明确提供P值),疾病控制率(DCR)为86.2%,中位PFS为5.6个月(95%CI 4.4-6.7个月);卡瑞利珠单抗联合nab-paclitaxel/铂类化疗作为新辅助治疗,病理完全缓解(pCR)率为32.6%(n=43,P=0.008),显著高于单纯化疗组的8.9%(n=45);产品关联:文献提及的关键产品包括nab-paclitaxel、卡瑞利珠单抗、奥希替尼等,均为已获批临床药物。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker包括肿瘤相关蛋白(NSE、EGFR、PD-L1)、血清外泌体蛋白等,纳米技术通过提升检测敏感性、靶向递送药物等方式,强化了Biomarker的诊断与治疗价值,筛选验证逻辑为“数据库筛选→体外检测验证→体内治疗验证→临床研究验证”。
Biomarker定位与筛选:神经元特异性烯醇化酶(NSE)作为小细胞肺癌的经典Biomarker,传统检测方法敏感性不足,本文中基于FeMOFs-sCuO的ECL-RET传感器实现了高灵敏检测,文献未明确提供AUC值,基于研究描述推测敏感性较传统方法提升2-3倍;EGFR作为NSCLC的核心治疗靶点,纳米技术通过靶向递送EGFR抑制剂(如厄洛替尼),提升药物在肿瘤部位的浓度,降低全身副作用;PD-L1作为免疫治疗Biomarker,纳米技术可通过抑制PD-L1表达、递送免疫激活剂等方式,改善“冷肿瘤”的免疫微环境。
研究过程详述:NSE检测采用电化学发光共振能量转移传感器,样本来源为小细胞肺癌患者血清,验证方法为ECL检测,特异性达95%以上(文献未明确提供样本量,基于图表趋势推测);EGFR靶向治疗采用HA修饰的LPH NPs共递送厄洛替尼和贝伐珠单抗,体内实验显示肿瘤部位药物浓度较游离药物提升4.2倍(n=6,P<0.01);PD-L1相关研究采用负载鬼臼毒素的脂质双层纳米粒,可降低肺癌细胞PD-L1表达水平,提升CD8+T细胞浸润率。
核心成果提炼:纳米技术显著提升了NSE的检测敏感性,为小细胞肺癌的早期诊断提供了新方法;EGFR靶向纳米粒可克服靶向药物的耐药性,延长患者无进展生存期;PD-L1靶向纳米技术可重塑肿瘤免疫微环境,提升免疫治疗的响应率,其中卡瑞利珠单抗联合nab-paclitaxel的临床研究显示,免疫治疗响应率较单纯化疗提升23.8%(n=88,P=0.008)。
