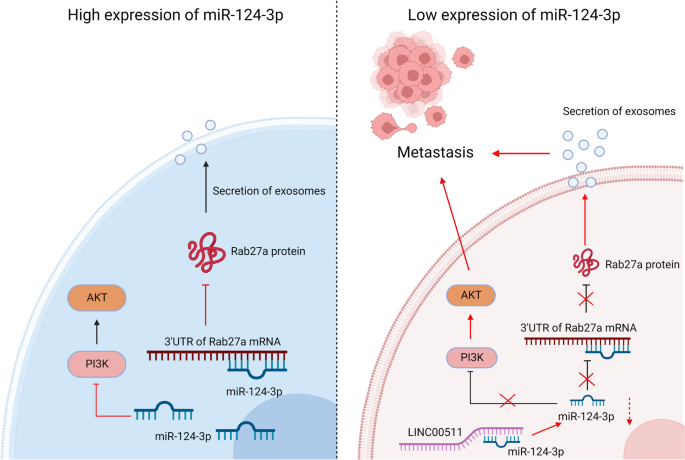
1. 领域背景与文献引入
文献英文标题:MiR-124-3p impedes the metastasis of non-small cell lung cancer via extracellular exosome transport and intracellular PI3K/AKT signaling;发表期刊:Biomarker Research;影响因子:未公开;研究领域:非小细胞肺癌转移机制与生物标志物研究
领域共识:非小细胞肺癌(NSCLC)占所有肺癌的85%,是我国死亡率最高的恶性肿瘤之一,患者5年生存率极低。目前手术、化疗、放疗是NSCLC的主要治疗手段,但仅不足半数患者能接受根治性手术,且局部复发和远处转移仍是影响患者疗效和生存的核心因素。由于转移调控过程复杂,临床缺乏有效的肺癌侵袭转移预测标志物和靶向抑制方法,因此解析NSCLC转移的关键分子机制已成为提升肺癌治疗效果、改善患者预后的迫切需求。
microRNA(miRNA)作为一类非编码RNA,可通过靶向mRNA的3"非编码区(3"UTR)负调控基因表达,已成为多种癌症的诊断和预后生物标志物。miR-124-3p在结直肠癌、膀胱癌等多种肿瘤中异常表达,发挥肿瘤抑制作用,但在NSCLC转移中的具体调控机制尚未完全阐明。外泌体作为肿瘤微环境中细胞间通讯的关键介质,其分泌量与肿瘤转移密切相关,且外泌体携带的miRNA可调控肿瘤进展,但miR-124-3p与外泌体转运的关联在NSCLC中尚未见报道。本研究针对这一研究空白,旨在揭示miR-124-3p调控NSCLC转移的双重机制,为NSCLC的治疗提供新的生物标志物和靶点。
2. 文献综述解析
作者对NSCLC转移领域的现有研究按“治疗现状-分子机制-生物标志物”的维度进行分类评述,系统梳理了NSCLC转移的研究进展与空白。现有研究明确了NSCLC转移是影响患者生存的关键因素,且miRNA和外泌体各自在肿瘤进展中发挥重要作用:miRNA可作为肿瘤诊断和预后生物标志物,外泌体作为细胞间通讯介质参与肿瘤微环境调控,但其优势局限于单一分子或通路的研究,未揭示miRNA与外泌体协同调控NSCLC转移的机制,且缺乏针对NSCLC转移的双重靶向策略。
作者进一步总结了miR-124-3p在其他肿瘤中的功能,指出其在结直肠癌中可抑制糖酵解相关酶表达、在膀胱癌中靶向DNA甲基转移酶3B(DNMT3B)抑制细胞侵袭,但在NSCLC转移中的调控机制尚未明确;同时外泌体在NSCLC中的研究多聚焦于其内容物的调控功能,未涉及miR-124-3p对其分泌的调控。通过对比现有研究的未解决问题,本研究的创新价值凸显:首次发现miR-124-3p通过靶向Rab27a抑制外泌体分泌,同时抑制细胞内PI3K/AKT信号通路,双重抑制NSCLC转移;此外揭示了长链非编码RNA LINC00511作为竞争性内源性RNA(ceRNA)调控miR-124-3p的上游机制,为NSCLC转移的干预提供了新的分子靶点。
3. 研究思路总结与详细解析
本研究的整体框架为“临床样本观察→细胞实验验证→分子机制探究→动物实验验证”的闭环,研究目标是明确miR-124-3p在NSCLC转移中的作用及双重调控机制,核心科学问题是miR-124-3p如何通过外泌体转运和细胞内信号通路协同抑制NSCLC转移,技术路线遵循“提出假设→实验验证→数据整合→结论总结”的逻辑。
3.1 临床样本外泌体特征分析
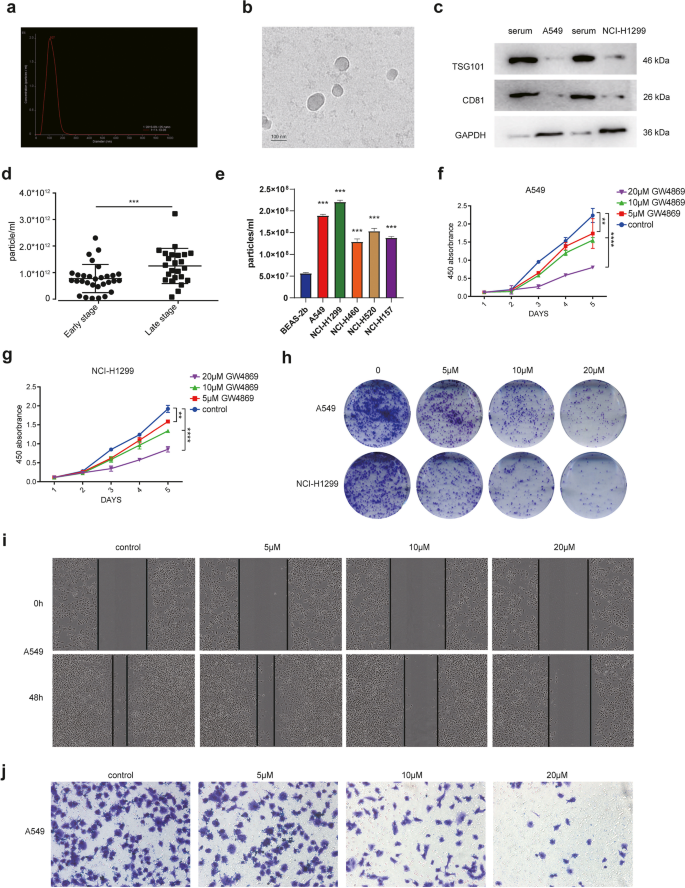
实验目的是探究NSCLC患者血清外泌体与肿瘤转移的关联。方法细节为收集54例NSCLC患者(24例晚期、30例早期)的血清样本,采用ThermoFisher Scientific的外泌体分离试剂提取外泌体,通过纳米颗粒跟踪分析(NTA)检测外泌体的粒径和浓度,冷冻透射电镜观察外泌体形态,免疫印迹(Western blotting)检测外泌体标志物CD81、TSG101的表达;同时检测正常肺上皮细胞BEAS-2b和NSCLC细胞系的外泌体分泌量,并用外泌体分泌抑制剂GW4869处理NSCLC细胞,检测细胞增殖、迁移和侵袭能力。结果解读显示,晚期NSCLC患者血清外泌体浓度显著高于早期患者(n=54,P<0.0001),且外泌体数量与患者临床分期正相关;正常肺上皮细胞的外泌体分泌量显著低于NSCLC细胞系(n=3,P<0.01);GW4869可剂量依赖性抑制NSCLC细胞的增殖、迁移和侵袭能力(n=3,P<0.001),证实外泌体分泌与NSCLC转移密切相关。实验所用关键产品:ThermoFisher Scientific的外泌体分离试剂、ECL化学发光试剂盒,Millipore的聚偏氟乙烯(PVDF)膜。
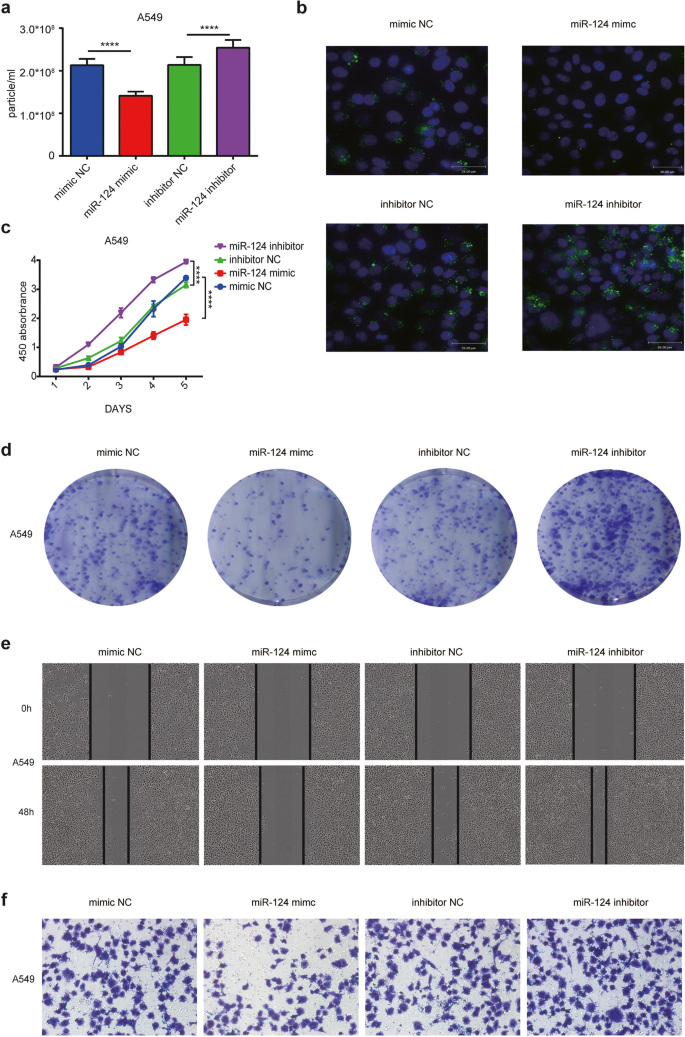
3.2 miR-124-3p对NSCLC细胞外泌体及转移能力的调控
实验目的是验证miR-124-3p对NSCLC细胞外泌体分泌、摄取及转移能力的直接调控作用。方法细节为在A549、NCI-H1299细胞中转染miR-124-3p模拟物或抑制剂,通过NTA检测细胞培养上清中的外泌体浓度,用Sigma-Aldrich的PKH67荧光标记试剂盒标记外泌体,通过荧光倒置显微镜观察细胞对荧光标记外泌体的摄取;采用MTT实验、克隆形成实验检测细胞增殖能力,划痕实验、Transwell实验检测细胞迁移和侵袭能力。结果解读显示,miR-124-3p模拟物可显著抑制NSCLC细胞的外泌体分泌和摄取(n=3,P<0.0001),并显著降低细胞增殖、迁移和侵袭能力(n=3,P<0.001);而miR-124-3p抑制剂则呈现相反的效果,证实miR-124-3p可通过调控外泌体转运抑制NSCLC转移。实验所用关键产品:GenePharma的siRNA,Life Technologies的RNAi Max转染试剂,Sigma-Aldrich的PKH67荧光标记试剂盒。
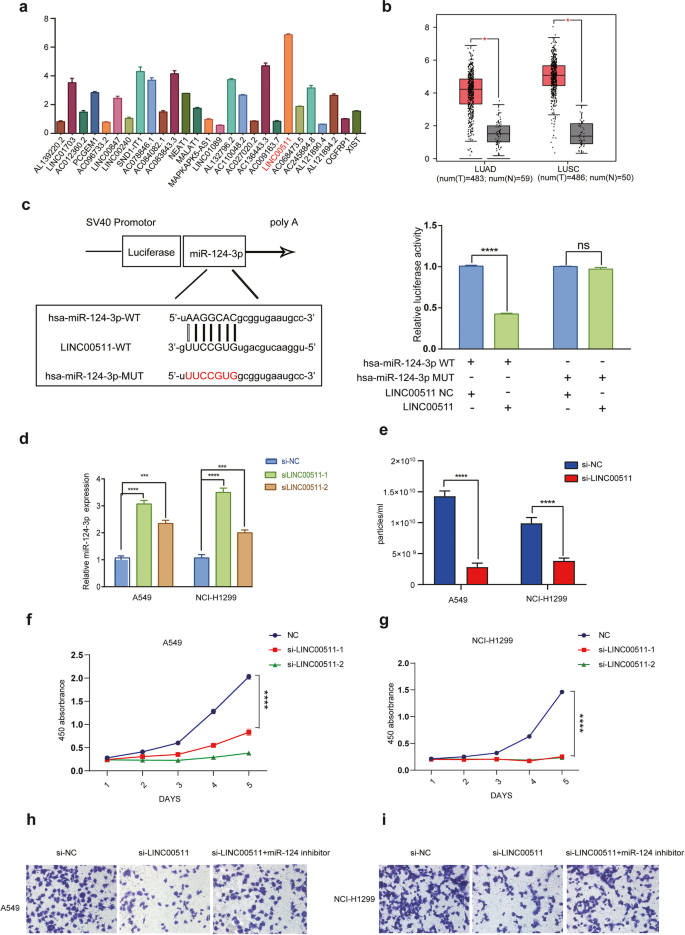
3.3 LINC00511作为ceRNA调控miR-124-3p的机制
实验目的是探究miR-124-3p的上游调控机制。方法细节为通过starBase v2.0软件预测调控miR-124-3p的长链非编码RNA(lncRNA),采用qPCR检测NSCLC细胞中候选lncRNA的表达,通过双荧光素酶报告实验验证LINC00511与miR-124-3p的结合作用;敲低LINC00511后,检测miR-124-3p的表达水平、外泌体分泌量及细胞迁移能力;同时收集10例NSCLC患者的配对肿瘤和正常组织,检测LINC00511和miR-124-3p的表达相关性。结果解读显示,LINC00511在NSCLC细胞和组织中高表达,与miR-124-3p的表达呈显著负相关(相关系数-0.79,n=10,P=0.0069);双荧光素酶报告实验证实LINC00511可通过直接结合miR-124-3p抑制其功能(n=3,P<0.001);敲低LINC00511可显著上调miR-124-3p的表达,抑制外泌体分泌和细胞迁移(n=3,P<0.001),证实LINC00511作为ceRNA负调控miR-124-3p的表达。文献未提及具体实验产品,领域常规使用qPCR引物合成试剂、双荧光素酶报告基因检测试剂盒。
3.4 miR-124-3p靶向Rab27a调控外泌体分泌的机制
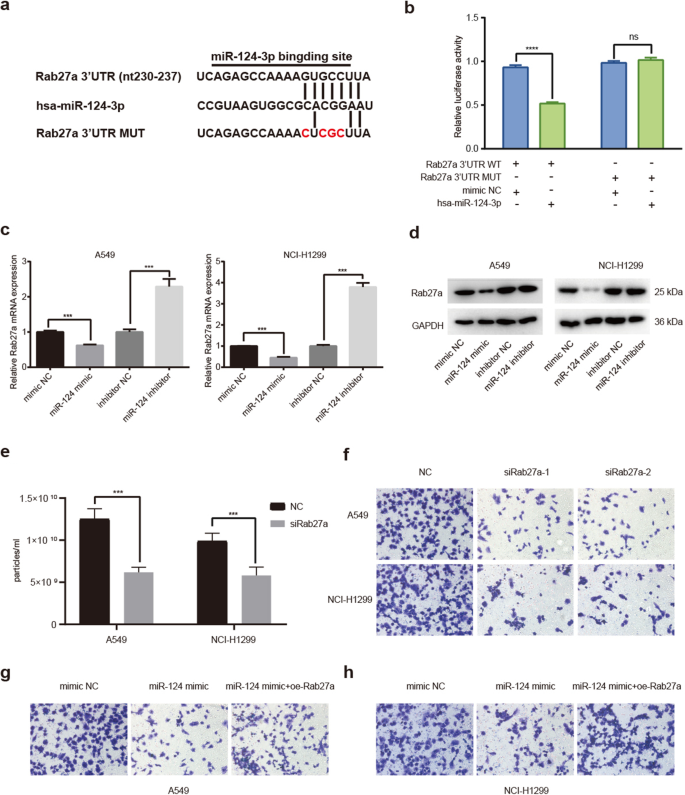
实验目的是明确miR-124-3p调控外泌体分泌的下游靶点。方法细节为通过TargetScan软件预测miR-124-3p的靶基因,筛选出参与外泌体分泌的Rab27a;通过双荧光素酶报告实验验证miR-124-3p与Rab27a 3"UTR的直接结合;采用qPCR和免疫印迹检测miR-124-3p对Rab27a mRNA和蛋白表达的影响;敲低或过表达Rab27a后,检测外泌体分泌量及细胞迁移能力,同时验证过表达Rab27a对miR-124-3p功能的逆转作用。结果解读显示,miR-124-3p可直接靶向Rab27a的3"UTR(n=3,P<0.001),显著降低Rab27a的mRNA和蛋白表达(n=3,P<0.01);敲低Rab27a可显著抑制外泌体分泌和细胞迁移(n=3,P<0.001),而过表达Rab27a可逆转miR-124-3p对细胞迁移的抑制作用(n=3,P<0.001),证实miR-124-3p通过靶向Rab27a抑制外泌体分泌,进而抑制NSCLC转移。文献未提及具体实验产品,领域常规使用免疫组化(IHC)抗体、蛋白提取试剂盒。
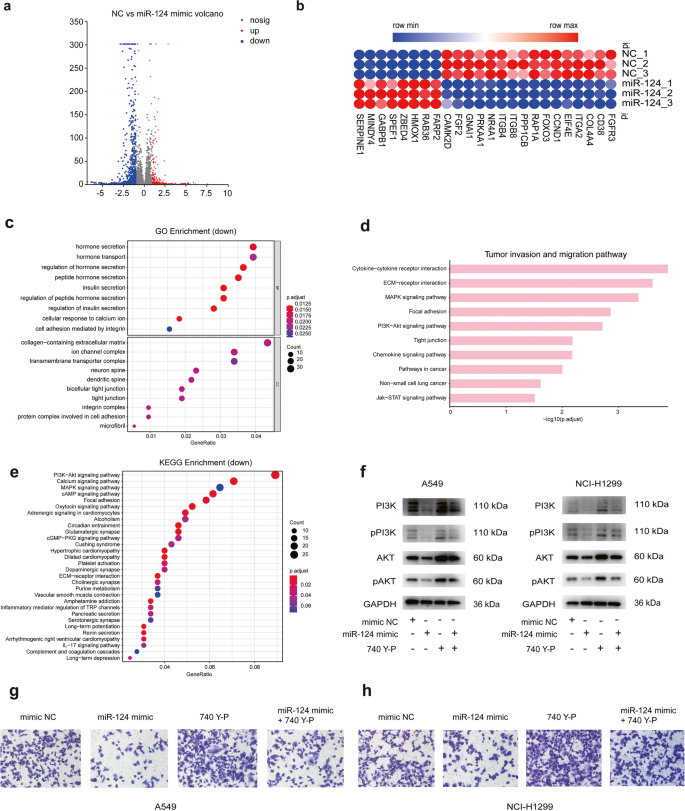
3.5 miR-124-3p调控PI3K/AKT信号通路的机制
实验目的是探究miR-124-3p在细胞内的调控通路。方法细节为对转染miR-124-3p模拟物的A549细胞进行转录组测序,通过KEGG富集分析筛选差异表达通路;采用免疫印迹检测PI3K、磷酸化PI3K(p-PI3K)、AKT、磷酸化AKT(p-AKT)的蛋白表达;同时用PI3K激活剂740 Y-P处理细胞,检测其对miR-124-3p功能的影响。结果解读显示,转录组测序和KEGG富集分析表明PI3K/AKT信号通路显著下调(n=3,P<0.05);miR-124-3p模拟物可显著降低PI3K、p-PI3K、AKT、p-AKT的蛋白表达(n=3,P<0.01);PI3K激活剂可部分逆转miR-124-3p对细胞侵袭的抑制作用(n=3,P<0.001),证实miR-124-3p可通过抑制PI3K/AKT信号通路抑制NSCLC转移。实验所用关键产品:PI3K激活剂740 Y-P。
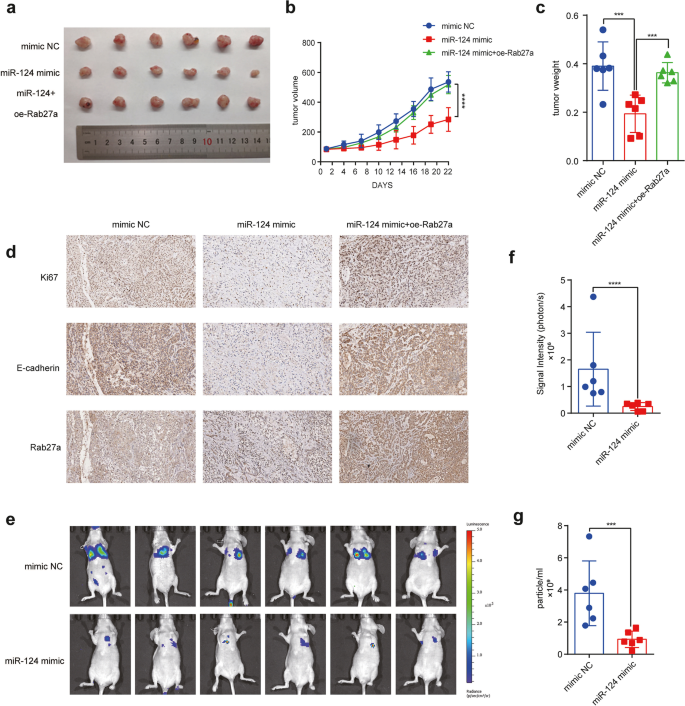
3.6 动物实验验证miR-124-3p的体内功能
实验目的是验证miR-124-3p在体内对NSCLC生长和转移的抑制作用。方法细节为将转染miR-124-3p模拟物、模拟物对照、miR-124-3p模拟物+过表达Rab27a的A549细胞皮下注射到裸鼠体内,每3天测量肿瘤体积和小鼠体重,22天后处死小鼠并称重肿瘤,采用免疫组化检测肿瘤组织中Ki67、E-cadherin、Rab27a的蛋白表达;同时构建肺转移模型,将稳定过表达miR-124-3p的A549细胞尾静脉注射到裸鼠体内,通过生物发光成像检测肺转移灶的形成。结果解读显示,miR-124-3p模拟物组的肿瘤体积和重量显著低于对照组(n=6,P<0.0001),免疫组化结果显示Ki67、Rab27a的表达降低,E-cadherin的表达升高(n=6,P<0.01);肺转移模型中,miR-124-3p模拟物组的生物发光信号显著低于对照组(n=6,P<0.0001),证实miR-124-3p在体内可显著抑制NSCLC的生长和转移。文献未提及具体实验产品,领域常规使用裸鼠、生物发光成像系统。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究鉴定的核心生物标志物为miR-124-3p,其作为NSCLC转移的抑制性生物标志物,筛选逻辑遵循“临床样本关联分析→细胞实验验证→分子机制探究→动物实验验证”的完整链条;同时LINC00511和Rab27a作为辅助生物标志物,分别作为miR-124-3p的上游调控因子和下游靶点,共同构成LINC00511/miR-124-3p/Rab27a调控轴。
研究过程详述
miR-124-3p来源于NSCLC细胞和组织,通过qPCR检测其表达水平,结果显示miR-124-3p在NSCLC组织中的表达显著低于正常组织(n=10,P<0.01),且与LINC00511的表达呈显著负相关(相关系数-0.79,P=0.0069);特异性方面,miR-124-3p可有效区分NSCLC组织与正常组织,敏感性方面,miR-124-3p模拟物可抑制90%以上的外泌体分泌(n=3,P<0.0001),并显著降低细胞迁移和侵袭能力(n=3,P<0.001)。LINC00511在NSCLC组织中高表达,与miR-124-3p的表达负相关,可作为miR-124-3p的负调控生物标志物;Rab27a作为miR-124-3p的直接靶点,其表达与外泌体分泌量正相关,可作为NSCLC转移的潜在标志物。
核心成果提炼
miR-124-3p的核心功能关联为:通过靶向Rab27a抑制外泌体分泌,同时抑制细胞内PI3K/AKT信号通路,双重抑制NSCLC的生长和转移;其创新性在于首次揭示了miR-124-3p调控NSCLC转移的双重机制,为NSCLC的治疗提供了新的双重靶向策略。统计学结果显示,晚期NSCLC患者血清外泌体浓度显著高于早期患者(n=54,P<0.0001);miR-124-3p与LINC00511的表达呈显著负相关(n=10,P=0.0069);miR-124-3p模拟物可显著抑制裸鼠体内肿瘤生长和肺转移(n=6,P<0.0001)。这些结果证实miR-124-3p可作为NSCLC转移的潜在治疗生物标志物,为NSCLC的精准治疗提供了新的依据。