1. 领域背景与文献引入
文献英文标题:Inotuzumab ozogamicin in clinical development for acute lymphoblastic leukemia and non-Hodgkin lymphoma;发表期刊:Biomark Res;影响因子:未公开;研究领域:血液系统恶性肿瘤(急性淋巴细胞白血病、非霍奇金淋巴瘤)的抗体药物偶联物靶向治疗。
B细胞来源的急性淋巴细胞白血病(ALL)和非霍奇金淋巴瘤(NHL)是常见的血液系统恶性肿瘤,其中复发/难治性(R/R)患者的预后极差,传统化疗方案的缓解率低且毒性显著,5年生存率不足30%。领域共识:近年来,免疫治疗成为血液肿瘤治疗的核心突破方向,CD20单克隆抗体、CD19靶向双特异性抗体、嵌合抗原受体T细胞(CAR-T)等疗法相继获批,显著改善了部分患者的生存结局,但仍存在未解决的核心问题,如部分患者对CD19、CD20等靶点产生耐药性,CAR-T治疗的细胞因子释放综合征等毒性风险较高,且部分罕见亚型缺乏有效治疗手段。CD22作为B细胞表面特异性表达的抑制性受体,在不同分化阶段的B细胞恶性肿瘤中均呈高表达状态,是极具潜力的新型治疗靶点,而Inotuzumab ozogamicin(INO)是首个针对CD22的抗体药物偶联物(ADC),本文系统综述了INO在ALL和NHL中的临床前研究、各期临床试验结果及毒性管理策略,为该靶点药物的临床应用提供全面的学术参考。
2. 文献综述解析
本文以CD22靶点的生物学特性为基础,按疾病类型(ALL、NHL)和研究阶段(临床前、临床I/II/III期)对INO的开发进展进行分类综述,重点对比了INO与传统治疗、其他免疫疗法的疗效差异,明确了其临床应用的优势与局限性。
现有研究已证实CD22在B细胞恶性肿瘤中的高表达特性,不同亚型ALL中CD22表达率为83%-100%,其中成熟B细胞ALL的表达率达100%,NHL中滤泡淋巴瘤、套细胞淋巴瘤等亚型的表达率也超过95%,为靶向治疗提供了可靠的靶点基础。临床前研究显示,INO通过人源化抗CD22抗体与细胞毒素加利车霉素偶联,经内吞作用进入细胞后释放毒素,诱导DNA双链断裂导致细胞死亡,其对CD22阳性细胞的细胞毒性是游离加利车霉素的1.5-39倍,且在小鼠异种移植模型中呈剂量依赖性抑制肿瘤生长。已完成的临床研究中,III期INO-VATE试验证实单药INO治疗R/R B细胞前体ALL的完全缓解(CR)率显著高于传统化疗(80.7% vs 29.4%,P<0.001),中位CR持续时间延长至4.6个月;但在NHL中的试验结果相对有限,单药或联合治疗在难治性NHL中的客观缓解率(ORR)仅为20%,且治疗相关肝静脉闭塞病(VOD)的发生率较高,尤其是在造血干细胞移植(HSCT)预处理阶段,限制了其广泛应用。
与现有研究相比,本文首次系统整合了INO在ALL和NHL中的所有临床开发数据,包括联合化疗方案的探索、毒性管理的优化策略,填补了该领域缺乏全面综述的空白,为临床医生制定治疗方案提供了循证依据,同时明确了未来研究方向,如优化给药方案降低VOD风险、探索在初诊患者中的应用等。
3. 研究思路总结与详细解析
本文的研究目标是全面总结INO在B细胞恶性肿瘤中的临床开发进展,核心科学问题是明确INO在不同疾病中的疗效、安全性及优化策略,技术路线遵循“靶点合理性验证→药物机制与临床前活性→各期临床试验结果→毒性管理→未来方向”的逻辑闭环,通过文献回顾与数据整合完成综述分析。
3.1 CD22靶点生物学特性验证
实验目的是明确CD22作为B细胞恶性肿瘤治疗靶点的临床合理性,方法是通过整合已发表的流式细胞术研究数据,分析CD22在B细胞发育过程中的表达模式,以及在不同亚型ALL和NHL中的表达率,结果显示CD22仅在前B细胞、未成熟B细胞和成熟B细胞表面表达,分化为浆细胞后丢失,在Pro-B ALL中的表达率为83%,普通B细胞ALL为96.4%,成熟B细胞ALL为100%,NHL中慢性淋巴细胞白血病、滤泡淋巴瘤的表达率分别为95%、98%,证实其在绝大多数B细胞恶性肿瘤中高表达,是特异性靶向治疗的理想靶点。
文献未提及具体实验产品,领域常规使用流式细胞术检测细胞表面抗原表达。
3.2 INO的结构与临床前活性研究
实验目的是验证INO的抗肿瘤活性与作用机制,方法是通过体外细胞毒性试验,对比INO与游离加利车霉素对CD22阳性B淋巴瘤细胞系的杀伤作用;建立CD22阳性B细胞淋巴瘤和ALL的小鼠异种移植模型,评估不同剂量INO的肿瘤生长抑制效果,结果显示INO对CD22阳性细胞的细胞毒性是游离加利车霉素的1.5-39倍,在小鼠模型中以剂量依赖性方式抑制肿瘤生长,且能预防ALL细胞的移植和播散性疾病的发生,在儿科ALL细胞的研究中还发现,其诱导凋亡的效果不依赖于CD22的表达水平和受体饱和,进一步扩大了潜在适用人群。文献未提及具体实验产品,领域常规使用细胞增殖/毒性检测试剂盒、免疫缺陷小鼠移植模型等。
3.3 复发/难治性ALL中的临床试验研究
实验目的是评估INO在R/R ALL中的疗效、安全性及最优给药方案,方法是分阶段开展临床试验:I期剂量探索试验设置1.2mg/m²、1.6mg/m²、1.8mg/m²三个剂量组,确定1.8mg/m²为II期推荐剂量;II期扩展试验评估该剂量的疗效,CR/CRi率达69%,微小残留病(MRD)阴性率为75%;III期INO-VATE随机对照试验对比INO与传统化疗,结果显示INO组的CR率为80.7%(n=164,P<0.001),显著高于化疗组的29.4%,中位CR持续时间为4.6个月,长于化疗组的3.1个月(P=0.03);联合mini-Hyper-CVD化疗的II期试验中,ORR达78%(CR59%),1年总生存率(OS)为46%,首次挽救治疗患者的中位OS接近17个月。主要不良反应为VOD,23%接受HSCT的患者出现该毒性,提示需要优化治疗方案以降低风险。文献未提及具体实验产品,领域常规使用临床疗效评价标准(如CR、CRi、MRD)、血液学及肝功能检测等。
3.4 复发/难治性NHL中的临床试验研究
实验目的是评估INO在R/R NHL中的疗效与安全性,方法是开展I期单药及联合利妥昔单抗的试验,确定单药最大耐受剂量(MTD)为1.8mg/m²,联合利妥昔单抗的MTD相同;I/II期联合试验显示,复发滤泡淋巴瘤的ORR达87%,2年无进展生存率(PFS)为68%,弥漫大B细胞淋巴瘤的ORR为74%,中位PFS为17.1个月,但难治性B细胞NHL的ORR仅为20%;后续联合R-CVP、R-GDP等化疗方案的试验中,ORR分别为84%、53%,主要毒性为3级以上血小板减少(75%)、中性粒细胞减少(62%)及VOD。文献未提及具体实验产品,领域常规使用淋巴瘤疗效评价标准、不良事件通用术语标准(CTCAE)等。
3.5 INO相关毒性管理策略研究
实验目的是探索降低INO相关VOD风险的有效方法,方法是通过回顾性分析临床试验数据,评估不同给药方案、移植间隔时间对VOD发生率的影响,结果显示将INO的治疗周期限制在2个周期,或采用拆分剂量的给药方式,可降低VOD的发生风险;在INO治疗后加入blinatumomab作为巩固治疗,延长HSCT的间隔时间,也能减少VOD的发生率;同时,避免使用双烷化剂预处理方案,可进一步降低移植后VOD的风险。文献未提及具体实验产品,领域常规使用肝功能监测、体重监测等手段评估毒性。
4. Biomarker研究及发现成果
本文聚焦CD22作为INO治疗的伴随诊断Biomarker,系统梳理了其筛选、验证过程及临床价值,为INO的精准应用提供了依据。
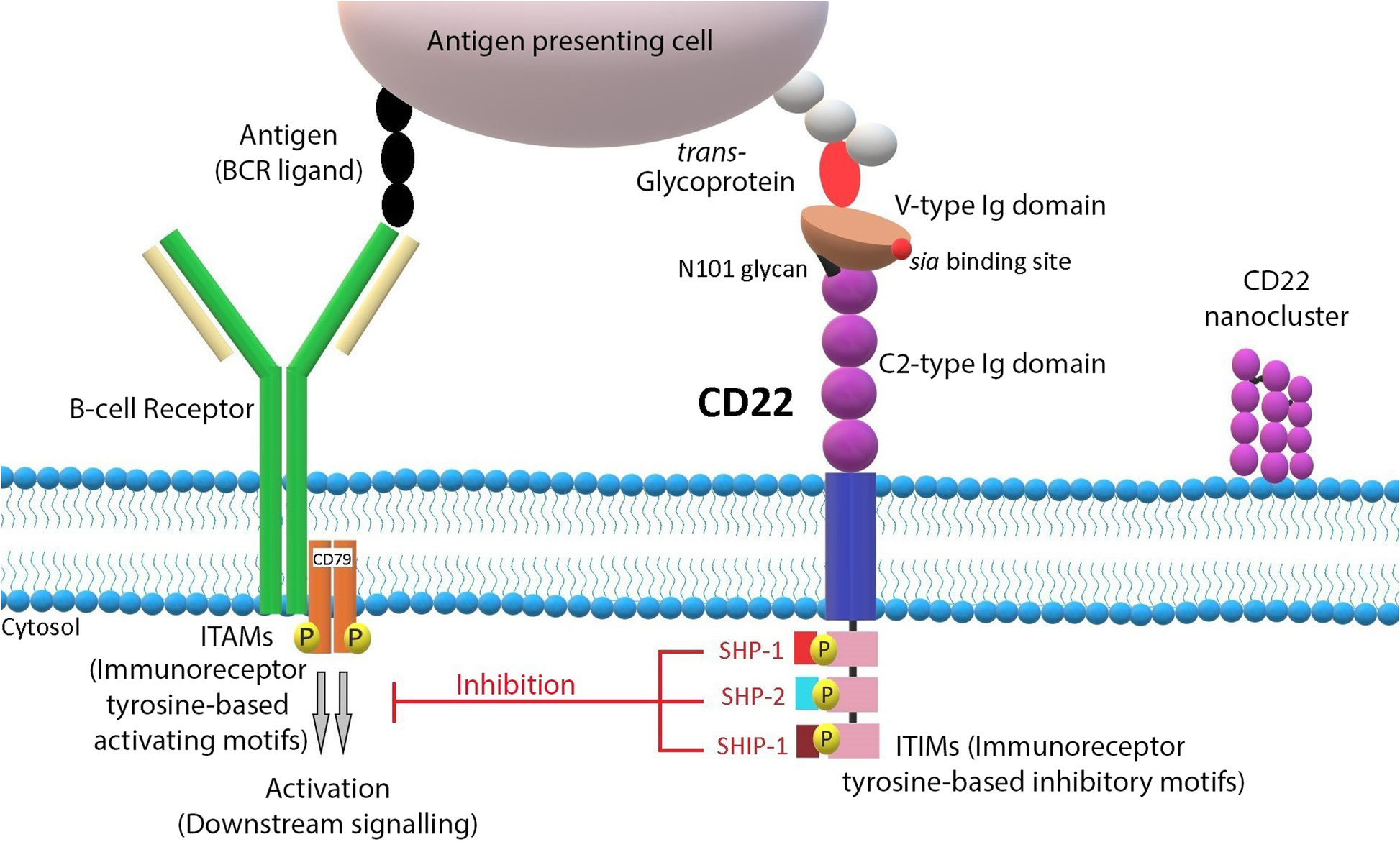
Biomarker定位:CD22属于唾液酸结合免疫球蛋白样凝集素(SIGLEC)家族,是B细胞表面的抑制性受体,作为INO治疗的Biomarker,其筛选逻辑基于B细胞恶性肿瘤中CD22的高表达特性,验证逻辑通过临床前细胞系实验、动物模型及临床试验的相关性分析完成,即CD22阳性细胞对INO的敏感性显著高于阴性细胞,高表达CD22的患者可能获得更好的疗效。
研究过程详述:CD22的来源为B细胞恶性肿瘤细胞的表面抗原,验证方法主要为流式细胞术,通过特异性抗体标记检测细胞表面CD22的表达率;特异性方面,CD22仅在B细胞谱系表达,分化为浆细胞后丢失,避免了对正常组织的非特异性损伤;敏感性数据显示,不同亚型ALL中CD22的表达率为83%-100%,NHL中各亚型的表达率为89%-100%,其中成熟B细胞ALL、毛细胞白血病等亚型的表达率达100%。目前尚未明确CD22表达水平与疗效相关性的具体统计学数据,如ORR或OS的风险比(HR)等,需进一步研究明确。
核心成果提炼:CD22是首个被证实的INO治疗伴随诊断Biomarker,其高表达特性为INO的靶向治疗提供了精准的人群筛选依据,创新性在于明确了CD22在不同B细胞恶性肿瘤中的表达谱,为临床医生选择治疗方案提供了参考;但目前仍缺乏统一的CD22表达检测标准及疗效预测的cut-off值,未来需开展大样本研究完善该Biomarker的临床应用体系。
