1. 领域背景与文献
文献英文标题:Haemostatic changes during CART cell therapy and risk of complications;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:肿瘤免疫治疗(嵌合抗原受体T细胞治疗相关并发症)
领域共识:嵌合抗原受体T细胞(CAR-T)疗法是血液恶性肿瘤治疗领域的重大突破,2017年首个靶向CD19的CAR-T产品获批上市后,该类疗法已成为复发/难治性B细胞淋巴瘤、多发性骨髓瘤、急性B淋巴细胞白血病等疾病的重要治疗选择,显著延长了难治性患者的生存期。但CAR-T治疗的毒性管理是临床应用的核心挑战,目前经典的细胞因子释放综合征(CRS)、免疫效应细胞相关神经毒性综合征(ICANS)的病理机制和管理策略已较为明确,但血栓、出血等止血系统相关并发症的研究仍较为滞后,现有研究对这类并发症的发生率、动态特征认识不足,缺乏可用于术前风险分层的生物标志物,临床尚无统一的止血并发症预防和管理方案,是CAR-T治疗领域亟待解决的临床问题。本研究针对上述研究空白,前瞻性监测CAR-T治疗患者多个时间点的止血功能指标变化,探索其与各类并发症的关联,旨在为CAR-T治疗相关止血并发症的风险分层和早期干预提供依据。
2. 文献综述解析
作者的文献综述按研究主题分为三个维度展开,系统梳理了CAR-T治疗毒性、止血并发症、止血功能检测技术三个领域的研究进展,明确现有研究的局限性并引出本研究的必要性。
第一部分为CAR-T治疗的常规毒性研究,现有研究已明确CRS、ICANS、免疫效应细胞相关血液学毒性的临床表现、病理机制,相关国际共识已建立了标准化的分级和管理体系,为临床常规毒性的防控提供了依据,但现有研究对止血系统相关并发症的关注较少,未将止血功能指标纳入常规风险分层体系。第二部分为CAR-T相关止血并发症的流行病学研究,现有Meta分析显示CAR-T治疗后首个月内静脉血栓栓塞发生率为2.4%每患者月,临床相关出血发生率为1.9%每患者月,证实这类并发症的临床负担,但现有研究多为回顾性研究,缺乏前瞻性队列的多时间点动态监测数据,尚未明确可预测这类并发症的特异性标志物。第三部分为止血功能检测技术的应用研究,现有研究证实凝血酶生成实验(TGA)是可全面评估凝血系统动态功能的检测技术,相比常规静态凝血指标能更准确反映整体凝血状态,可用于多种疾病的出血/血栓风险评估;P选择素是血小板和内皮细胞激活的特异性标志物,其血浆水平升高与血栓风险显著相关,但上述两项技术尚未在CAR-T治疗人群中进行系统的并发症预测效能验证。
本研究的创新价值在于首次针对CD19和BCMA靶向CAR-T治疗人群,开展前瞻性多时间点止血功能动态监测,明确了止血指标与CRS、ICANS、出血等并发症的关联,填补了CAR-T止血并发症风险分层标志物的研究空白,为临床个体化管理提供了新的潜在指标。
3. 研究思路总结与详细解析
本研究的整体研究目标为明确CAR-T治疗过程中止血功能的动态变化特征,筛选可预测CRS、ICANS、出血、血栓并发症的止血相关生物标志物;核心科学问题为止血功能基线异常及治疗过程中的动态变化是否与CAR-T相关炎症及止血并发症存在独立关联;技术路线遵循“前瞻性队列招募→多时间点样本采集→止血功能指标检测→临床结局规范随访→统计分析指标与结局的关联→验证标志物预测效能”的闭环逻辑,研究设计严谨,结果可靠性较高。
3.1 研究队列与样本采集
本环节的核心目标是建立符合临床实际的前瞻性CAR-T治疗患者队列,获取不同治疗阶段的高质量血液样本用于后续检测。研究连续纳入2022年2月至2024年7月在西班牙纳瓦拉大学临床医院和萨拉曼卡大学医院接受CD19或BCMA靶向CAR-T治疗的成年患者,排除需要治疗性抗凝的患者以避免抗凝药物对止血检测结果的干扰,最终共纳入62例患者,其中B细胞淋巴瘤31例、多发性骨髓瘤29例、急性B淋巴细胞白血病2例,队列中位年龄62岁(IQR 53-69岁),中位既往治疗线数为2线(IQR 2-3线),94%的患者输注时ECOG体能评分为0-1,24%的患者有静脉血栓栓塞病史,8%有动脉血栓病史,基线特征与临床常规CAR-T治疗人群相符。研究分别在清淋预处理前(基线)、CAR-T细胞输注前、输注后第3天、第14天、第28天五个时间点采集静脉血样本,血液样本采集至3.2%枸橼酸钠抗凝管中,经两次离心获得乏血小板血浆后置于-80℃保存待检。实验所用关键产品:BD的3.2%枸橼酸钠采血管。
3.2 实验室检测与临床结局评估
本环节的核心目标是准确检测各样本的止血功能相关指标,规范评估患者的临床结局,为后续关联分析提供可靠数据。常规凝血指标包括凝血酶原时间(PT)、活化部分凝血活酶时间(APTT)、纤维蛋白原、D-二聚体、血管性血友病因子(vWF),采用ACL-TOP 350或STA-Compact分析仪按常规流程检测;凝血酶生成实验采用Stago的ST-Genesia全自动凝血分析仪及配套Thromboscreen试剂盒检测,评估滞后时间、达峰时间、凝血酶峰值、内源性凝血酶潜能(ETP)、血栓调节素诱导的ETP抑制率等参数,检测过程遵循ISTH相关指南要求;P选择素采用R&D Systems的人P选择素/CD62P免疫检测试剂盒(ELISA法)检测,C反应蛋白(CRP)采用罗氏的Tina-quant C反应蛋白IV检测试剂盒(乳胶免疫比浊法)检测。临床结局随访至CAR-T输注后30天,CRS和ICANS按ASTCT共识分级,其中≥2级CRS和任意级别的ICANS定义为临床相关;出血事件按ISTH标准分级,包括大出血和临床相关非大出血;血栓事件经影像学检查确认。随访结果显示,94%的患者发生CRS,其中39%为≥2级的临床相关CRS,中位发生时间为输注后3天(IQR 2-6天);39%的患者发生ICANS,46%为≥3级,中位发生时间为输注后6天(IQR 5-7天);13%的患者发生临床相关出血,中位发生时间为输注后24天(IQR 14-28天),其中90%的出血事件发生在输注后14天以后;仅1.6%的患者发生导管相关静脉血栓栓塞,无动脉血栓事件发生,提示CAR-T治疗后早期出血风险显著高于血栓风险。各类并发症的分布和发生时间见下图:
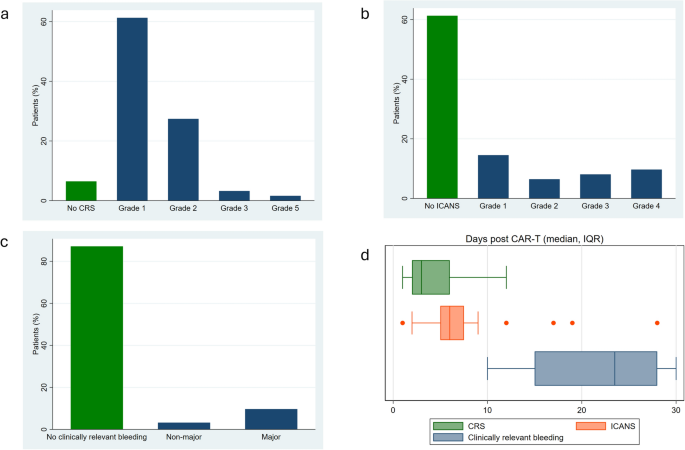
文献未提及ACL-TOP 350、STA-Compact分析仪的配套试剂品牌,领域常规使用对应仪器的原厂配套凝血检测试剂。
3.3 止血功能动态变化分析
本环节的核心目标是明确CAR-T治疗全过程中止血相关指标的动态变化规律,解析治疗对止血系统的影响特征。研究对比了五个时间点的各检测指标水平,采用配对检验分析差异的统计学显著性。结果显示,清淋预处理后凝血酶生成出现一过性抑制,输注前和输注后第3天的凝血酶生成滞后时间、达峰时间较基线显著延长(P<0.05),凝血酶峰值显著降低(P<0.05),上述指标在第14天逐渐恢复正常,但ETP水平在整个随访期间无显著波动,提示整体凝血酶生成潜能未受明显影响。常规凝血指标中,PT和APTT在输注后第3天显著延长,PT延长持续至随访末期,APTT在第14天、28天出现缩短;纤维蛋白原水平在输注后第3天开始显著下降,D-二聚体水平从基线到输注前显著升高,持续至第14天后出现部分恢复,提示治疗过程中存在持续的凝血激活和纤维蛋白溶解。炎症指标CRP在输注后第3天达到峰值(中位2.2mg/dL,P<0.05),之后显著下降至低于基线水平,与CRS的发生时间规律吻合。血小板和内皮功能相关指标中,P选择素在清淋后显著降低(P<0.05),第14天部分恢复;血小板计数从基线到第28天呈进行性下降趋势,所有 post-基线时间点的降低均具有统计学显著性(P<0.05);vWF活性/抗原比值在第14、28天显著降低,提示后期存在血管性血友病因子功能异常。本环节所用关键产品与上述检测环节一致。
3.4 生物标志物与临床结局的关联分析
本环节的核心目标是筛选与CAR-T相关并发症显著关联的止血生物标志物,评估其临床预测效能。研究采用单因素和多因素Logistic回归分析各指标与临床结局的关联,通过受试者工作特征(ROC)曲线评估标志物的预测效能,采用约登指数确定最佳截断值。结果显示,基线ETP水平与临床相关CRS风险显著相关,ETP每升高1倍,临床相关CRS的发生风险升高12.39倍(OR=12.39,95%CI 1.46-105.06,n=62,P=0.02),其预测ROC曲线下面积(AUC)为0.72(95%CI 0.6-0.9),最佳截断值为99.8%,对应的敏感性为77.8%,特异性为65.7%。基线CRP水平与ICANS风险显著相关,单因素分析显示CRP每升高1倍,ICANS发生风险升高1.66倍(OR=1.66,P<0.01),多因素校正后仍为独立危险因素(OR=1.86,95%CI 1.28-2.69,n=62,P<0.01),其预测AUC为0.78(95%CI 0.6-0.9),最佳截断值为1.66mg/dL,敏感性为62.5%,特异性为94.6%。出血风险相关的标志物中,基线P选择素水平与出血风险显著负相关,P选择素每升高1倍,出血风险降低80%(OR=0.20,95%CI 0.05-0.82,n=62,P=0.03),其预测AUC为0.67(95%CI 0.42-0.93),最佳截断值为34.8ng/mL,敏感性为50.0%,特异性为89.6%;基线血小板计数与出血风险也呈显著负相关,血小板计数每升高1倍,出血风险降低61%(OR=0.39,95%CI 0.21-0.74,n=62,P<0.01),其预测AUC为0.73(95%CI 0.45-1.0),最佳截断值为102×10^9/L,敏感性为75.0%,特异性为83.3%。各标志物的预测ROC曲线见下图:
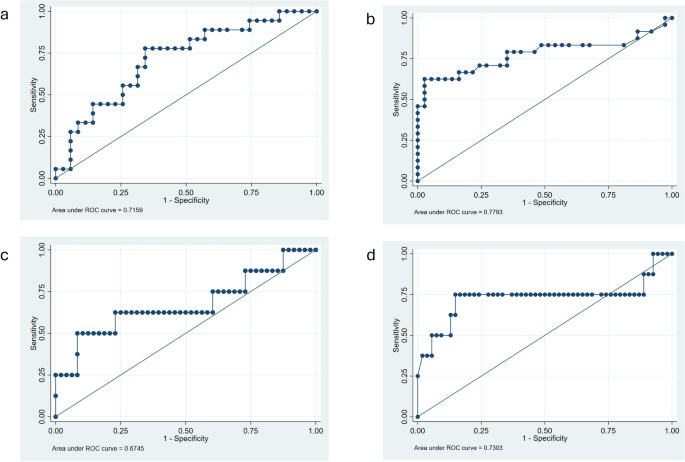
由于血栓事件发生率过低,未进行相关标志物的关联分析。本环节所用关键产品与上述检测环节一致。
4. Biomarker研究及发现成果
本研究涉及的Biomarker包括凝血功能整体评估类(内源性凝血酶潜能ETP)、炎症类(C反应蛋白CRP)、血小板/内皮激活类(P选择素)、常规血液学类(血小板计数)四类,筛选验证逻辑遵循“基线水平检测→单因素关联分析→多因素校正排除混杂→ROC曲线评估预测效能”的完整链条,结果可靠。
所有Biomarker的检测样本均来自患者外周静脉血,无需侵入性操作,临床可及性高。ETP通过全自动凝血酶生成实验检测,操作标准化程度高;CRP通过乳胶免疫比浊法检测,是临床常规检测项目;P选择素通过ELISA法检测,目前已在部分临床中心开展;血小板计数通过常规血常规检测,临床普及度极高。各标志物的预测效能数据明确:基线ETP预测临床相关CRS的AUC为0.72(95%CI 0.6-0.9,n=62,P=0.02),敏感性77.8%,特异性65.7%;基线CRP预测ICANS的AUC为0.78(95%CI 0.6-0.9,n=62,P<0.01),敏感性62.5%,特异性94.6%;基线P选择素预测出血的AUC为0.67(95%CI 0.42-0.93,n=62,P=0.03),敏感性50.0%,特异性89.6%;基线血小板计数预测出血的AUC为0.73(95%CI 0.45-1.0,n=62,P<0.01),敏感性75.0%,特异性83.3%。
本研究的核心成果包括三个方面:第一,首次发现基线ETP水平与临床相关CRS风险显著正相关,证实凝血功能基线状态与CAR-T相关炎症综合征的发生存在关联,为CRS的风险分层提供了新的凝血相关标志物;第二,证实基线CRP是ICANS的独立预测因素,且截断值1.66mg/dL具有较高的特异性,可作为临床术前评估ICANS风险的简单易用指标;第三,明确基线P选择素和血小板计数降低是出血的独立危险因素,其中血小板计数的最佳截断值为102×10^9/L,提示临床可考虑调整CAR-T患者抗凝预防的血小板阈值,从传统的50×10^9/L提升至100×10^9/L,以降低治疗后的出血风险。推测:后续可扩大样本量进一步验证上述标志物的预测效能,探索联合多个标志物建立风险预测模型,以提升预测的准确性,为CAR-T患者的个体化并发症防控提供更精准的依据。
