1. 领域背景与文献
文献英文标题:Nintedanib enhances the antitumor efficacy of pd-1 blockade, potentially through inhibition of myeloid-derived suppressor cells and cancer-associated fibroblasts;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:肿瘤免疫治疗。
领域共识:程序性死亡受体1(programmed cell death-1, PD-1)/程序性死亡配体1(PD-L1)免疫检查点抑制剂是当前肿瘤免疫治疗的核心手段,2014年首个PD-1抑制剂获批上市以来,已在黑色素瘤、非小细胞肺癌、头颈部鳞状细胞癌等多种实体瘤中展现出持久的抗肿瘤应答,但临床数据显示仅有约20%-40%的患者能从中获益,原发性或获得性耐药是限制其临床应用的核心瓶颈。当前研究热点集中于探索免疫耐药机制及联合治疗策略,其中肿瘤微环境中的髓系来源抑制细胞(myeloid-derived suppressor cells, MDSCs)、癌相关成纤维细胞(cancer-associated fibroblasts, CAFs)被证实是介导PD-1抑制剂耐药的关键因素,二者可通过抑制效应T细胞的活化、增殖及肿瘤浸润,形成“免疫排斥型”或“免疫沙漠型”肿瘤微环境,而现有针对单一免疫抑制细胞的干预策略疗效有限,缺乏同时靶向多重免疫抑制通路的联合方案。本研究针对这一空白,探索多靶点酪氨酸激酶抑制剂尼达尼布联合PD-1抑制剂的抗肿瘤效果及机制,为克服PD-1抑制剂耐药提供新的联合治疗范式。
2. 文献综述解析
本部分核心评述逻辑按照“免疫检查点抑制剂耐药机制→肿瘤微环境免疫抑制细胞的作用→靶向相关通路的药物潜力”的维度展开,系统梳理现有研究的进展与不足。
现有研究的关键支持结论包括:PD-1/PD-L1抑制剂通过阻断PD-1与PD-L1的结合,重新活化耗竭的肿瘤特异性T细胞发挥抗肿瘤作用,多项III期临床试验已证实其较传统化疗可显著延长多种实体瘤患者的生存期;肿瘤微环境中的MDSCs可抑制肿瘤引流淋巴结中效应T细胞的致敏,CAFs可阻碍效应T细胞向肿瘤实质浸润,二者共同介导PD-1抑制剂耐药;血管内皮生长因子(VEGF)、成纤维细胞生长因子(FGF)、血小板衍生生长因子(PDGF)等细胞因子是诱导MDSCs和CAFs生成及活化的关键上游信号,阻断上述通路可改善肿瘤免疫抑制微环境。现有技术方法的优势在于,单靶点抗血管生成药物可一定程度上减少MDSCs浸润,但其仅靶向VEGF通路,无法同时抑制CAFs活化相关的FGF、PDGF通路,临床转化价值有限;局限性包括:现有联合方案多聚焦于PD-1抑制剂与单靶点药物的组合,未能同时覆盖MDSCs和CAFs两类关键免疫抑制细胞的调控通路,且缺乏对相关机制的系统验证。
本研究的创新价值在于,首次探索同时靶向VEGFR、FGFR、PDGFR的多激酶抑制剂尼达尼布与PD-1抑制剂的联合效应,系统揭示其通过同时抑制MDSCs和CAFs增强抗肿瘤免疫的机制,弥补了现有联合治疗策略的不足,为PD-1抑制剂耐药患者的治疗提供了新的潜在方案。
3. 研究思路总结与详细解析
本研究的核心目标是明确尼达尼布联合PD-1抑制剂的抗肿瘤疗效及相关免疫调控机制,核心科学问题是尼达尼布是否可通过抑制MDSCs和CAFs改善肿瘤免疫抑制微环境,增强PD-1抑制剂的抗肿瘤效果;技术路线遵循“假设提出→转录组学初筛→免疫细胞表型验证→功能验证→体内疗效验证”的闭环逻辑:首先提出“尼达尼布可通过阻断VEGF、FGF、PDGF通路抑制MDSCs和CAFs,增强PD-1抑制剂疗效”的假设,随后通过RNA测序分析联合治疗对肿瘤组织基因表达谱的影响,再通过流式细胞术、免疫组化等方法验证尼达尼布对MDSCs、CAFs及肿瘤浸润淋巴细胞的调控作用,最后通过小鼠移植瘤模型验证联合治疗的体内抗肿瘤效果。
3.1 肿瘤组织转录组学分析
本环节核心目标是明确尼达尼布联合PD-1抑制剂对肿瘤组织免疫相关基因表达谱的影响,初步探索其作用机制。
方法细节:采用CT26结肠癌荷瘤BALB/c小鼠模型,第5天腹腔注射10mg/kg PD-1单抗,同时第5-11天灌胃给予50mg/kg尼达尼布,第12天收集肿瘤组织进行bulk RNA测序,采用基因集富集分析(GSEA)对差异表达基因进行功能富集分析。
结果解读:火山图显示,与PD-1单抗单药组相比,联合用药组有295个基因表达下调(倍数变化<0.5),7个基因表达上调(倍数变化>2);GSEA分析显示,联合用药组的上皮间质转化、血管生成、IL-6/JAK/STAT3信号通路等特征基因集显著富集下调,同时MDSCs、CAFs相关特征基因集及VEGF、PDGF、FGF通路基因集也显著下调(标准化富集分数NES均<0,P<0.05),提示尼达尼布可同时抑制MDSCs、CAFs相关基因表达及上游调控通路。
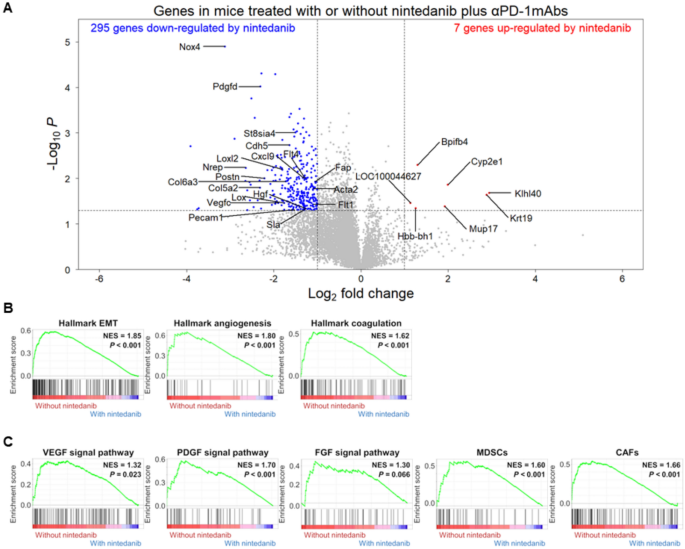
产品关联:文献未提及具体实验产品,领域常规使用RNA提取试剂盒、转录组建库试剂盒及二代测序平台完成相关实验。
3.2 尼达尼布对髓系来源抑制细胞的调控作用验证
本环节核心目标是验证尼达尼布对MDSCs的扩增及免疫抑制功能的影响。
方法细节:采用CT26荷瘤小鼠模型,第5、12、19、26、33天给予PD-1单抗,第5-39天给予尼达尼布,第40天收集脾脏及肿瘤组织,通过流式细胞术检测CD11b+Gr-1+Ly-6G+多形核MDSCs(PMN-MDSCs)及CD11b+Gr-1+Ly-6C+单核MDSCs(M-MDSCs)的比例;分离尼达尼布处理或未处理荷瘤小鼠的脾脏MDSCs,与活化的肿瘤引流淋巴结细胞、CT26肿瘤细胞共培养24h,流式检测CD4+、CD8+T细胞的干扰素-γ(IFN-γ)分泌水平。
结果解读:流式结果显示,尼达尼布可显著降低脾脏及肿瘤组织中总MDSCs和PMN-MDSCs的比例(n=5,P<0.05);功能实验显示,未接受尼达尼布处理小鼠的MDSCs可显著抑制CD4+、CD8+T细胞的IFN-γ分泌(n=5,P<0.01),而尼达尼布处理组的MDSCs无明显免疫抑制功能,提示尼达尼布不仅可减少MDSCs的扩增,还可削弱其免疫抑制活性。
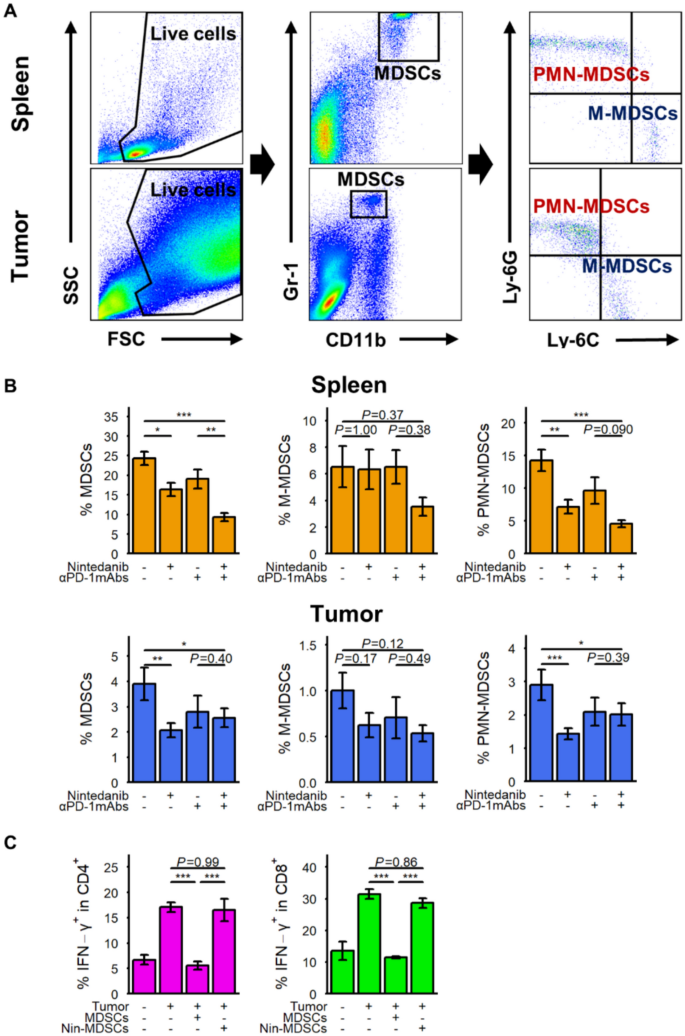
产品关联:实验所用关键产品:BD的流式抗体(抗CD11b、Gr-1、Ly-6G、Ly-6C、IFN-γ等)、美天旎的髓系来源抑制细胞分离试剂盒(货号130-094-538)。
3.3 尼达尼布对癌相关成纤维细胞的调控作用验证
本环节核心目标是验证尼达尼布对肿瘤微环境中CAFs的抑制作用。
方法细节:采用GFP转基因小鼠接种MC38结肠癌细胞,第7、14天给予PD-1单抗,第5-20天给予尼达尼布,第21天收集肿瘤组织,流式检测GFP+CD45-细胞中αSMA+PDPN+及αSMA+CD90+ CAFs的比例。
结果解读:流式结果显示,尼达尼布可显著降低肿瘤组织中αSMA+PDPN+及αSMA+CD90+ CAFs的比例(n=5,P<0.05),提示尼达尼布可有效抑制肿瘤微环境中CAFs的积累。
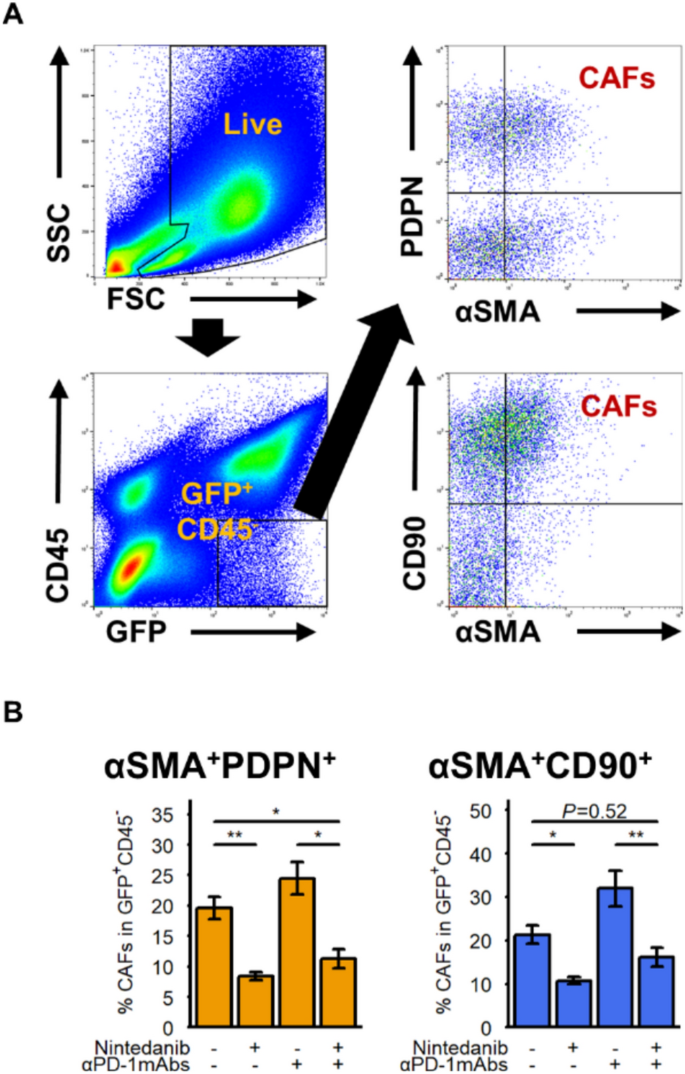
产品关联:文献未提及CAFs检测相关的具体抗体品牌,领域常规使用抗αSMA、PDPN、CD90的流式抗体完成检测。
3.4 尼达尼布对肿瘤浸润淋巴细胞的调控作用验证
本环节核心目标是明确尼达尼布对肿瘤微环境中效应T细胞浸润及功能的影响。
方法细节:CT26荷瘤小鼠第10、15天给予PD-1单抗,第0-18天给予尼达尼布,第19天收集肿瘤组织,分别通过流式细胞术检测肿瘤浸润CD4+、CD8+T细胞的IFN-γ分泌水平,通过免疫组化(immunohistochemistry, IHC)检测肿瘤边缘区及内部区域的CD4+、CD8+T细胞数量。
结果解读:流式结果显示,尼达尼布可显著提高肿瘤浸润CD4+、CD8+T细胞中IFN-γ阳性细胞的比例(n=5,P<0.01);免疫组化结果显示,尼达尼布可显著增加肿瘤边缘区的CD4+T细胞密度,以及边缘区和内部区域的CD8+T细胞密度(n=5,P<0.001),提示尼达尼布可促进效应T细胞向肿瘤实质浸润并增强其功能。
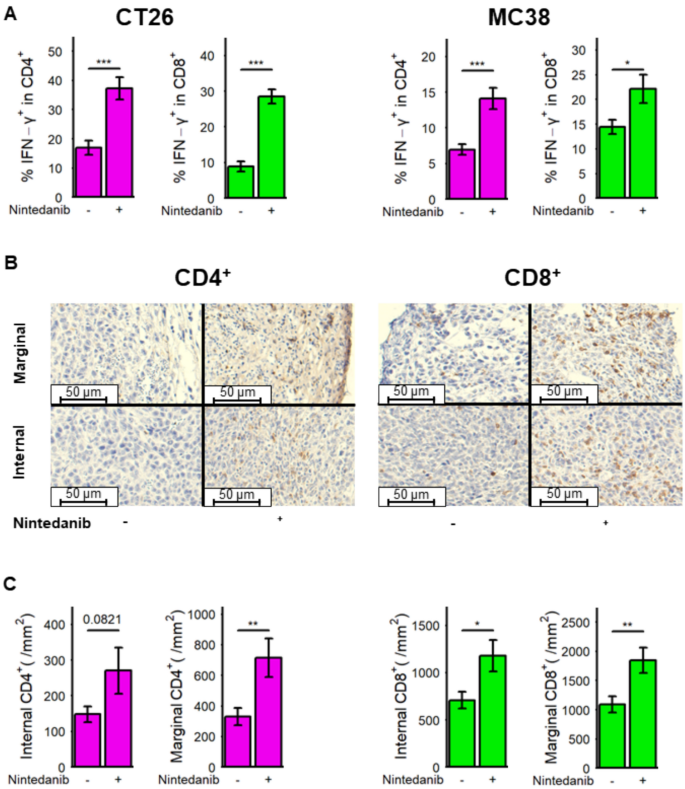
产品关联:实验所用关键产品:Nichirei Corporation的抗CD4抗体(货号413951)、抗CD8抗体(货号413201)、Histofine Simple Stain MAX-PO(multi)试剂盒(货号414191)、DAB底物试剂盒(货号725191)。
3.5 联合治疗的体内抗肿瘤疗效验证
本环节核心目标是验证尼达尼布联合PD-1抑制剂的体内抗肿瘤效果。
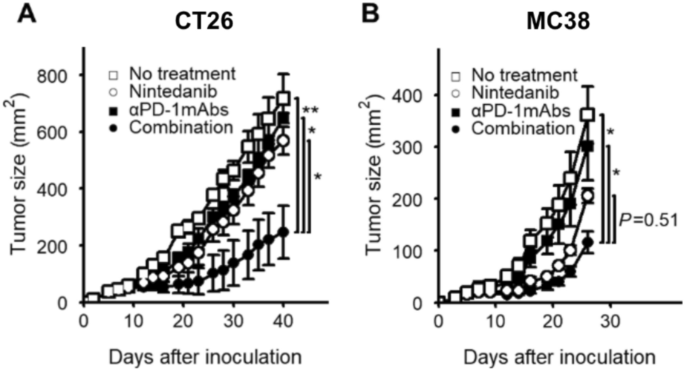
方法细节:分别构建CT26(BALB/c背景)及MC38(C57BL/6背景)结肠癌移植瘤模型,尼达尼布按50mg/kg每日灌胃给药,PD-1单抗按10mg/kg每7天腹腔注射给药,每周3次测量肿瘤面积,评估肿瘤生长情况。
结果解读:与单药组相比,尼达尼布联合PD-1单抗可显著抑制CT26及MC38移植瘤的生长(n=5,P<0.01),提示二者联合具有显著的协同抗肿瘤效应。
产品关联:实验所用关键产品:Bio X cell的抗PD-1单抗(货号BE0146)、ChemScene的尼达尼布(货号CS-0104)。
4. Biomarker研究及发现成果
本研究涉及的生物标志物主要包括免疫抑制细胞标志物及效应免疫细胞标志物两类,用于评估尼达尼布对肿瘤免疫微环境的调控效果及联合治疗的响应预测,筛选验证逻辑遵循“转录组水平特征基因富集→细胞水平表型验证→功能水平验证→疗效关联”的完整链条。
免疫抑制相关Biomarker包括髓系来源抑制细胞(PMN-MDSCs表型为CD11b+Gr-1+Ly-6G+、M-MDSCs表型为CD11b+Gr-1+Ly-6C+)、癌相关成纤维细胞(表型为αSMA+PDPN+、αSMA+CD90+),检测样本为荷瘤小鼠的脾脏、肿瘤组织,采用流式细胞术进行定量检测,结果显示尼达尼布处理后脾脏PMN-MDSCs比例较对照组降低约30%(n=5,P<0.05),肿瘤组织CAFs比例降低约40%(n=5,P<0.01);免疫激活相关Biomarker包括IFN-γ+CD4+T细胞、IFN-γ+CD8+T细胞,检测样本为肿瘤组织,采用流式细胞术及免疫组化检测,结果显示尼达尼布处理后肿瘤浸润CD8+T细胞中IFN-γ阳性比例升高约2.1倍(n=5,P<0.01),肿瘤内部区域CD8+T细胞密度升高约1.8倍(n=5,P<0.001);文献未明确报道上述Biomarker的ROC曲线下面积、敏感性特异性数据。
核心成果提炼:本研究证实,尼达尼布可显著降低肿瘤微环境中MDSCs、CAFs的丰度及免疫抑制功能,同时提高效应T细胞的浸润及IFN-γ分泌水平,上述Biomarker的变化与联合治疗的抗肿瘤疗效显著相关(P<0.01);创新性在于首次证实尼达尼布可同时靶向MDSCs和CAFs两类免疫抑制细胞,为PD-1抑制剂联合治疗的响应人群筛选提供了潜在的Biomarker组合。推测:本研究发现的MDSCs、CAFs及效应T细胞的表达特征组合,可作为后续临床研究中尼达尼布联合PD-1抑制剂治疗响应的预测标志物,需进一步大样本验证。
