1. 领域背景与文献
文献英文标题:Allogeneic CD56 + cell infusion as a bridge to hematopoietic stem cell transplantation in relapsed/refractory acute myeloid leukemia: a phase I clinical trial;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:血液肿瘤免疫治疗(复发难治性急性髓系白血病细胞治疗)。
领域共识:急性髓系白血病是造血干祖细胞发生克隆性恶性增殖导致的血液系统肿瘤,成人患者的标准一线治疗为强化化疗序贯异基因造血干细胞移植(HSCT),但复发/难治性患者的临床预后极差,5年总生存率在老年患者中仅为8.3%,年轻患者也不足50%。该领域的核心发展节点包括:2005年首次证实半相合自然杀伤(NK)细胞输注在高危急性髓系白血病中的安全性与抗白血病活性;2018年多项I期临床试验验证自然杀伤细胞输注可作为桥接治疗使复发/难治性患者获得异基因造血干细胞移植机会;当前研究热点聚焦于优化自然杀伤细胞制备工艺、增强体内抗肿瘤活性、降低治疗成本。目前领域未解决的核心问题包括:复发/难治性急性髓系白血病缺乏高效低毒的挽救治疗方案,现有自然杀伤细胞产品多采用多步富集工艺,制备成本高、周期长,难以在临床广泛推广;自然杀伤细胞联合NKT样细胞输注的协同抗肿瘤效应与安全性尚未得到临床验证。
针对上述临床需求,本研究探索采用单步磁珠富集工艺制备CD56+细胞(包含自然杀伤细胞与NKT样细胞),联合氟达拉滨联合阿糖胞苷及粒细胞集落刺激因子(FLAG)预处理方案,评估其在复发/难治性非M3型急性髓系白血病患者中的安全性与可行性,旨在为该类患者提供一种可及性更高的桥接异基因造血干细胞移植治疗方案,填补现有细胞治疗产品临床可及性不足的研究空白。
2. 文献综述解析
本研究作者对领域现有研究的分类维度为细胞产品制备工艺、预处理方案选择、临床应用场景三类,系统梳理了自然杀伤细胞治疗急性髓系白血病的研究进展与局限性。
现有研究的支持结论包括:半相合来源的自然杀伤细胞具有明确的抗白血病活性,当供受者存在杀伤细胞免疫球蛋白样受体(KIR)配体错配时,可增强移植物抗白血病(GVL)效应且不会增加移植物抗宿主病(GVHD)风险;氟达拉滨联合阿糖胞苷及粒细胞集落刺激因子预处理方案作为复发/难治性急性髓系白血病的常用挽救化疗方案,可有效降低肿瘤负荷,同时通过淋巴细胞清除促进输注的免疫细胞体内增殖,提升细胞治疗疗效。现有技术的优势为:采用CD3阴性选择联合CD56阳性选择的多步富集工艺可获得高纯度自然杀伤细胞,已在多项I期临床试验中证实安全性,完全缓解率可达30%~50%,约30%的患者可成功桥接异基因造血干细胞移植。现有研究的局限性包括:多步富集工艺制备周期长、成本高,临床可及性较低;多数研究仅单独使用自然杀伤细胞,未探索NKT样细胞联合输注的协同效应;缺乏针对非M3型复发/难治性急性髓系白血病的大样本桥接治疗临床数据。
本研究的创新价值体现在两方面:一是首次采用单步CD56阳性选择工艺制备混合自然杀伤/NKT样细胞产品,大幅简化制备流程、降低制备成本,提升细胞治疗的临床可及性;二是首次在复发/难治性非M3型急性髓系白血病人群中评估氟达拉滨联合阿糖胞苷及粒细胞集落刺激因子预处理方案联合CD56+细胞输注的桥接治疗价值,同时探索NKT样细胞在降低移植物抗宿主病风险、增强抗白血病活性中的协同作用,为后续大样本研究提供了基础数据支持。
3. 研究思路总结与详细解析
本研究的核心目标是评估氟达拉滨联合阿糖胞苷及粒细胞集落刺激因子预处理方案联合杀伤细胞免疫球蛋白样受体配体错配的异基因CD56+细胞输注,治疗复发/难治性非M3型急性髓系白血病的安全性与可行性;核心科学问题为单步富集的CD56+细胞产品能否在保证安全性的前提下有效降低患者肿瘤负荷,使其满足异基因造血干细胞移植的纳入标准;技术路线遵循“I期临床试验设计→患者与供者筛选→CD56+细胞制备与质控→预处理联合细胞输注→安全性与疗效随访→统计分析”的闭环逻辑。
3.1 临床试验设计与入组筛选
实验目的为明确试验设计规范,筛选符合要求的复发/难治性急性髓系白血病患者与杀伤细胞免疫球蛋白样受体配体错配供者,保证研究的科学性与伦理合规性。
方法细节方面,本研究为单中心、开放标签、非随机I期临床试验,经所属机构伦理委员会批准(编号IR.SBMU.RETECH.REC.1402.153)并注册于伊朗临床试验注册中心(编号IRCT20230801058996N3),所有患者与供者均签署书面知情同意书。患者入组标准为:年龄≥18岁,非M3型复发/难治性急性髓系白血病(复发定义为初始完全缓解后骨髓原始细胞占比>5%,难治定义为至少2疗程诱导化疗未达到完全缓解),卡氏功能状态评分≥70%,无异基因造血干细胞移植史,器官功能满足治疗要求。供者入组标准为:18~50岁的患者直系亲属,存在移植物抗宿主方向的杀伤细胞免疫球蛋白样受体配体错配,无活动性感染,血常规与生化指标均处于正常范围。
结果解读显示,共15例患者签署知情同意书,12例符合入组标准,其中1例在预处理前发生肺部感染退出研究,最终11例患者纳入分析(n=11)。入组患者中位年龄为41.5岁(范围22~64岁),男性6例,中位既往化疗线数为3线(范围2~5线),入组时骨髓原始细胞中位占比为18%(范围7%~91%),所有患者均不符合异基因造血干细胞移植的纳入标准。
产品关联:文献未提及具体实验产品,领域常规使用临床试验伦理审查体系、人类白细胞抗原/杀伤细胞免疫球蛋白样受体基因分型试剂。
3.2 CD56+细胞产品制备与质控
实验目的为制备符合临床输注标准的高纯度CD56+细胞产品,保证产品的安全性与批次一致性。
方法细节方面,供者首先接受4小时的外周血白细胞单采(采用Spectra Optia单采系统,Terumo BCT),采集的单个核细胞采用CliniMACS Plus设备与抗CD56微珠(Miltenyi Biotec,货号200-070-206)进行单步阳性选择,富集CD56+细胞。产品质控内容包括:采用BACTEC 9120系统进行无菌检测(涵盖需氧菌、厌氧菌、真菌),采用支原体检测试剂盒(PrimerDesign,货号z-path-mycoplasma)进行支原体检测,采用鲎试剂试剂盒(Charles River,货号R13012)进行内毒素检测,采用流式细胞术检测细胞表型(所用CD3、CD16、CD56、CD14、CD19抗体均来自Miltenyi Biotec),采用7-氨基放线菌素D染色(新鲜细胞)或台盼蓝染色(冻融细胞)检测细胞活性。产品放行标准为:新鲜细胞活性>90%、冻融后细胞活性>70%,CD56+细胞占比≥90%,CD3+CD56- T细胞占比<1%,CD19+B细胞与CD14+单核细胞占比各<5%,内毒素含量<0.125 EU/ml,无菌与支原体检测结果为阴性。
结果解读显示,所有制备的CD56+细胞产品均符合放行标准,中位单采体积为242 ml,富集前产品中自然杀伤细胞中位数量为5.5×10^8、NKT样细胞中位数量为7.0×10^8;富集后CD56+细胞中位纯度为96.9%(范围90.6%~99.1%,n=11),回收率为59.3%,T细胞清除的中位log值为-3.11,新鲜产品中位活性为96.5%,冻融后产品中位活性为86%。细胞富集前后的代表性流式细胞术检测结果如下:
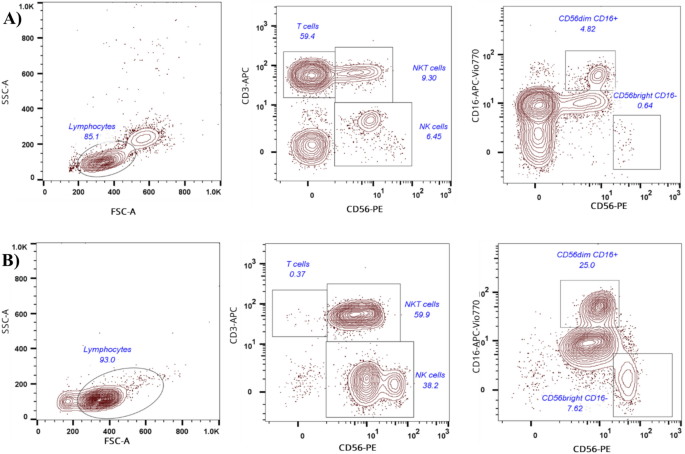
产品关联:实验所用关键产品:Terumo BCT的Spectra Optia单采系统,Miltenyi Biotec的CliniMACS Plus设备、CD56富集试剂(货号200-070-206)、流式检测抗体、7-氨基放线菌素D染色试剂(货号130-111-568),PrimerDesign的支原体检测试剂盒(货号z-path-mycoplasma),Charles River的内毒素检测试剂盒(货号R13012)。
3.3 治疗方案实施
实验目的为明确标准化治疗流程,评估该方案的安全性与耐受性。
方法细节方面,患者在首次CD56+细胞输注前7天至前2天接受氟达拉滨联合阿糖胞苷及粒细胞集落刺激因子预处理方案,具体为:氟达拉滨25 mg/m²/天(第-7天至第-3天静脉输注)、阿糖胞苷3 g/m²/天(第-7天至第-3天静脉输注)、粒细胞集落刺激因子5 μg/kg/天(第-6天至第-2天皮下注射)。预处理结束后休息2天,分别在第0、5、10天输注剂量为1×10^6、3×10^6、5×10^6 cells/kg的CD56+细胞,首次输注使用新鲜制备的细胞,后两次输注使用冻存复苏的细胞;输注前10分钟给予患者10 mg氯苯那敏或100 mg氢化可的松静脉输注,预防过敏反应;细胞输注后不给予外源性细胞因子支持。治疗流程示意图如下:
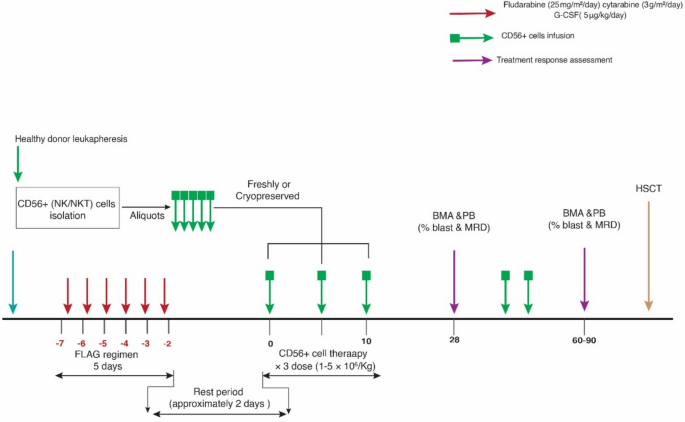
结果解读显示,所有患者均完成3次计划的细胞输注,未出现剂量限制性毒性,最高输注剂量5×10^6 cells/kg(为单步富集工艺的理论最高产量)耐受良好。未观察到3~5级输注相关不良反应,6例患者出现1~2级轻度不良反应(包括恶心、寒战、头痛、呕吐、骨痛),经对症处理后完全缓解,未发生移植物抗宿主病、细胞因子释放综合征、神经毒性事件。化疗相关不良反应为预期的血液学毒性:中性粒细胞减少发生率为100%(50%为2级,其余为3~4级,n=11),血小板减少发生率为83.3%(58.3%为1~2级,25%为3级,n=12),贫血发生率为58.3%,25%的患者出现发热性中性粒细胞减少,无治疗相关死亡事件发生。
产品关联:文献未提及具体化疗药物品牌,领域常规使用氟达拉滨、阿糖胞苷、粒细胞集落刺激因子类化疗药物。
3.4 临床疗效评估与随访
实验目的为评估该治疗方案的抗肿瘤活性,明确其作为异基因造血干细胞移植桥接治疗的有效性。
方法细节方面,疗效评估参照国际工作组制定的急性髓系白血病疗效标准,分别在细胞输注后第28天、第60~90天进行骨髓穿刺检查,采用流式细胞术检测微小残留病(MRD)状态。总生存期定义为首次细胞输注至全因死亡的时间,无事件生存期定义为首次细胞输注至复发、疾病进展或死亡的时间。
结果解读显示,中位随访时间为6.5个月(范围2~19个月,n=11),输注后第28天疗效评估显示,5例(45.4%,n=11)患者达到完全缓解或完全缓解伴不完全血液学恢复,其中4例(36.3%,n=11)患者满足异基因造血干细胞移植纳入标准,并接受人类白细胞抗原相合的异基因造血干细胞移植,中位桥接时间为85天(范围57~128天),至随访终点时4例移植患者均维持无事件生存。1例达到完全缓解的患者在2个月后复发,最终死于疾病进展;其余6例未缓解患者接受后续挽救化疗。全队列的1年总生存率与无事件生存率均为36.4%(95%置信区间:10.9%~69.2%,n=11);达到完全缓解/完全缓解伴不完全血液学恢复的患者1年无事件生存率为80.0%(95%置信区间:28.4%~99.5%,P=0.015,n=5),显著高于未缓解患者;接受异基因造血干细胞移植的患者1年无事件生存率为100%(95%置信区间:39.8%~100%,P=0.005,n=4),显著高于未接受移植的患者。疗效结果示意图如下:
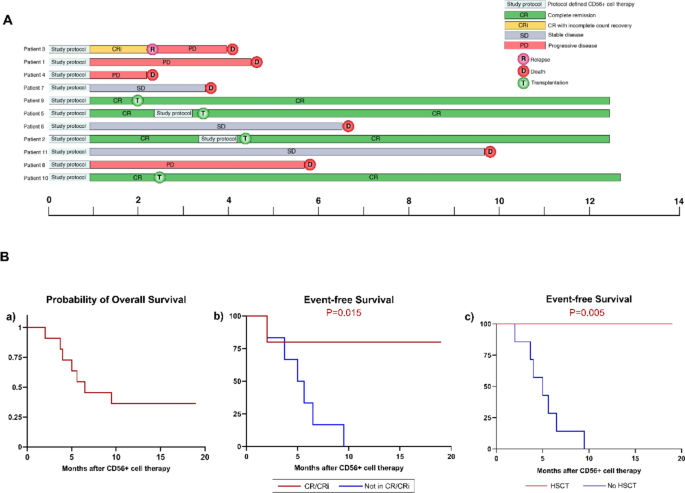
产品关联:文献未提及具体流式检测试剂品牌,领域常规使用急性髓系白血病微小残留病检测流式抗体套餐。
推测:本研究采用的单步CD56+富集工艺可在保证产品纯度与安全性的前提下,大幅降低细胞制备成本与周期,适合在医疗资源有限地区推广,其疗效需后续大样本II期临床试验进一步验证。
4. Biomarker 研究及发现成果
本研究未针对疾病诊断或预后相关的新型生物标志物进行探索,主要涉及两类已在临床应用的生物标志物,分别为供者筛选相关的杀伤细胞免疫球蛋白样受体配体错配,以及疗效评估相关的骨髓原始细胞比例、微小残留病状态。
生物标志物定位与筛选逻辑方面,杀伤细胞免疫球蛋白样受体配体错配作为供者筛选的核心生物标志物,其筛选逻辑基于既往研究证实的该标志物可增强自然杀伤细胞的移植物抗白血病效应,且不增加移植物抗宿主病风险;骨髓原始细胞比例与微小残留病状态作为急性髓系白血病疗效评估的常规生物标志物,用于判断患者的治疗应答与异基因造血干细胞移植的适宜性。研究过程中,杀伤细胞免疫球蛋白样受体配体错配采用PCR基因分型方法检测,通过比对供受者的人类白细胞抗原C1/C2、Bw4表位,当患者缺乏供者的至少1种抑制性杀伤细胞免疫球蛋白样受体配体时,判定为配体错配;骨髓原始细胞比例采用骨髓涂片形态学检测,微小残留病采用多参数流式细胞术检测(使用急性髓系白血病特异性抗体套餐)。本研究未针对上述标志物的诊断敏感性、特异性进行单独分析,所有入组患者的供者均符合杀伤细胞免疫球蛋白样受体配体错配标准,5例应答患者治疗后骨髓原始细胞比例降至5%以下,其中1例患者达到微小残留病阴性。
核心成果提炼方面,杀伤细胞免疫球蛋白样受体配体错配作为供者筛选标志物,可保证输注的CD56+细胞具有稳定的移植物抗白血病活性,本研究中所有输注细胞均来自配体错配供者,未发生移植物抗宿主病,同时实现了45.4%的完全缓解率(n=11),提示该筛选策略的安全性与有效性;微小残留病阴性作为疗效预后标志物,1例达到微小残留病阴性的患者成功接受异基因造血干细胞移植并维持长期无事件生存,与已发表的临床研究中微小残留病阴性患者异基因造血干细胞移植预后更佳的结论一致。本研究未提供上述标志物的单独统计学分析数据(如受试者工作特征曲线下面积、风险比等)。
推测:杀伤细胞免疫球蛋白样受体配体错配的供者筛选策略可进一步推广至其他自然杀伤细胞相关的细胞治疗研究中,需后续研究验证该标志物与治疗应答的相关性。
