1. 领域背景与文献
文献英文标题:Mega-scale single-cell profiling reveals novel biomarkers associated with acute GvHD after allogeneic hematopoietic stem cell transplantation;发表期刊:Biomarker Research;影响因子:未公开;研究领域:血液肿瘤异基因造血干细胞移植免疫生物标志物研究。
领域共识:异基因造血干细胞移植(allogeneic hematopoietic stem cell transplantation, alloHSCT)是目前复发/难治性急性髓系白血病(acute myeloid leukemia, AML)唯一的治愈性手段,其疗效依赖于供体来源T细胞介导的移植物抗白血病(graft-versus-leukemia, GvL)效应,但该效应同时会攻击受体正常组织,导致移植物抗宿主病(graft-versus-host disease, GvHD)的发生,两者的平衡是决定移植预后的核心因素。领域发展关键节点包括1990年首次明确移植物抗白血病效应的核心作用,2010年后随着单细胞RNA测序(single-cell RNA sequencing, scRNA-seq)等高通量技术的普及,研究重点从临床特征分析转向细胞分子层面的机制解析。当前研究热点主要集中在移植后免疫重建动态追踪、移植物抗白血病/急性移植物抗宿主病特异性生物标志物筛选、免疫干预靶点开发三个方向。目前领域未解决的核心问题包括:缺乏可早期、无创区分移植物抗白血病效应和急性移植物抗宿主病的特异性生物标志物,无法实现移植后患者的精准风险分层,导致干预时机延误或过度治疗;已发现的潜在标志物多局限于骨髓样本,外周血适用性不足,难以推广至临床常规监测。
针对上述研究空白,本研究采用超大规模组合条形码单细胞RNA测序技术,纵向追踪10例急性髓系白血病患者移植前移植物、移植后30天、100天外周血的免疫细胞转录组特征,筛选与急性移植物抗宿主病、移植物抗白血病效应相关的新型外周血生物标志物,为移植后预后评估和干预靶点开发提供新的依据。
2. 文献综述解析
本部分核心内容为梳理领域现有研究进展,明确本研究的创新定位,作者对现有研究的分类维度为按研究方向划分为移植物抗白血病效应机制、急性移植物抗宿主病发病机制、生物标志物研究进展三类。
现有研究的关键支持结论包括:同种反应性CD8+T细胞是介导移植物抗白血病效应的核心细胞亚群,近年研究在骨髓样本中发现ADGRG1(GPR56)、ZNF683(HOBIT)可作为同种反应性细胞毒性T细胞的标志物,与移植后完全缓解显著相关;急性移植物抗宿主病的发生与供体来源的CXCR3+T细胞、CD11b+CD163+单核细胞浸润皮肤、胃肠道等靶器官密切相关。现有技术方法的优势在于,单细胞RNA测序技术可实现全转录组水平的无偏筛选,避免传统靶向检测的偏好性,近年已在移植免疫研究中成功鉴定多个潜在生物标志物。现有研究的局限性主要包括三方面:已发现的移植物抗白血病相关标志物仅在骨髓样本中得到验证,外周血中的表达特征尚不明确,临床采样便利性不足;现有急性移植物抗宿主病标志物多为泛炎症相关的细胞亚群或细胞因子,特异性不足,无法与感染等其他炎症性并发症区分;多数研究样本量较小、缺乏纵向动态追踪,结果的临床转化价值有限。
本研究的创新价值体现在三个层面:首次采用超大规模单细胞RNA测序技术,单次实验完成超过77万个细胞的转录组检测,大幅降低批次效应的影响;同时覆盖移植前、移植后两个随访时间点的纵向样本,可动态追踪免疫重建过程中的分子变化;不仅验证了ADGRG1在外周血细胞毒性T细胞中的移植物抗白血病预后价值,还首次发现MDGA1可作为急性移植物抗宿主病的新型标志物,两个标志物互不关联,可实现对两种临床结局的互补评估,弥补了现有研究的不足,为临床无创监测提供了新的候选靶点。
3. 研究思路总结与详细解析
本研究的核心目标是筛选可区分异基因造血干细胞移植后急性移植物抗宿主病和移植物抗白血病效应的外周血生物标志物,核心科学问题包括移植后供体来源免疫细胞的长期存活特征、预处理后残留宿主免疫细胞的表型特征、不同临床结局患者的免疫细胞转录组差异。技术路线采用“临床队列构建与样本采集→超大规模单细胞RNA测序与数据分析→生物标志物无偏筛选→多维度验证”的闭环逻辑,确保研究结果的可靠性。
3.1 临床队列构建与样本采集
实验目的:建立临床特征匹配的急性髓系白血病移植患者队列,收集纵向时间点样本用于免疫重建动态分析。
方法细节:纳入10例接受异基因造血干细胞移植的完全缓解期成年急性髓系白血病患者(n=10),其中8例为无关供者匹配移植,2例为亲缘供者匹配移植;7例接受清髓性预处理,9例接受抗胸腺细胞球蛋白免疫清除。采集三个时间点样本:移植时的外周血干细胞移植物样本(n=9)、移植后30天外周血单个核细胞(peripheral blood mononuclear cell, PBMC)样本(n=10)、移植后100天外周血单个核细胞样本(n=6),所有样本经密度梯度离心分离单个核细胞后程序性降温冻存备用。随访中位时间20个月,期间5例患者发生II-IV级急性移植物抗宿主病(n=5),2例患者出现复发(n=2),3例患者死亡(n=3)。
结果解读:该队列覆盖了异基因造血干细胞移植后常见的临床结局(急性移植物抗宿主病、复发、持续缓解),为后续生物标志物筛选提供了良好的临床基础。
产品关联:文献未提及具体实验产品,领域常规使用人外周血淋巴细胞分离液、程序性降温仪、细胞冻存液等样本处理类试剂与仪器。
3.2 超大规模单细胞RNA测序文库构建与测序
实验目的:实现大批量样本的无偏单细胞转录组检测,降低批次效应对结果的影响。
方法细节:复苏冻存样本后,流式分选4",6-二脒基-2-苯基吲哚(DAPI)阴性的活细胞,采用Parse Biosciences的Evercode™ WT Mega v2试剂盒进行组合条形码标记的单细胞文库构建,所有样本同时处理以避免批次效应。构建得到的15个子文库在Illumina NovaSeq 6000平台进行测序,测序深度设置为每个细胞25000条reads。
结果解读:共获得777920个高质量细胞的转录组数据,每个细胞中位转录本数为5931,中位检测基因数为2511,数据质量满足后续生物信息学分析要求。
产品关联:实验所用关键产品:Parse Biosciences的Evercode™ WT Mega v2试剂盒(货号ECW02050)、Thermo Fisher Scientific的DAPI染色试剂(货号D1306)、Illumina NovaSeq 6000测序平台。
3.3 单细胞转录组数据预处理与细胞注释
实验目的:对单细胞数据进行质控和细胞类型注释,建立异基因造血干细胞移植后免疫细胞转录组图谱。
方法细节:原始测序数据比对至人类参考基因组GRCh38(hg38),使用Seurat、Scanpy等分析工具进行质控,去除双细胞、低质量细胞后,采用Harmony算法整合不同样本数据消除批次效应,通过均匀流形近似与投影(UMAP)降维和Louvain/Leiden聚类,基于经典免疫细胞标志物基因注释细胞亚群。
结果解读:经过质控和注释,最终得到包括αβ T细胞、γδ T细胞、自然杀伤(NK)细胞、B细胞、单核细胞、树突状细胞在内的共45个免疫细胞亚型,覆盖了外周血所有主要免疫细胞类型,可用于后续免疫重建动态分析和差异基因筛选。对应细胞聚类图谱如下:
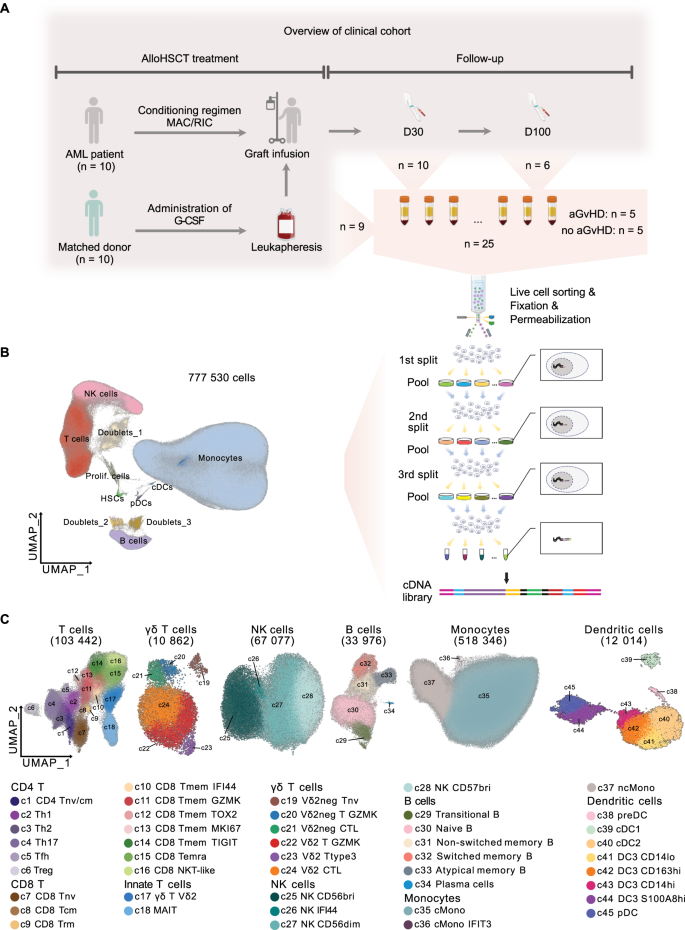
产品关联:文献未提及分析软件之外的实验产品,领域常规使用单细胞测序分析常用的生物信息学软件包。
3.4 供体来源免疫细胞的长期追踪与特征分析
实验目的:明确移植后供体来源免疫细胞的存活状态及功能特征。
方法细节:采用TRUST4算法从转录组数据中重建T细胞受体(TCR)和B细胞受体(BCR)序列,以互补决定区3(CDR3)序列作为克隆的特异性分子标签,追踪移植物和移植后样本中免疫细胞的克隆共享情况;对CD8+T细胞进行差异基因分析和功能富集分析,明确其激活状态。
结果解读:移植物中的αβ T细胞、γδ T细胞克隆可在移植后长期存活,而供体来源B细胞克隆未在移植后检出,与既往研究结果一致。持续存在的CD8+T细胞克隆发生显著克隆扩增,差异表达基因显著富集于细胞周期、代谢通路,呈现抗原诱导的激活表型,提示其具有潜在同种反应性。对应克隆追踪结果如下:
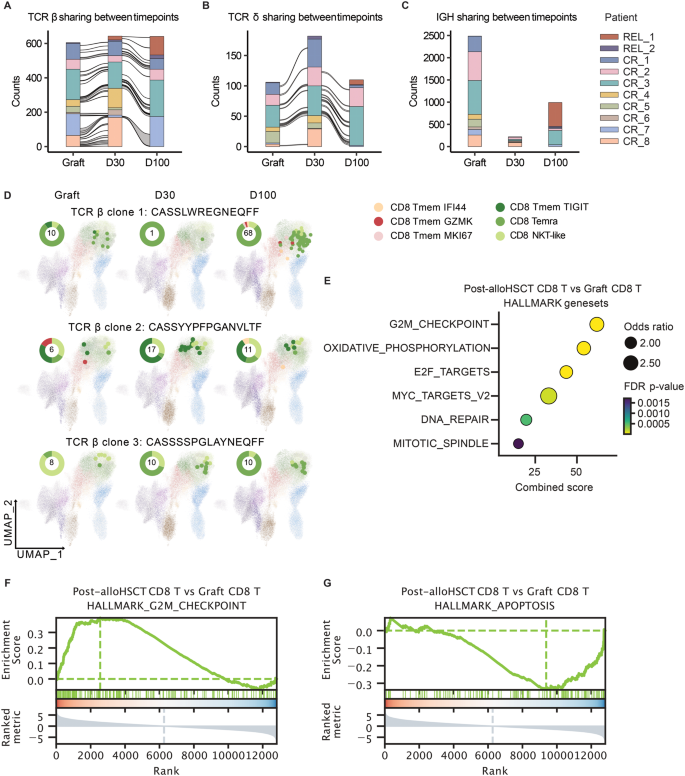
产品关联:文献未提及具体实验产品,领域常规使用TCR/BCR重建分析工具。
3.5 残留宿主免疫细胞的鉴定与表型分析
实验目的:明确清髓性预处理后残留的宿主免疫细胞的表型特征。
方法细节:针对性别错配移植的患者,通过性染色体相关基因(Y染色体基因UTY、DDX3Y等,X染色体基因XIST等)的表达打分区分供体和宿主来源细胞,比较两者的细胞亚群组成差异。
结果解读:共鉴定到1064个残留宿主来源细胞,其中98%以上为T细胞,且以CD4+辅助性T细胞为主,缺乏终末分化的CD8+效应T细胞亚群,提示残留宿主T细胞的抗白血病功能可能受损。对应细胞来源区分结果如下:
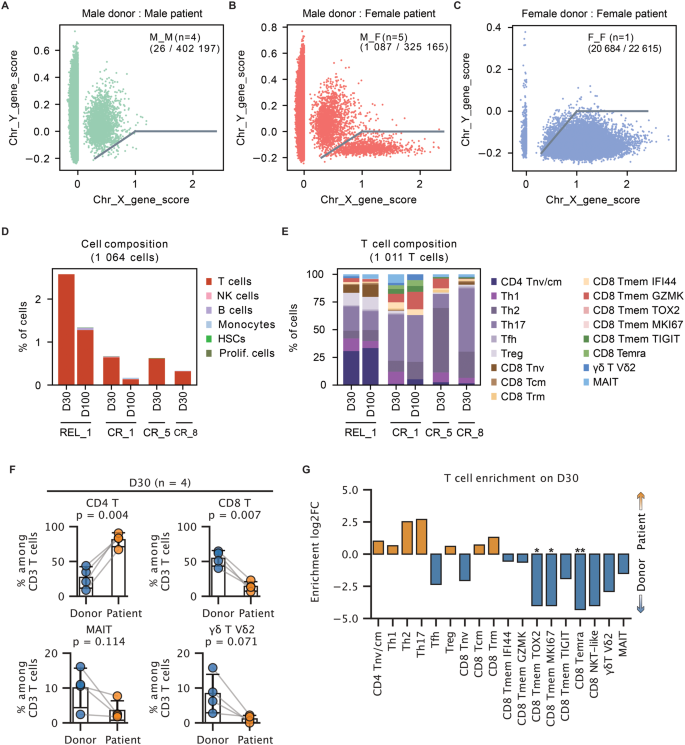
产品关联:文献未提及具体实验产品,领域常规使用基因集打分分析工具。
3.6 急性移植物抗宿主病相关标志物筛选与验证
实验目的:筛选与急性移植物抗宿主病发生相关的特异性分子标志物。
方法细节:比较急性移植物抗宿主病患者和无急性移植物抗宿主病患者移植后T细胞、自然杀伤细胞的差异表达基因,筛选候选标志物后,通过两个公共数据集验证其调控因素和疾病特异性:一是细胞因子处理的健康人外周血单个核细胞数据集,分析细胞因子对候选标志物的调控作用;二是多发性硬化患者外周血单细胞数据集,验证其在其他炎症性疾病中的表达特征;同时采用定量聚合酶链反应(quantitative polymerase chain reaction, qPCR)检测独立队列患者T细胞中的表达水平。
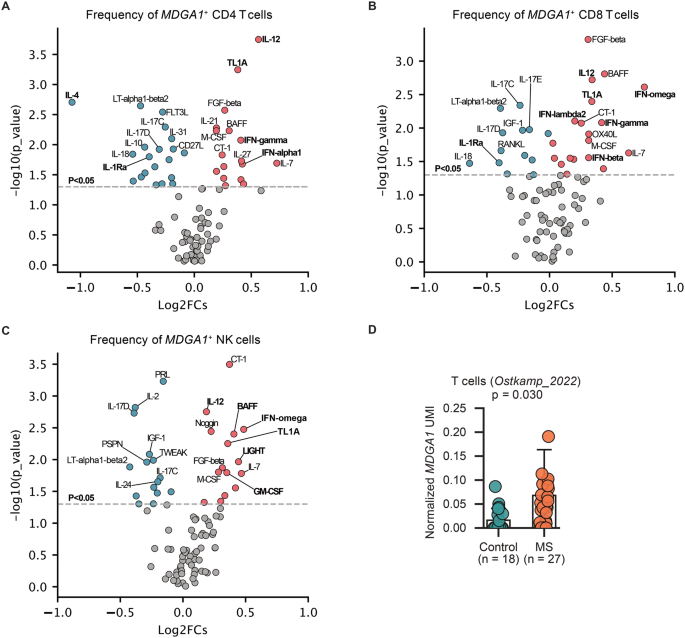
结果解读:MDGA1在急性移植物抗宿主病患者移植后30天、100天的T细胞和自然杀伤细胞中表达显著上调(n=10,P<0.05);公共数据集验证显示IL-12、干扰素等促炎细胞因子可显著诱导MDGA1表达,IL-4、IL-10等抗炎症因子可抑制其表达,且多发性硬化患者T细胞中MDGA1表达也显著升高,提示MDGA1是炎症状态下淋巴细胞的通用标志物。定量聚合酶链反应验证结果显示,4例急性移植物抗宿主病患者的T细胞MDGA1表达显著高于3例非患者(n=7,P<0.05)。对应MDGA1表达差异结果如下:
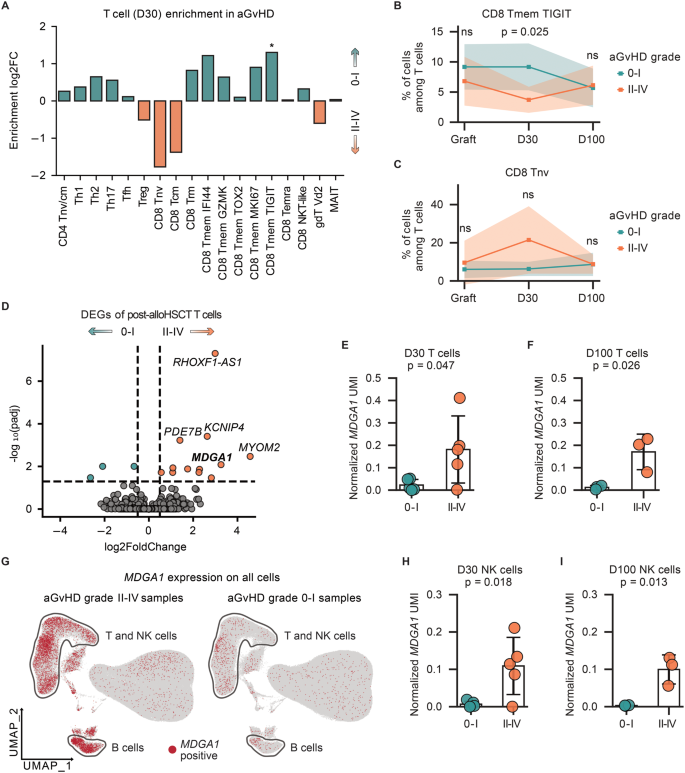
对应细胞因子调控验证结果如下:
产品关联:实验所用关键产品:Qiagen的RNeasy Mini Kit(货号74106)、Invitrogen的Qubit RNA BR Assay Kit(货号Q10210)、Takara的SMARTScribe逆转录酶(货号639536)、Thermo Fisher Scientific的PowerUp SYBR Green PCR Master Mix(货号A25742)。
3.7 移植物抗白血病相关标志物验证
实验目的:验证ADGRG1作为外周血移植物抗白血病相关标志物的可行性。
方法细节:分析ADGRG1在不同T细胞亚群中的表达特征,基于已发表的骨髓ADGRG1+细胞毒性T细胞的20个特征基因集,计算不同预后患者的ADGRG1特征打分;由于本研究复发患者样本量较小(n=2),结合公共异基因造血干细胞移植队列数据集验证其与复发的相关性。
结果解读:ADGRG1在CD8+αβ T细胞和γδ T细胞中特异性高表达,复发患者移植后100天外周血CD8+T细胞和γδ T细胞的ADGRG1特征打分显著低于持续缓解患者(P<0.05),且ADGRG1表达与急性移植物抗宿主病无显著相关性,提示其可特异性指示移植物抗白血病效应。对应ADGRG1表达特征结果如下:
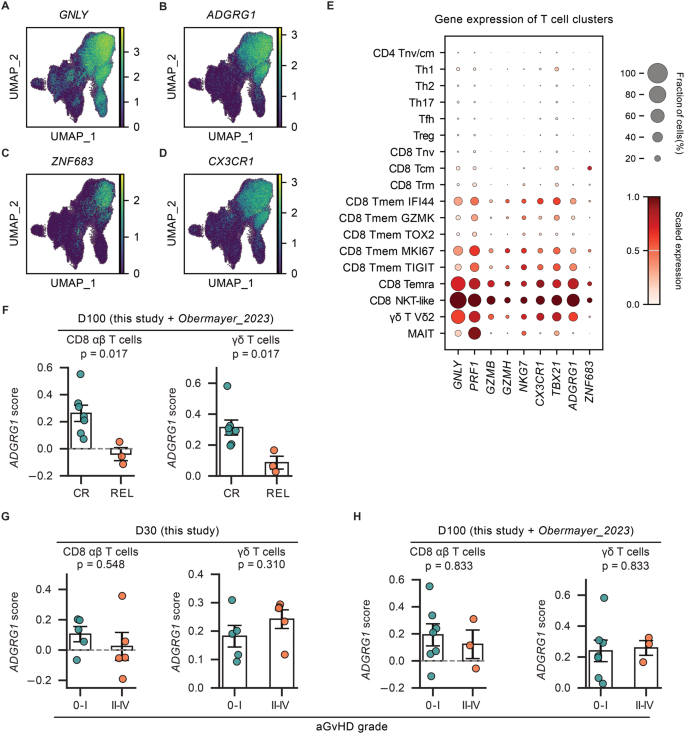
产品关联:文献未提及具体实验产品,领域常规使用基因集富集分析工具。
4. Biomarker 研究及发现成果
本研究共鉴定到两个功能互补的生物标志物,分别指示急性移植物抗宿主病和移植物抗白血病效应,筛选逻辑均采用“超大规模单细胞转录组无偏筛选→独立样本/公共队列验证→功能关联分析”的完整链条,结果具有较高的可靠性。
MDGA1属于细胞表面糖蛋白类生物标志物,筛选逻辑为:急性移植物抗宿主病患者与非患者T细胞差异基因筛选→移植后30天、100天两个时间点的表达一致性验证→公共数据集验证调控机制和疾病特异性→定量聚合酶链反应独立样本验证。该标志物的来源为外周血T细胞、自然杀伤细胞的转录本和细胞表面蛋白,验证方法包括单细胞转录组定量、定量聚合酶链反应表达验证、细胞因子刺激体外验证、独立炎症疾病队列验证。本研究中移植后30天T细胞MDGA1表达区分急性移植物抗宿主病的差异具有统计学意义(n=10,P<0.05),文献未提供受试者工作特征(ROC)曲线相关的特异性、敏感性数据。核心成果:MDGA1为糖基磷脂酰肌醇(GPI)锚定的细胞表面蛋白,可被促炎细胞因子诱导表达,不仅与异基因造血干细胞移植后急性移植物抗宿主病相关,还在多发性硬化患者T细胞中表达上调,提示其可作为全身炎症状态的通用标志物;创新性体现在首次在异基因造血干细胞移植领域发现其与急性移植物抗宿主病的关联,且细胞表面定位使其可通过流式细胞术快速检测,适合临床转化。推测:其他病原体感染诱导的炎症反应也可能诱导MDGA1表达,后续需排除感染等混杂因素进一步验证其对急性移植物抗宿主病的特异性。
ADGRG1(GPR56)属于细胞表面受体类生物标志物,筛选逻辑为:基于已发表的骨髓移植物抗白血病相关标志物→验证其在外周血免疫细胞中的表达特征→关联患者预后验证临床价值。该标志物的来源为外周血CD8+αβ T细胞、γδ T细胞的转录本和细胞表面蛋白,验证方法包括单细胞转录组亚群定位、特征基因集打分、复发患者与缓解患者的表达差异比较,同时结合公共移植队列数据集弥补本研究样本量不足的缺陷。本研究联合公共队列验证显示,移植后100天外周血T细胞ADGRG1特征打分区分复发患者的差异具有统计学意义(P<0.05),文献未提供受试者工作特征曲线相关数据。核心成果:ADGRG1是同种反应性细胞毒性T细胞的标志物,其表达水平与移植物抗白血病效应正相关,与急性移植物抗宿主病无显著相关性,可特异性指示移植后抗白血病效应;创新性体现在首次证实该标志物在外周血中同样具有预后价值,突破了既往仅能通过骨髓样本检测的限制,便于临床常规监测。
推测:可进一步开发ADGRG1的流式检测抗体,用于移植后患者的常规随访监测,早期识别移植物抗白血病效应不足的高复发风险患者。