1. 领域背景与文献
文献英文标题:Immune, blood-brain barrier, and metabolic biomarkers mediate gut-brain axis crosstalk in alzheimer’s disease;发表期刊:Biomarker Research;影响因子:未公开;研究领域:神经退行性疾病(阿尔茨海默病)的肠-脑轴生物标志物研究。
阿尔茨海默病是老年人群中最常见的进行性神经退行性疾病,其病理进程呈现连续发展特征,脑内β-淀粉样蛋白沉积、tau蛋白过度磷酸化形成神经原纤维缠结、神经炎症及脑萎缩等改变可早于临床症状15至20年出现。领域共识:当前阿尔茨海默病的发病机制尚未完全阐明,针对β-淀粉样蛋白的临床药物研发大多未达预期终点,缺乏有效的早期诊断标志物和干预靶点。近年来,肠道菌群作为肠-脑轴的核心调控组分,其与阿尔茨海默病的关联受到广泛关注,临床前研究已证实肠道菌群紊乱可通过代谢产物调控、外周免疫激活、血脑屏障通透性改变等途径影响中枢病理进展,但受限于人群研究的样本量限制、混杂因素干扰及伦理约束,目前仍缺乏人群层面的因果证据明确三者间的调控关系,免疫、血脑屏障、代谢通路的中介效应机制也未得到系统阐明。本研究针对这一领域空白,基于大样本全基因组关联研究汇总数据,通过孟德尔随机化方法解析肠道菌群与阿尔茨海默病的双向因果关联,明确循环生物标志物的中介效应,为阿尔茨海默病的菌群靶向干预提供人群层面的理论依据。
2. 文献综述解析
作者的文献综述按照“关联证据→机制研究→因果推断进展”的逻辑框架展开,系统梳理了肠-脑轴调控阿尔茨海默病的现有研究进展,并明确了现有研究的核心局限性。
首先,作者梳理了肠-脑轴与阿尔茨海默病的关联研究证据:临床队列研究显示阿尔茨海默病患者的肠道菌群结构与健康人群存在显著差异,产短链脂肪酸菌丰度降低、促炎菌丰度升高,且菌群紊乱与脑脊液病理标志物水平、认知功能下降显著相关;动物模型研究证实菌群移植可改善阿尔茨海默病模型小鼠的病理表型和认知功能,明确了菌群紊乱的致病作用。其次,作者总结了现有因果推断研究的进展:已发表的孟德尔随机化研究初步探索了肠道菌群、血液代谢物与阿尔茨海默病的因果关联,但研究仅覆盖少量代谢物,未系统纳入免疫、血脑屏障相关生物标志物,且未分析双向调控效应。最后,作者指出现有研究的核心局限性:人群研究多为观察性关联,无法排除混杂因素和反向因果干扰;动物模型与人类在饮食结构、遗传背景、菌群组成上存在固有差异,研究结果的转化价值有限;缺乏多维度生物标志物的整合分析,无法明确肠-脑轴串扰的具体中介通路。基于上述研究空白,本研究的创新价值体现在:首次整合肠道菌群分类与功能特征、免疫、血脑屏障、代谢四类暴露因素,结合大样本多维度阿尔茨海默病表型数据,通过双向孟德尔随机化、共定位分析系统阐明肠-脑轴的因果调控网络,弥补了现有研究中因果证据不足、中介机制不明确的缺陷,为阿尔茨海默病的早期干预提供了新的靶点方向。
3. 研究思路总结与详细解析
本研究的核心目标是明确免疫应答、血脑屏障完整性及代谢重编程在肠道菌群与阿尔茨海默病双向因果关联中的中介作用,核心科学问题为“肠道菌群如何通过外周通路调控阿尔茨海默病病理进展,阿尔茨海默病病理又如何反向影响肠道菌群稳态”,整体技术路线遵循“大样本全基因组关联研究数据整合→双向两样本孟德尔随机化分析→多方法交叉验证→贝叶斯模型平均优先级排序→中介效应量化→共定位验证→生物学功能注释”的闭环逻辑,有效降低了混杂因素和反向因果的干扰。
3.1 研究数据来源与分析框架构建
实验目的:搭建无混杂的因果推断分析体系,确保关联结果的稳健性。方法细节:整合多来源公共全基因组关联研究汇总数据,其中肠道菌群数据覆盖3个队列共32037名受试者,包含629项分类和功能特征;循环生物标志物数据覆盖1155项免疫相关性状、699项血脑屏障相关性状、249项代谢性状,样本量范围为3301至563964名;阿尔茨海默病表型数据包含迟发型阿尔茨海默病(63926名受试者)、阿尔茨海默病代理表型(基于父母病史定义的遗传风险表型,472868名受试者)、脑脊液β-淀粉样蛋白42和磷酸化tau蛋白水平(13116名受试者)三类。分析阶段采用6种孟德尔随机化方法交叉验证,包括逆方差加权、MR-Egger回归、加权中位数、加权模型、多效性残差和异常值检验、约束最大似然模型平均法,其中约束最大似然模型平均法为主要分析方法;关联显著性需满足4项标准:所有方法的效应方向一致、至少半数方法的P值<0.05(包含主要分析)、无显著多效性或异质性、通过Steiger方向性检验。文献未提及具体实验产品,领域常规使用全基因组关联研究生物信息学分析工具包、孟德尔随机化分析R语言程序包开展相关研究。结果解读:该分析框架通过多方法交叉验证、非重叠大样本队列整合,有效降低了假阳性和混杂偏倚,为后续因果关联的识别奠定了方法学基础。研究设计的整体流程见图1:
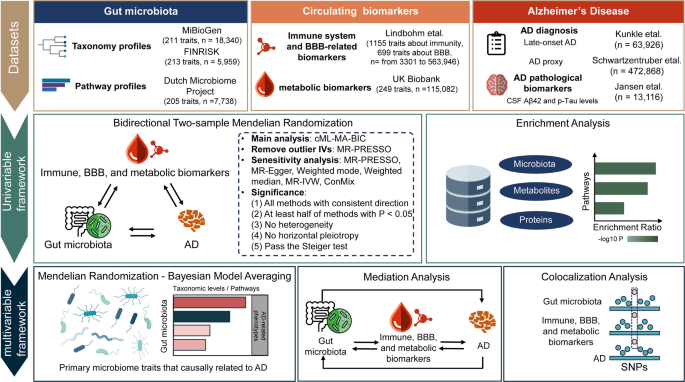
3.2 阿尔茨海默病相关肠道菌群与循环生物标志物的因果关联筛选
实验目的:识别与阿尔茨海默病发生发展存在因果关联的肠道菌群特征和循环生物标志物。方法细节:以肠道菌群、循环生物标志物为暴露因素,阿尔茨海默病相关表型为结局开展单变量孟德尔随机化分析,关联显著的生物标志物进一步通过功能富集分析注释其参与的生物学通路。结果解读:共识别到84种细菌物种、100种高阶分类单元(属到门水平)、52条代谢通路与至少1种阿尔茨海默病表型显著相关,其中δ-变形菌纲-脱硫弧菌目-脱硫弧菌科谱系与迟发型阿尔茨海默病、阿尔茨海默病代理表型均呈正相关,产短链脂肪酸的黏液降解菌(如嗜黏蛋白阿克曼菌、双歧杆菌属)为阿尔茨海默病保护类群;共识别59项循环生物标志物与阿尔茨海默病表型相关,其中程序性死亡受体1/程序性死亡配体1通路相关蛋白为保护因素,β-淀粉样蛋白相关蛋白、低密度脂蛋白胆固醇等为风险因素。功能富集分析显示,保护类代谢物富集于丙氨酸-天冬氨酸-谷氨酸代谢、乙醛酸和二羧酸代谢、三羧酸循环等通路,风险类代谢物富集于支链氨基酸降解通路。肠道菌群、循环生物标志物与阿尔茨海默病的因果关联结果见图2:
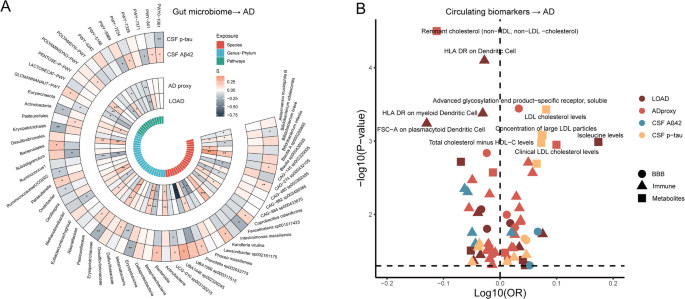
3.3 关键菌群特征的优先级排序与中介效应分析
实验目的:排除菌群间共线性干扰,识别驱动阿尔茨海默病发生的核心菌群特征,并量化循环生物标志物的中介效应占比。方法细节:采用孟德尔随机化-贝叶斯模型平均方法对关联显著的菌群特征进行优先级排序,评估每个菌群特征的边际纳入概率和后验概率;通过两步孟德尔随机化框架开展中介效应分析,采用乘积法计算间接效应,通过delta法计算标准误和置信区间,最终量化中介效应占总效应的比例。结果解读:优先级排序分析显示,脱硫弧菌科、甲烷短杆菌属为阿尔茨海默病的核心驱动菌群,其中脱硫弧菌科与阿尔茨海默病代理表型正相关(边际纳入概率=0.34~0.37,校正P<0.05),甲烷短杆菌属与脑脊液β-淀粉样蛋白42水平负相关(后验概率=0.4,边际纳入概率=0.64,校正P<0.01);UDP-葡萄糖衍生O抗原合成超通路为保护性功能通路(后验概率=0.2,边际纳入概率=0.95,校正P=0.01),N-乙酰葡糖胺等降解通路为风险性功能通路(后验概率=0.4,边际纳入概率=0.88,校正P<0.05)。中介效应分析显示,CD28阴性CD8阳性T细胞比例介导了脱硫弧菌科对阿尔茨海默病代理表型22.0%~28.2%的效应,免疫球蛋白D阳性CD24阳性B细胞表面CD19分子介导了UDP-葡萄糖衍生O抗原合成超通路对迟发型阿尔茨海默病25.2%的保护效应,整体循环生物标志物的中介效应占比约为25%。核心菌群的优先级排序与中介效应结果见图3:
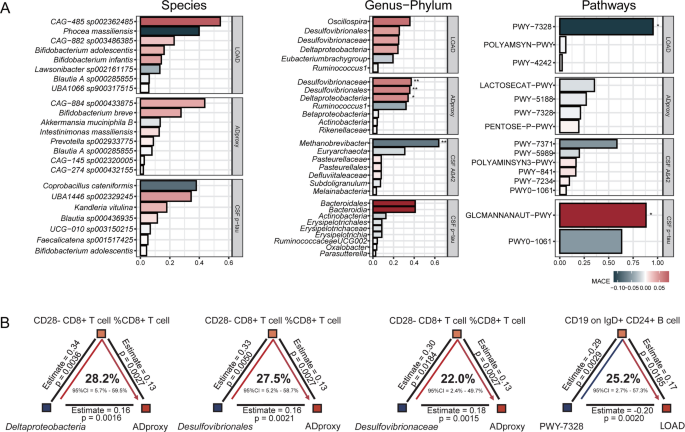
3.4 阿尔茨海默病对肠道菌群和循环生物标志物的反向调控效应分析
实验目的:明确阿尔茨海默病病理对肠道菌群稳态的反向调控作用,验证肠-脑轴的双向串扰特征。方法细节:以阿尔茨海默病相关表型为暴露因素,肠道菌群、循环生物标志物为结局开展单变量孟德尔随机化分析,关联显著的特征进一步通过功能富集分析注释反向调控的生物学通路。结果解读:共识别19项肠道菌群特征、323项循环生物标志物受阿尔茨海默病病理调控,其中丹毒丝菌科丰度随阿尔茨海默病病理进展升高,产短链脂肪酸的球杆状粪杆菌等菌群丰度降低;阿尔茨海默病病理可上调循环低密度脂蛋白、总脂肪酸水平,下调支链氨基酸、乳酸水平。功能富集分析显示,阿尔茨海默病调控的蛋白富集于免疫球蛋白A生成的肠道免疫网络通路,代谢物富集于脂肪酸生物合成通路。阿尔茨海默病对肠道菌群和循环生物标志物的反向调控结果见图4:
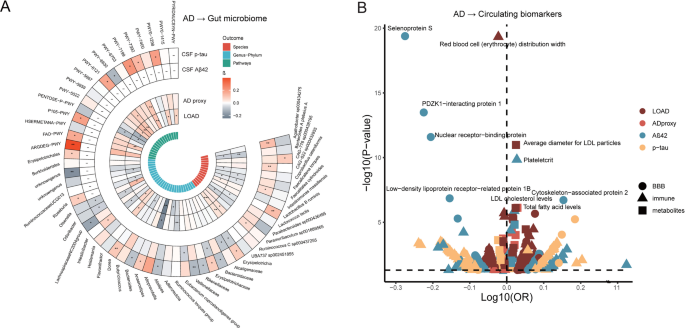
3.5 反向调控通路的中介效应与共定位验证
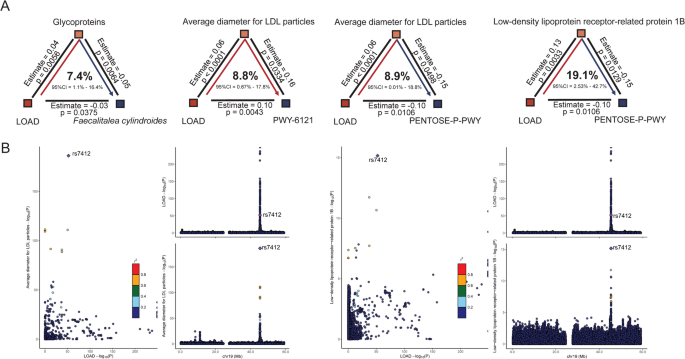
实验目的:验证阿尔茨海默病反向调控肠道菌群的中介通路,确认因果关联的遗传共定位证据。方法细节:针对阿尔茨海默病显著调控的5项核心菌群特征开展中介效应分析,通过共定位分析验证暴露与结局是否共享同一遗传变异,计算共定位后验概率。结果解读:糖蛋白、低密度脂蛋白相关性状介导了阿尔茨海默病对核心菌群0.05~0.20的调控效应,其中糖蛋白介导了阿尔茨海默病对球杆状粪杆菌7.4%的效应,低密度脂蛋白颗粒直径介导了对5-氨基咪唑核糖核苷酸生物合成通路8.8%的效应,低密度脂蛋白受体相关蛋白1B介导了对磷酸戊糖通路19.1%的效应。共定位分析显示,迟发型阿尔茨海默病与低密度脂蛋白颗粒平均直径共享遗传位点rs7412(共定位后验概率=1.0),该位点解释了100%的后验贡献,进一步验证了低密度脂蛋白代谢在肠-脑轴串扰中的核心作用。反向调控的中介效应与共定位结果见图5:
3.6 肠-脑轴双向反馈回路的机制解析
实验目的:阐明肠道菌群与阿尔茨海默病病理间的自我增强反馈回路机制。方法细节:整合双向孟德尔随机化的关联结果,结合领域已发表的机制研究,构建反馈回路的分子机制模型。结果解读:研究识别到8种菌群、3项免疫生物标志物与阿尔茨海默病存在双向因果关联,其中丹毒丝菌科丰度与脑脊液磷酸化tau蛋白水平负相关(β=-0.25,P=0.0087),而脑脊液β-淀粉样蛋白42水平降低可正向调控丹毒丝菌科丰度(β=0.07,P=0.0198),形成“阿尔茨海默病病理加重→菌群紊乱→进一步加速阿尔茨海默病进展”的自我增强回路;共定位分析显示脑脊液β-淀粉样蛋白42与磷酸化tau蛋白在位点rs71352238存在共定位(共定位后验概率=1.0),该位点为线粒体外膜转位酶40基因的剪接数量性状位点,与阿尔茨海默病病理直接相关。肠-脑轴双向反馈回路的机制模型见图6:

4. Biomarker 研究及发现成果
本研究涉及的生物标志物涵盖肠道菌群标志物、循环免疫/血脑屏障/代谢标志物三类,通过“大样本全基因组关联研究筛选→多方法孟德尔随机化因果验证→中介效应量化→共定位遗传确认”的完整逻辑链,明确了各标志物在肠-脑轴串扰中的调控作用。
从生物标志物类型来看,可分为三大类:第一类为肠道菌群标志物,包括保护类菌群(产短链脂肪酸的黏液降解菌如嗜黏蛋白阿克曼菌、双歧杆菌属、甲烷短杆菌属,保护性功能通路为UDP-葡萄糖衍生O抗原合成超通路)、风险类菌群(脱硫弧菌科、丹毒丝菌科,风险性功能通路为N-乙酰葡糖胺降解超通路);第二类为免疫类生物标志物,包括CD28阴性CD8阳性T细胞比例、免疫球蛋白D阳性CD24阳性B细胞表面CD19分子、程序性死亡受体1/程序性死亡配体1通路相关蛋白;第三类为代谢与血脑屏障类生物标志物,包括低密度脂蛋白胆固醇、糖蛋白乙酰基、支链氨基酸、短链脂肪酸。上述生物标志物的筛选逻辑为:首先基于大样本全基因组关联研究识别与暴露因素显著相关的遗传工具变量,再通过多方法孟德尔随机化验证其与阿尔茨海默病表型的因果关联,随后通过中介效应分析确认其在肠-脑轴中的调控作用,最终通过共定位分析验证暴露与结局的遗传共享性,形成完整的证据链条。
所有生物标志物的关联均基于大样本欧洲人群全基因组关联研究汇总数据,验证过程包含多方法交叉验证、多效性与异质性检验、Steiger方向性检验、共定位分析多重质控步骤。核心验证数据包括:脱硫弧菌科与阿尔茨海默病代理表型的正相关具有统计学显著性(校正P<0.05);甲烷短杆菌属与脑脊液β-淀粉样蛋白42水平的负相关具有统计学显著性(校正P<0.01);CD28阴性CD8阳性T细胞对脱硫弧菌科-阿尔茨海默病关联的中介效应占比为22.0%~28.2%(P<0.05);遗传位点rs7412的共定位后验概率为1.0,确认迟发型阿尔茨海默病与低密度脂蛋白代谢存在因果共享。
本研究的生物标志物相关核心成果包括三点:第一,首次在人群层面明确了肠道菌群与阿尔茨海默病的双向因果关联,揭示了“菌群紊乱→免疫/代谢/血脑屏障异常→阿尔茨海默病病理进展→进一步加重菌群紊乱”的自我增强反馈回路,其中短链脂肪酸耗竭是回路中的核心驱动环节;第二,识别到脱硫弧菌科、甲烷短杆菌属为阿尔茨海默病的核心菌群标志物,CD28阴性CD8阳性T细胞、低密度脂蛋白为关键中介标志物,可为阿尔茨海默病的早期诊断和菌群靶向干预提供潜在靶点;第三,验证了载脂蛋白E基因位点rs7412、线粒体外膜转位酶40基因位点rs71352238为肠-脑轴串扰的核心遗传位点,为阿尔茨海默病的遗传机制解析提供了新的视角。所有关联结果均经过严格的统计学检验,P值均<0.05,共定位后验概率≥0.95,结果稳健性良好。