1. 领域背景与文献
文献英文标题:Circular RNAs and enhancer RNAs in neurodegenerative disorders: regulatory roles and clinical potential;发表期刊:Journal of Neuroinflammation;影响因子:5.8(2024);研究领域:神经退行性疾病、非编码RNA调控
神经退行性疾病是一类以中枢或外周神经元进行性丢失、功能障碍为核心特征的难治性疾病,涵盖阿尔茨海默病(AD)、帕金森病(PD)、亨廷顿病(HD)、多发性硬化(MS)等多种类型,其发病率随人口老龄化持续上升,已成为全球公共卫生的重大挑战。目前临床缺乏有效的早期诊断生物标志物,且现有治疗手段仅能缓解症状,无法逆转疾病进程。非编码RNA(ncRNA)作为基因调控网络的关键参与者,在神经系统发育、突触可塑性维持及神经元功能稳态中发挥核心作用。其中,环状RNA(circRNA)因独特的共价闭环结构具有极强的稳定性,不易被核酸酶降解,可在体液中稳定存在;增强子RNA(eRNA)由基因组活性增强子区域双向转录生成,直接参与基因转录调控及染色质构象重塑,二者均为近年神经科学领域的研究热点。然而,此前多数研究仅聚焦于单一类型ncRNA或单一疾病,对环状RNA与增强子RNA在不同神经退行性疾病中的协同调控机制及临床转化潜力的系统性整合分析较为匮乏。该文献旨在填补这一空白,通过系统梳理两类ncRNA在四大神经退行性疾病中的调控作用,构建跨疾病的ncRNA调控网络模型,为疾病的早期诊断和靶向治疗提供新的理论依据与潜在靶点。
2. 文献综述解析
该文献采用按疾病类型(AD、PD、HD、MS)与ncRNA功能类型(转录调控、转录后调控)的双重分类维度,系统整合了近年环状RNA与增强子RNA在神经退行性疾病中的研究成果,重点分析了两类ncRNA在疾病病理过程中的调控机制、临床应用潜力及研究挑战。
现有研究已证实环状RNA主要通过微小RNA(miRNA)海绵作用、蛋白支架功能、转录调控及非经典翻译等多种方式参与神经退行性疾病的病理过程,例如在AD中环状RNA可调控Aβ生成与清除通路,在PD中参与多巴胺能神经元存活及α-突触核蛋白聚集的调控;增强子RNA则主要通过调控增强子-启动子相互作用、转录因子招募及染色质可及性,影响疾病相关基因的转录活性,如AD中增强子RNA调控APOE基因表达,PD中参与SNCA基因的转录延伸调控。现有研究的优势在于揭示了大量疾病相关的差异表达ncRNA及其初步功能,为后续研究奠定了基础;但同时存在局限性,如多数研究集中于环状RNA,增强子RNA的研究深度与广度相对不足,且多数研究仅在细胞或动物模型中验证,缺乏大规模临床队列的独立验证,部分研究未明确ncRNA异常表达与疾病发生的因果关系,仅为相关性分析。
该文献的创新点在于首次系统整合了环状RNA与增强子RNA在四大神经退行性疾病中的调控网络,揭示了跨疾病的共同调控模式,即两类ncRNA均聚焦于突触可塑性维持、神经炎症激活、蛋白稳态调控三大核心通路,且在转录与转录后水平形成协同调控机制;同时,文献首次强调了两类ncRNA之间的潜在交互作用,为神经退行性疾病的多靶点治疗提供了新的思路。此外,文献还系统梳理了两类ncRNA作为疾病生物标志物的临床潜力,为非侵入性诊断工具的开发提供了全面的候选靶点列表,弥补了此前研究缺乏系统性整合的不足。
3. 研究思路总结与详细解析
该文献的整体研究思路为:首先阐述环状RNA与增强子RNA的基础生物学特征,明确其生物发生过程与核心功能;随后分别针对AD、PD、HD、MS四大神经退行性疾病,系统梳理两类ncRNA在疾病病理过程中的具体调控机制;接着分析跨疾病的共同调控模式及两类ncRNA的转录-转录后调控界面;最后讨论当前研究的挑战与未来方向,形成“基础特征-疾病机制-跨疾病整合-未来展望”的完整逻辑闭环。研究目标是揭示环状RNA与增强子RNA在神经退行性疾病中的调控网络,为疾病诊断与治疗提供新靶点;核心科学问题是两类ncRNA如何协同调控神经退行性疾病的核心病理通路,以及其作为生物标志物与治疗靶点的可行性。
3.1 环状RNA与增强子RNA的基础生物学特征解析
实验目的:明确环状RNA与增强子RNA的生物发生机制、结构特征及核心生物学功能,为后续疾病层面的机制分析奠定理论基础。
方法细节:通过系统性综述已发表的基础研究文献,梳理环状RNA的反向剪接生成过程(包括顺式作用元件与反式作用因子的调控)、环状结构赋予的高稳定性特征,以及增强子RNA的双向转录生成机制、与增强子活性的紧密关联。
结果解读:环状RNA由前体mRNA通过反向剪接形成共价闭环结构,无5"帽与3"多聚腺苷酸尾,不易被RNase R降解,其功能包括作为miRNA海绵竞争性结合miRNA、作为蛋白支架招募蛋白质复合物、调控亲本基因的转录、以及少数含内部核糖体进入位点(IRES)的环状RNA可进行非经典翻译生成多肽;增强子RNA由基因组中活性增强子区域双向转录生成,通常长度较短、稳定性较低,其核心功能包括促进增强子-启动子的染色质环化、招募转录共激活因子(如p300/CBP)、调控染色质可及性、以及释放停滞的RNA聚合酶II以促进基因转录延伸。
产品关联:文献未提及具体实验产品,领域常规使用RNA测序(RNA-seq)、RNase R酶切实验验证环状RNA稳定性、荧光原位杂交(FISH)定位ncRNA亚细胞分布、RNA免疫沉淀(RIP)检测ncRNA-蛋白相互作用等试剂/仪器。
3.2 环状RNA与增强子RNA在阿尔茨海默病中的调控机制解析
实验目的:揭示环状RNA与增强子RNA在AD核心病理过程(Aβ沉积、tau蛋白过度磷酸化、神经炎症激活、突触功能障碍)中的具体调控作用及分子机制。
方法细节:整合多个已发表研究的疾病样本RNA-seq数据、细胞模型(如Aβ处理的SK-N-SH细胞、原代神经元)、动物模型(如APP/PS1转基因小鼠)的功能实验结果,分析差异表达的环状RNA与增强子RNA及其靶基因与信号通路。
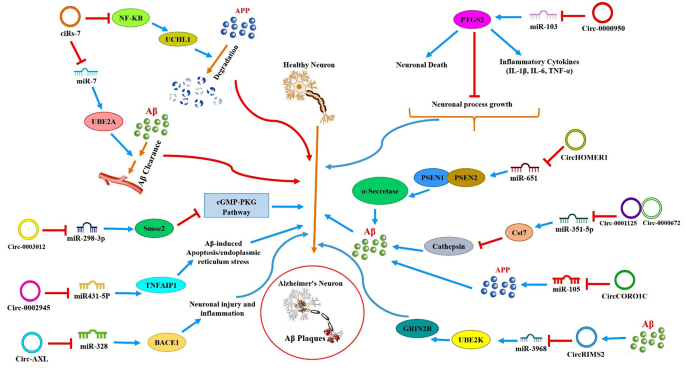
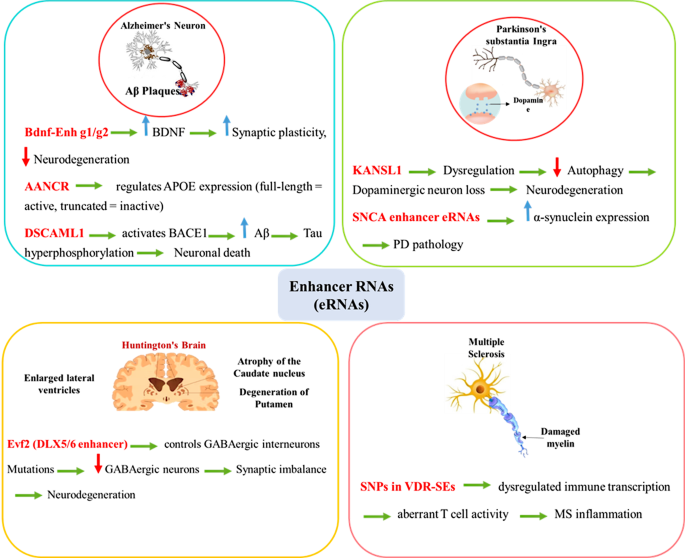
结果解读:在AD中,ciRS-7(CDR1as)在健康人脑内高表达,在AD脑内表达下调,其通过作为miRNA海绵结合miR-7,解除miR-7对泛素结合酶UBE2A的抑制,促进Aβ的泛素化降解,从而减少Aβ沉积;circCwc27通过直接结合RNA结合蛋白Pur-α,抑制Pur-α与AD相关基因(如APP)启动子的结合,减少APP表达及Aβ生成;增强子RNA AANCR由APOE基因的增强子区域转录生成,其全长转录本可促进APOE基因的表达,而部分转录本则失去调控功能,AANCR的序列变异可影响APOE表达水平,进而调控神经炎症反应;此外,多个环状RNA(如circRIMS2、circGigyf2)的异常表达与AD的突触功能障碍及认知障碍密切相关。

产品关联:文献未提及具体实验产品,领域常规使用APP/PS1、5xFAD等AD转基因动物模型、ELISA试剂盒检测脑脊液与血浆中Aβ水平、免疫组化(IHC)检测脑内tau蛋白磷酸化水平、Morris水迷宫实验评估动物认知功能等试剂/仪器。
3.3 环状RNA与增强子RNA在帕金森病中的调控机制解析
实验目的:明确环状RNA与增强子RNA在PD核心病理过程(多巴胺能神经元进行性丢失、α-突触核蛋白异常聚集、线粒体功能障碍、神经炎症)中的调控作用及分子机制。
方法细节:整合已发表研究的PD患者脑区RNA-seq数据、细胞模型(如MPP+处理的SH-SY5Y细胞)、动物模型(如MPTP诱导的PD小鼠模型)的功能实验结果,分析差异表达ncRNA的靶基因及信号通路。
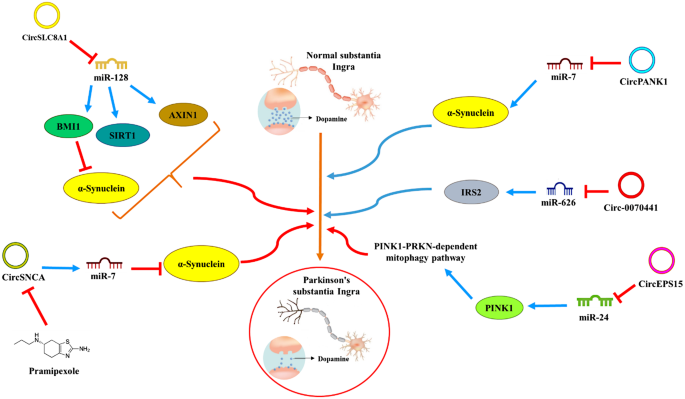
结果解读:circSLC8A1在PD患者黑质中表达上调,其通过作为miRNA海绵结合miR-128,解除miR-128对SIRT1、BMI1、AXIN1等靶基因的抑制,其中SIRT1具有抗炎与神经保护作用,BMI1可负调控α-突触核蛋白表达,AXIN1参与Wnt/β-catenin通路调控多巴胺能神经元存活;circSNCA与circPANK1均通过结合miR-7,上调α-突触核蛋白(SNCA)的表达,促进α-突触核蛋白的异常聚集,加重多巴胺能神经元损伤;增强子RNA由SNCA基因的内含子增强子区域转录生成,可通过解离负延伸因子(NELF)复合物,释放停滞的RNA聚合酶II,促进SNCA基因的转录延伸,从而增加SNCA蛋白的表达;此外,circEps15在PD患者血浆中表达下调,其通过结合miR-24维持PINK1基因的表达,促进PINK1-PRKN依赖的线粒体自噬通路,维持线粒体稳态,与PD的疾病进展密切相关。
产品关联:文献未提及具体实验产品,领域常规使用MPTP/MPP+诱导的PD动物/细胞模型、Western blot检测α-突触核蛋白表达水平、流式细胞术检测线粒体膜电位、高效液相色谱(HPLC)检测脑内多巴胺含量等试剂/仪器。
3.4 环状RNA与增强子RNA在亨廷顿病中的调控机制解析
实验目的:探索环状RNA与增强子RNA在HD核心病理过程(突变亨廷顿蛋白(mHTT)异常聚集、自噬功能障碍、GABA能神经元丢失、神经环路失衡)中的调控作用及分子机制。
方法细节:整合已发表研究的HD患者脑区RNA-seq数据、细胞模型(如携带mHTT的神经前体细胞)、动物模型(如HD转基因小鼠)的功能实验结果,分析差异表达ncRNA的靶基因及信号通路。
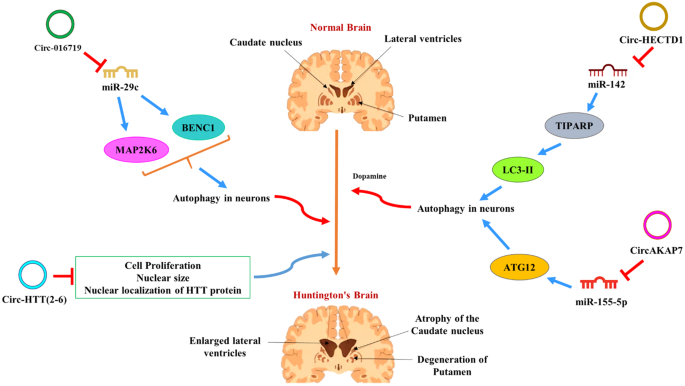
结果解读:circLRP1B、circDLGAP4、circHIPK2等环状RNA可分别通过海绵miR-27a-3p、miR-134-5p、miR-124,上调自噬相关基因的表达,促进mHTT的自噬降解;circHTT(2-6)由HTT基因的外显子2-6反向剪接生成,在HD患者脑内表达上调,其过表达可导致细胞增殖能力降低、细胞核形态异常及HTT蛋白核定位异常,模拟HD的细胞病理特征;增强子RNA Evf2由Dlx5/6基因的增强子区域转录生成,可调控GABA能中间神经元的发育与功能,Evf2功能异常可导致海马与齿状回GABA能神经元数量减少,突触抑制功能减弱,加重HD的神经环路失衡;此外,环状RNA表达水平与HTT基因的CAG重复长度呈负相关,提示环状RNA可作为HD疾病遗传负担的分子标志物。
产品关联:文献未提及具体实验产品,领域常规使用携带mHTT的细胞模型与转基因动物模型、Western blot检测mHTT表达水平、免疫荧光检测自噬小体(LC3)、电生理实验检测突触功能等试剂/仪器。
3.5 环状RNA与增强子RNA在多发性硬化中的调控机制解析
实验目的:分析环状RNA与增强子RNA在MS核心病理过程(血脑屏障破坏、神经炎症激活、脱髓鞘、轴索损伤)中的调控作用及分子机制。
方法细节:整合已发表研究的MS患者外周血、脑脊液RNA-seq数据、实验性自身免疫性脑脊髓炎(EAE)动物模型的功能实验结果,分析差异表达ncRNA的靶基因及信号通路。
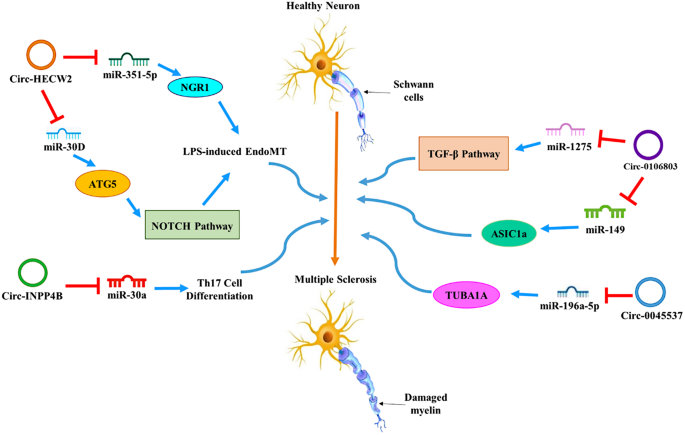
结果解读:hsa_circ_0106803在复发缓解型MS(RRMS)患者外周血中表达上调2.8倍,其通过作为miRNA海绵结合miR-149,解除miR-149对酸敏感离子通道ASIC1a的抑制,促进ASIC1a表达,加重神经炎症反应;circINPP4B在EAE小鼠中表达上调,其通过结合miR-30a,抑制miR-30a对Th17细胞分化的负调控作用,促进Th17细胞分化,加重自身免疫性炎症;circ_HECW2通过结合miR-30D与miR-30e-5p,分别上调ATG5与NGR1的表达,诱导内皮细胞-间充质转化(EndoMT),破坏血脑屏障完整性;此外,MS风险单核苷酸多态性(SNPs)富集于维生素D受体(VDR)结合的超级增强子区域,提示增强子RNA可通过调控免疫细胞的基因转录活性,参与MS的遗传易感性调控。
产品关联:文献未提及具体实验产品,领域常规使用EAE动物模型、流式细胞术检测外周血免疫细胞亚群、免疫荧光检测血脑屏障完整性、髓鞘染色(LFB)检测脱髓鞘程度等试剂/仪器。
3.6 跨疾病调控模式与转录-转录后调控界面分析
实验目的:揭示环状RNA与增强子RNA在不同神经退行性疾病中的共同调控规律及两类ncRNA之间的交互作用机制。
方法细节:通过生物信息学分析整合四大疾病的ncRNA调控网络数据,挖掘共同的靶通路与调控模式,结合已发表的交互作用研究结果,分析两类ncRNA的协同调控机制。
结果解读:跨疾病的共同调控通路包括突触可塑性维持、神经炎症激活、蛋白稳态调控三大核心模块,环状RNA与增强子RNA分别在转录后与转录水平协同调控这些通路,例如在AD中增强子RNA AANCR调控APOE基因的转录,而circCORO1C则调控APP基因的转录后加工,二者共同影响Aβ生成与神经炎症;在PD中增强子RNA参与SNCA基因的转录调控,circSNCA则调控SNCA的转录后表达,协同促进α-突触核蛋白聚集;此外,初步研究提示增强子RNA可通过调控RNA结合蛋白的表达影响环状RNA的生物发生,而环状RNA也可通过结合染色质重塑蛋白影响增强子RNA的转录,形成双向调控的交互网络。
产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析工具(如STRING、Cytoscape、WGCNA)构建ncRNA调控网络、染色体构象捕获(Hi-C)检测增强子-启动子相互作用等试剂/仪器。
4. Biomarker研究及发现成果解析
该文献系统梳理了环状RNA与增强子RNA作为神经退行性疾病生物标志物的研究成果,明确了两类ncRNA的Biomarker类型、筛选验证逻辑及临床应用潜力,其中环状RNA因高稳定性更适合作为循环Biomarker,增强子RNA因组织特异性更适合作为组织Biomarker。
Biomarker定位
文献中涉及的Biomarker主要为循环环状RNA、脑区特异性环状RNA及增强子区域增强子RNA,类型包括诊断Biomarker、预后Biomarker、疾病负担Biomarker;筛选/验证逻辑为:首先基于疾病患者与健康对照的组织/体液样本进行RNA-seq筛选差异表达ncRNA→通过细胞/动物模型验证ncRNA的功能及与疾病病理的关联→在独立临床队列中验证ncRNA的诊断/预后价值。
研究过程详述
- AD:脑脊液样本的RNA-seq分析显示,112种环状RNA表达上调、51种表达下调,其中circ-LPAR1、circ-AXL等上调,circ-PCCA、circ-HAUS4等下调;ciRS-7在AD脑内表达下调,与Aβ沉积及认知障碍程度相关;增强子RNA AANCR的序列变异可影响APOE表达水平,与AD的发病风险相关;部分环状RNA的临床验证显示其可区分AD患者与健康对照,但文献未明确具体的ROC曲线AUC、敏感性与特异性数据。
- PD:一项纳入300例PD患者与100例健康对照的研究显示,血浆中circARID1B、circTCONS_l2_00002816等环状RNA可用于PD的早期诊断,ROC曲线分析显示具有较高的敏感性与特异性;circFAM83H、circHUWE1等可区分早期与晚期PD;circEps15在PD患者血浆中表达下调,其表达水平与疾病进展及运动症状严重程度相关。
- HD:circHTT(2-6)在HD患者脑内表达上调,与细胞病理异常相关;环状RNA表达水平与HTT基因的CAG重复长度呈负相关(文献未明确相关系数及P值),可作为HD疾病遗传负担的分子标志物;
- MS:hsa_circ_0106803在RRMS患者外周血中表达上调2.8倍(n=未明确,P值未明确),与ASIC1a表达及疾病活动度相关;circPGAP3在MS患者中表达下调,经两个独立临床队列验证,可作为MS的潜在诊断Biomarker;6种性别依赖的环状RNA(如hsa_circ_0141241、circPADI4)在女性MS患者中显著上调,可作为性别特异性Biomarker;MS风险SNPs富集于VDR相关超级增强子区域,提示增强子RNA可作为MS遗传易感性的潜在Biomarker,但尚未在临床样本中验证。
核心成果提炼
这些ncRNA Biomarker不仅可用于疾病的早期诊断与预后评估,部分还具有潜在的治疗价值,例如上调AD中ciRS-7的表达可促进Aβ清除,下调PD中circSLC8A1的表达可减轻多巴胺能神经元损伤;该研究的创新性在于首次系统整合了两类ncRNA在四大神经退行性疾病中的Biomarker潜力,揭示了跨疾病的ncRNA Biomarker特征,即多数Biomarker均聚焦于突触功能、神经炎症、蛋白稳态三大核心通路;统计学结果方面,部分研究显示ncRNA表达与疾病严重程度显著相关,例如circGigyf2在AD患者脑内的表达与痴呆严重程度负相关(文献未明确P值),circEps15在PD患者血浆中的表达与疾病进展相关(n=未明确,P值未明确);临床队列样本量从数十例到数百例不等,部分Biomarker经多队列验证,具有较好的重复性。此外,环状RNA作为循环Biomarker具有高稳定性、非侵入性的优势,增强子RNA作为组织Biomarker具有高特异性的优势;但目前多数Biomarker缺乏大规模多中心临床验证,部分Biomarker的疾病特异性不足,可能在其他疾病中也存在表达异常。