1. 领域背景与文献引入
文献英文标题:cGAS-STING pathway at the crossroads of neuroimmunology: Bridging innate immunity to aging and neurodegeneration;发表期刊:Journal of Neuroinflammation;影响因子:5.7(2024年);研究领域:神经免疫学、衰老与神经退行性疾病。
神经退行性疾病(如阿尔茨海默病、帕金森病)是全球老龄化进程中面临的重大公共健康挑战,其发病机制涉及遗传、环境、代谢及免疫等多因素复杂交互作用,目前仍缺乏有效的疾病修饰治疗手段。神经炎症作为神经退行性疾病的核心病理特征之一,其调控机制已成为领域研究热点。先天免疫通路在神经炎症中的作用逐渐受到关注,其中环鸟苷酸-腺苷酸合成酶-干扰素基因刺激蛋白(cGAS-STING)通路作为胞质DNA感应的核心通路,在感染免疫、自身免疫病中已被广泛研究,但在衰老及神经退行性疾病中的系统阐述仍较为缺乏。现有研究已初步揭示该通路异常激活与神经炎症、神经元损伤的关联,但不同神经退行性疾病中该通路的具体激活机制、细胞特异性作用及靶向治疗的转化潜力仍存在诸多空白。这篇综述系统梳理了cGAS-STING通路在衰老及多种神经退行性疾病中的作用机制,并总结了靶向该通路的抑制剂研究进展,为领域内后续研究及药物开发提供了全面参考。
2. 文献综述解析
这篇综述的核心评述逻辑以“通路基础-衰老调控-疾病特异性作用-靶向治疗”为分类维度,系统整合了cGAS-STING通路在衰老及神经退行性疾病领域的最新研究成果。
现有研究已证实cGAS-STING通路通过感应胞质DNA(包括线粒体DNA、核DNA、外源病毒DNA等)激活下游I型干扰素及炎症因子通路,在感染防御中发挥关键作用;在衰老领域,该通路的慢性激活与衰老相关分泌表型(SASP)、慢性炎症密切相关;在神经退行性疾病中,不同疾病(阿尔茨海默病、帕金森病、肌萎缩侧索硬化症等)中该通路的激活触发因素及下游效应存在差异,如阿尔茨海默病中主要由β-淀粉样蛋白诱导的线粒体DNA泄漏激活,帕金森病中与α-突触核蛋白诱导的DNA损伤相关。现有研究的优势在于明确了该通路在神经炎症中的核心地位,且部分预临床研究已验证了靶向抑制剂的治疗潜力;但局限性在于,不同细胞类型(小胶质细胞、星形胶质细胞、神经元)中该通路激活的特异性效应及相互调控机制仍不清晰,胞质DNA的具体来源及相对贡献尚未明确,且现有抑制剂大多处于临床前阶段,血脑屏障穿透性及长期安全性仍需验证。
这篇综述的创新价值在于,首次从通路组成、调控机制、疾病特异性作用、靶向治疗等多个层面进行了全面梳理,不仅总结了已知的激活机制,还深入探讨了该通路在不同疾病中的细胞特异性效应及潜在的治疗窗口,同时对现有抑制剂的分类、作用机制及临床转化挑战进行了详细分析。通过对比现有研究中“细胞类型特异性效应不明确”“临床转化数据缺乏”等未解决问题,凸显了本综述为领域提供系统研究框架、明确未来研究方向的学术必要性。
3. 研究思路总结与详细解析
这篇综述的研究目标是系统阐述cGAS-STING通路在衰老及神经退行性疾病中的作用机制,并总结靶向该通路的治疗策略;核心科学问题包括:cGAS-STING通路在衰老及不同神经退行性疾病中的激活机制是什么?该通路在不同细胞类型中的特异性效应及对神经元损伤的调控机制如何?靶向该通路的抑制剂有哪些类型,其临床转化潜力及挑战是什么?技术路线逻辑为:从通路基础组成与调控机制入手,依次阐述该通路在衰老及多种神经退行性疾病中的作用,最后总结靶向抑制剂的研究进展及临床转化挑战,形成“基础-疾病-治疗”的完整逻辑闭环。
3.1 cGAS-STING通路的组成与激活调控机制
实验目的:明确cGAS-STING通路的核心组成分子、结构特点及激活的上游触发因素与下游信号传导机制。
方法细节:通过系统检索PubMed、Web of Science等数据库中关于cGAS-STING通路的基础研究文献,梳理cGAS和STING的分子结构、亚细胞定位,以及上游DNA感应、下游I型干扰素及NF-κB通路激活的分子机制,同时总结该通路的调控机制(包括翻译后修饰、蛋白相分离、病毒逃逸等)。
结果解读:cGAS主要定位于细胞质、细胞核、线粒体及细胞膜,其N端正电荷区域负责结合双链DNA,C端催化结构域在结合DNA后构象变化,催化产生第二信使2"3"-cGAMP;STING定位于内质网,结合cGAMP后发生构象变化并向高尔基体转运,招募TANK结合激酶1(TBK1)及干扰素调节因子3(IRF3),激活下游I型干扰素及NF-κB通路,诱导炎症因子表达。该通路的激活受翻译后修饰(磷酸化、乙酰化、甲基化等)、蛋白液-液相分离(cGAS与DNA形成液滴促进激活)及病毒编码蛋白的负调控。
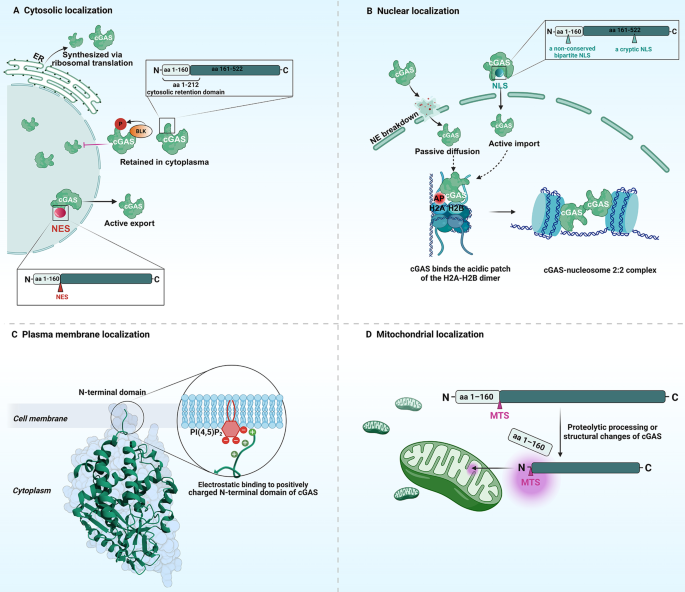
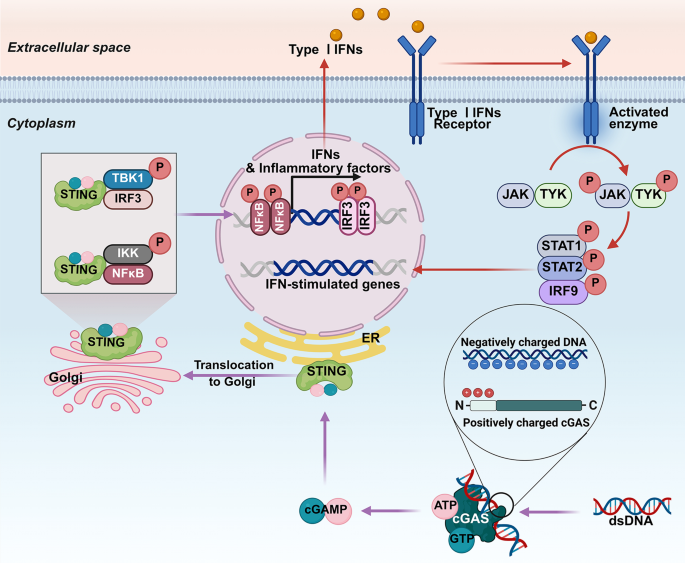
产品关联:文献未提及具体实验产品,领域常规使用免疫印迹、免疫荧光、实时荧光定量PCR、报告基因实验等试剂/仪器研究通路激活。
3.2 cGAS-STING通路在衰老中的作用机制
实验目的:揭示cGAS-STING通路在衰老过程中的激活机制及对衰老相关表型的调控作用。
方法细节:检索衰老相关的cGAS-STING通路研究文献,梳理衰老过程中胞质DNA积累的来源(线粒体DNA泄漏、核DNA损伤、DNA清除能力下降等),以及该通路激活对衰老相关炎症、细胞衰老、组织功能衰退的影响,同时总结靶向该通路改善衰老表型的预临床研究结果。
结果解读:衰老过程中,线粒体功能障碍、核膜完整性破坏及DNA修复能力下降导致胞质DNA(线粒体DNA、核DNA片段)积累,持续激活cGAS-STING通路,诱导慢性炎症(衰老相关炎症)及SASP,加速细胞衰老与组织功能衰退。在小鼠模型中,抑制cGAS或STING可减轻衰老相关炎症,改善认知功能及血管内皮功能。
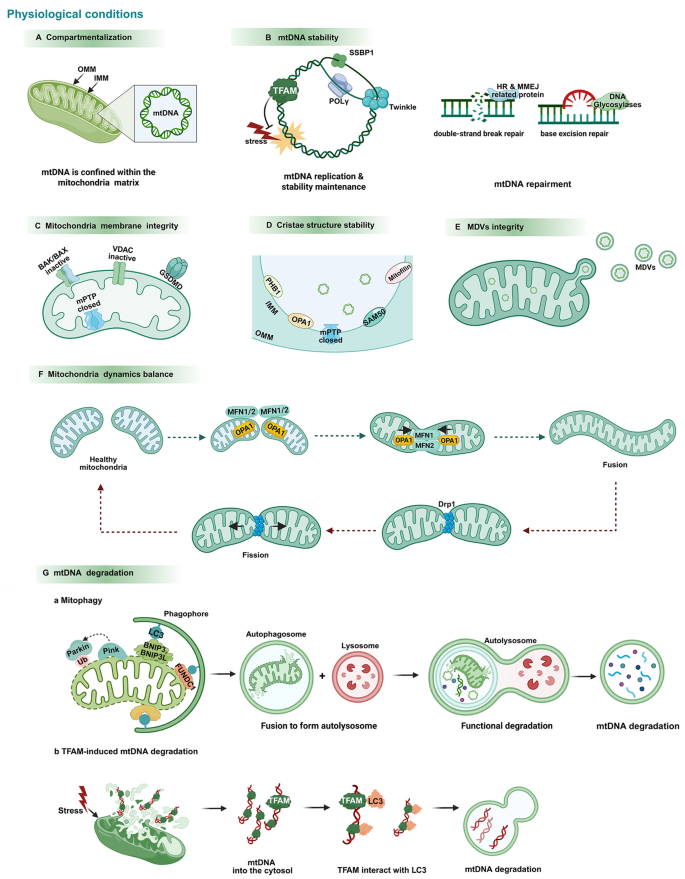
产品关联:文献未提及具体实验产品,领域常规使用衰老小鼠模型(如自然衰老小鼠、线粒体DNA突变小鼠)、细胞衰老模型(如复制性衰老细胞)等开展研究。
3.3 cGAS-STING通路在不同神经退行性疾病中的特异性作用
实验目的:分析cGAS-STING通路在阿尔茨海默病、帕金森病、肌萎缩侧索硬化症等神经退行性疾病中的激活触发因素、细胞特异性效应及对疾病进展的调控机制。
方法细节:针对每种神经退行性疾病,系统检索相关研究文献,梳理疾病病理因素(如β-淀粉样蛋白、α-突触核蛋白、TAR DNA结合蛋白43等)如何诱导胞质DNA积累,激活cGAS-STING通路,以及该通路在小胶质细胞、星形胶质细胞、神经元中的不同效应,同时总结基因敲除或药物抑制该通路对疾病表型的改善作用。
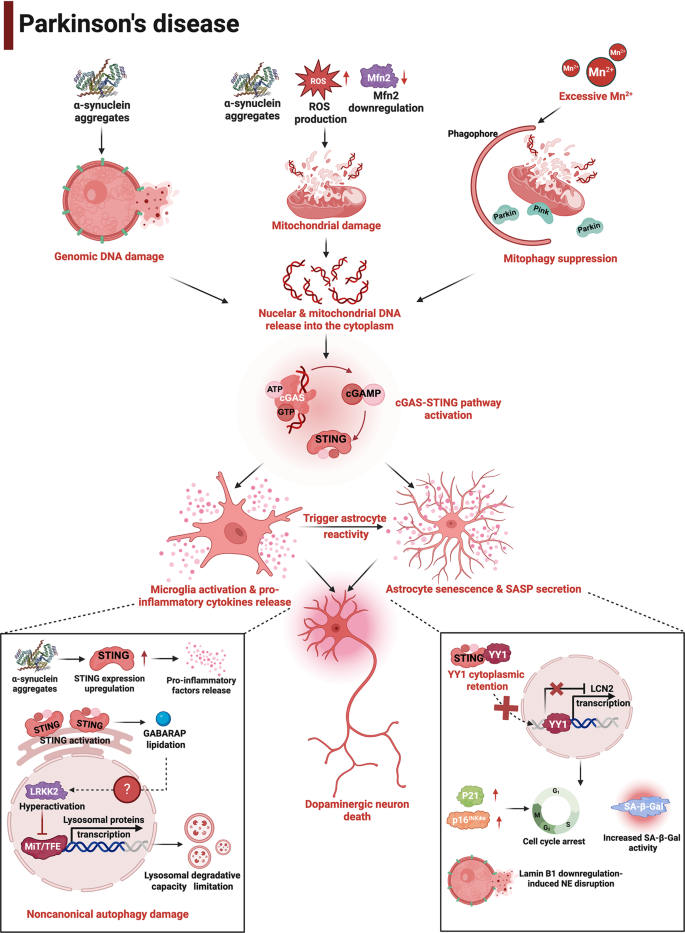
结果解读:在阿尔茨海默病中,β-淀粉样蛋白及tau蛋白诱导小胶质细胞线粒体DNA泄漏,激活cGAS-STING通路,促进神经炎症、突触丢失及β-淀粉样蛋白清除障碍;在5xFAD小鼠模型中,敲除cGAS可显著改善认知缺陷、β-淀粉样蛋白病理及神经炎症。在帕金森病中,α-突触核蛋白聚集体诱导DNA损伤及线粒体DNA泄漏,激活小胶质细胞及星形胶质细胞的cGAS-STING通路,加重多巴胺能神经元损伤;STING敲除小鼠在α-突触核蛋白预成纤维丝模型中表现出神经炎症减轻及多巴胺能神经元保留。在肌萎缩侧索硬化症中,TAR DNA结合蛋白43或超氧化物歧化酶1突变导致线粒体DNA泄漏,激活运动神经元及胶质细胞的cGAS-STING通路,诱导神经炎症及神经元死亡;患者脊髓样本中可检测到cGAMP水平升高,抑制cGAS或STING可减轻模型小鼠的疾病表型。
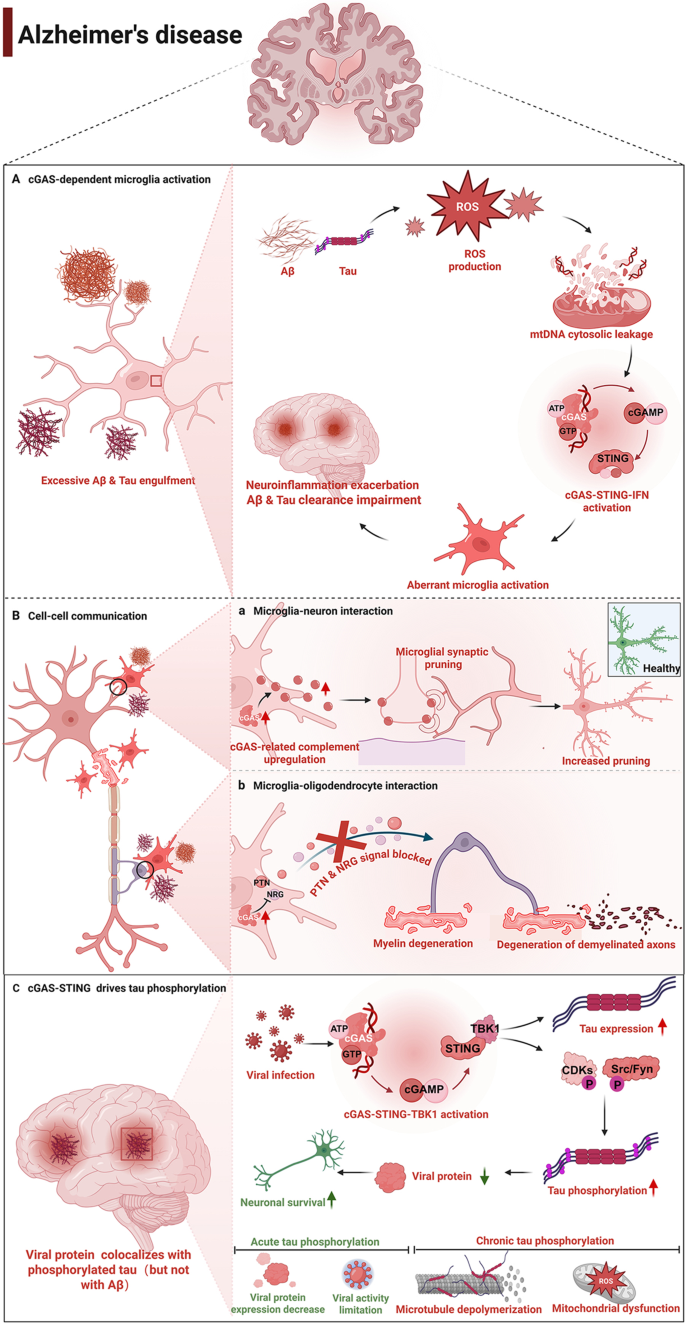
产品关联:文献未提及具体实验产品,领域常规使用神经退行性疾病动物模型(如5xFAD小鼠、α-突触核蛋白PFF小鼠、TAR DNA结合蛋白43突变小鼠)、诱导多能干细胞来源的神经元等开展研究。
3.4 靶向cGAS-STING通路的抑制剂研究进展
实验目的:总结现有cGAS-STING通路抑制剂的类型、作用机制、预临床疗效及临床转化挑战。
方法细节:检索靶向cGAS或STING的抑制剂研究文献,按作用靶点(cGAS催化位点、DNA结合位点;STING环二核苷酸结合位点、棕榈酰化位点等)对抑制剂进行分类,梳理每种抑制剂的作用机制、在细胞及动物模型中的疗效,同时分析临床转化面临的挑战(如血脑屏障穿透性、物种特异性、长期安全性等)。
结果解读:cGAS抑制剂主要包括催化位点抑制剂(如RU0.521、G150)、DNA结合位点抑制剂(如羟氯喹、Suramin);其中RU0.521可改善衰老相关内皮功能障碍及神经炎症,G150可抑制百草枯诱导的通路激活。STING抑制剂包括环二核苷酸结合位点抑制剂(如SN-011、Astin C)、棕榈酰化位点抑制剂(如H-151、C-176)及转运抑制剂(如ISD017);H-151可改善阿尔茨海默病、帕金森病模型的认知功能及病理损伤,C-176可减轻缺血性脑卒中的神经炎症。目前仅有VENT-03进入I期临床,针对神经退行性疾病的抑制剂仍处于临床前阶段,血脑屏障穿透性、物种特异性差异及长期抑制的安全性是主要挑战。


产品关联:文献未提及具体实验产品,领域常规使用细胞水平的通路激活模型(如双链DNA转染细胞)、动物疾病模型等筛选及验证抑制剂。
4. Biomarker研究及发现成果解析
这篇综述中涉及的Biomarker主要包括胞质DNA(线粒体DNA、核DNA片段)、cGAMP(cGAS催化产物)及通路激活相关分子(磷酸化STING、磷酸化TBK1等),其筛选逻辑基于cGAS-STING通路的激活机制,即胞质DNA是通路激活的上游触发因素,cGAMP及磷酸化分子是通路激活的直接标志。
在神经退行性疾病中,胞质DNA的来源包括线粒体DNA泄漏(如阿尔茨海默病中小胶质细胞、帕金森病中多巴胺能神经元)、核DNA损伤(如帕金森病中α-突触核蛋白诱导的DNA断裂),可通过实时荧光定量PCR检测细胞质中的线粒体DNA或核DNA片段水平;cGAMP作为cGAS的特异性产物,可通过液相色谱-质谱联用检测,如在肌萎缩侧索硬化症患者脊髓样本中已检测到cGAMP水平升高;通路激活相关分子(磷酸化STING、磷酸化TBK1)可通过免疫印迹或免疫荧光检测,如在阿尔茨海默病患者脑组织及5xFAD小鼠模型中可检测到磷酸化STING水平升高。这些Biomarker的特异性在于,其水平升高直接反映了cGAS-STING通路的激活状态,与疾病进展及神经炎症程度相关;但敏感性仍需进一步验证,且不同疾病中这些Biomarker的水平变化及临床意义存在差异,如阿尔茨海默病中主要是线粒体DNA水平升高,肌萎缩侧索硬化症中cGAMP水平升高更为显著。
这些Biomarker的功能关联在于,可作为cGAS-STING通路激活的直接标志,用于疾病的早期诊断、病情监测及靶向治疗的疗效评估;创新性在于,首次系统总结了胞质DNA、cGAMP及通路磷酸化分子在不同神经退行性疾病中的潜在Biomarker价值,为临床转化提供了参考。目前,部分Biomarker(如cGAMP)已在肌萎缩侧索硬化症患者样本中得到验证,但仍需大样本临床研究进一步确认其特异性与敏感性,且尚未有基于这些Biomarker的临床诊断方法获批。