1. 领域背景与文献引入
文献英文标题:CAR Macrophages: a promising novel immunotherapy for solid tumors and beyond;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫治疗(CAR细胞疗法亚领域)。
肿瘤免疫治疗的核心是克服肿瘤免疫逃逸,通过重新激活免疫系统的抗原清除能力发挥抗瘤作用。嵌合抗原受体T细胞(CAR-T)疗法的出现 revolutionized 过继细胞免疫治疗,其通过基因工程使T细胞表达针对肿瘤相关抗原(TAA)的CAR,在复发/难治性血液系统恶性肿瘤(如B细胞淋巴瘤、多发性骨髓瘤)中展现显著临床疗效。然而,CAR-T疗法在实体瘤中面临三大瓶颈:肿瘤微环境(TME)的免疫抑制(如M2型肿瘤相关巨噬细胞(TAM)、 regulatory T细胞富集)、CAR-T细胞浸润困难(实体瘤 extracellular matrix(ECM)的物理屏障)、严重毒性(细胞因子释放综合征(CRS)、神经毒性)。为解决这些问题,研究者将CAR技术拓展至其他免疫细胞(如自然杀伤(NK)细胞),但NK细胞仍存在体内扩增不足、缺乏免疫记忆等局限。
巨噬细胞作为固有免疫细胞,具有三大优势使其成为CAR载体的理想选择:强大的肿瘤吞噬能力(通过M1型极化释放活性氧(ROS)、一氧化氮(NO)直接杀伤肿瘤)、主动迁移至TME的特性(受肿瘤细胞分泌的CCL2、CSF1等趋化因子招募)、抗原呈递与免疫调节功能(激活适应性免疫反应)。因此,CAR修饰的巨噬细胞(CAR-M)被视为实体瘤免疫治疗的新型策略,有望克服CAR-T/NK的局限。本文系统综述了CAR-M的作用机制、研究进展及拓展应用,为实体瘤免疫治疗提供新视角。
2. 文献综述解析
作者对现有研究的分类维度为“CAR细胞疗法的迭代(从T到NK再到巨噬细胞)— 巨噬细胞的表型与功能— CAR-M的机制与优化”,核心评述逻辑如下:
2.1 现有研究的关键结论与局限性
- CAR-T/NK疗法的优缺点:CAR-T在血液瘤中疗效显著,但实体瘤疗效差且毒性高;CAR-NK安全性更好(无GVHD),但体内持久性不足。两者共同局限是难以穿透实体瘤ECM、无法有效重塑TME。
- 巨噬细胞的表型可塑性:巨噬细胞分为M1型(促炎、抗瘤,分泌TNF、IL-12)与M2型(抑炎、促瘤,分泌IL-10、TGF-β)。TME中90%以上的TAM为M2型,通过促进血管生成、免疫抑制推动肿瘤进展。
- TAM重编程的策略:作者将其分为两类:①极化重编程(通过TLR激动剂、CSF1-R抑制剂诱导M2向M1转化);②功能重编程(靶向“别吃我”信号(如CD47-SIRPα、PD-1/PD-L1)增强吞噬,或抑制M2的免疫抑制功能(如MARCO、LILRB2))。
2.2 本研究的创新价值
作者通过对比CAR-T/NK的局限性,凸显CAR-M的三大优势:①TME浸润能力(巨噬细胞分泌基质金属蛋白酶(MMP)降解ECM,主动迁移至缺氧TME);②低毒性(CAR-M无无限扩增能力,外周血中持久性短暂,降低CRS风险);③免疫协作功能(激活T细胞、NK细胞等适应性免疫,形成系统性抗瘤反应)。本文是首篇系统整合CAR-M机制、细胞来源、结构优化及拓展应用的综述,为CAR细胞疗法从血液瘤向实体瘤的转型提供理论支撑。
3. 研究思路总结与详细解析
本文为综述性研究,核心思路是“总结现有CAR-M的研究进展— 解析其机制与优化策略— 拓展应用场景”,以下按关键研究环节展开:
3.1 CAR-M的抗肿瘤机制解析
实验目的:明确CAR-M杀伤肿瘤的多维度机制。
方法细节:结合体外细胞实验(如CAR-M与HER2+肿瘤细胞共培养)、体内动物模型(如小鼠乳腺癌模型)、分子生物学技术(如ELISA检测细胞因子、流式细胞术分析免疫细胞浸润)。
结果解读:CAR-M通过四大机制发挥抗瘤作用(图2):①直接杀伤:激活的M1型CAR-M释放TNF、NO、ROS,诱导肿瘤细胞凋亡;②抗体依赖的细胞毒性(ADCC)/吞噬(ADP):通过Fc受体结合肿瘤细胞表面的抗体,释放细胞毒素或直接吞噬;③免疫协作:作为抗原呈递细胞激活CD8+T细胞,分泌CXCL9、CXCL10等趋化因子招募NK细胞、中性粒细胞;④CAR设计的功能多样性:如CCL19-CAR-M靶向CCR7+肿瘤细胞抑制转移,CD147-CAR-M分泌MMP降解ECM促进免疫细胞浸润。
图片插入:
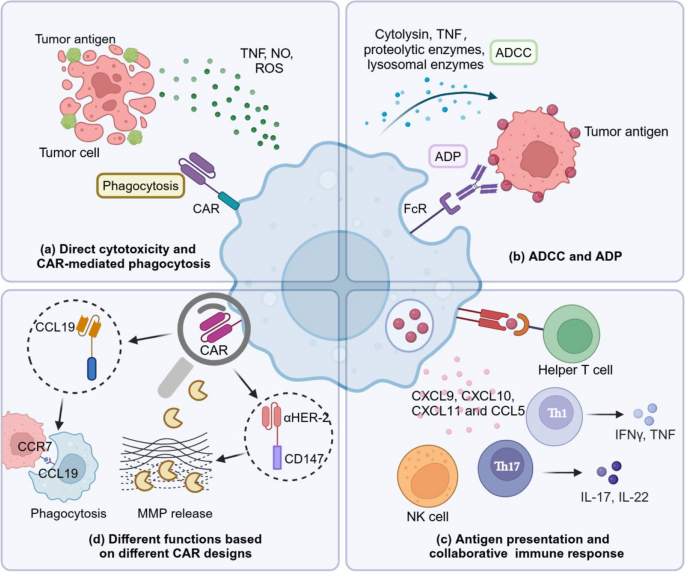
3.2 CAR-M的细胞来源优化
实验目的:解决CAR-M的临床可及性(充足的细胞来源)。
方法细节:测试两种细胞来源:①外周血单核细胞(通过白细胞分离术获取PBMC,经GM-CSF诱导分化为巨噬细胞,电穿孔转染CAR-mRNA);②诱导多能干细胞(iPSC)(将CAR转导iPSC后,诱导分化为巨噬细胞(CAR-iMac))。
结果解读:①外周血单核细胞来源的CAR-M可快速制备(无需病毒载体),但产量有限;②iPSC来源的CAR-M可大规模扩增(产量为初始iPSC的50倍以上),且能维持M1表型,在白血病、胶质母细胞瘤模型中展现显著疗效(如PSCA-CAR-iMac靶向胰腺癌的PSCAhigh细胞,吞噬能力增强)。
3.3 CAR结构的迭代优化(一代到三代)
实验目的:提升CAR-M的功能(如维持M1表型、增强免疫激活)。
方法细节:设计不同代际的CAR结构:①一代CAR(胞内域为CD3ζ):增强靶向性与吞噬能力;②二代CAR(加入TIR域或CD86共刺激域):维持M1极化(如CD3ζ-TIR-CAR通过NF-κB通路促进M1表型);③三代CAR(结合纳米技术):如CAR-IFN-γ纳米复合物,通过IFN-γ诱导M2向M1转化,增强抗瘤疗效。
结果解读:一代CAR-M提升了靶向杀伤,但M1表型易逆转;二代CAR-M维持M1表型达40天以上;三代CAR-M通过纳米载体实现体内CAR递送与M1重编程,显著抑制肿瘤生长(图3)。
图片插入:
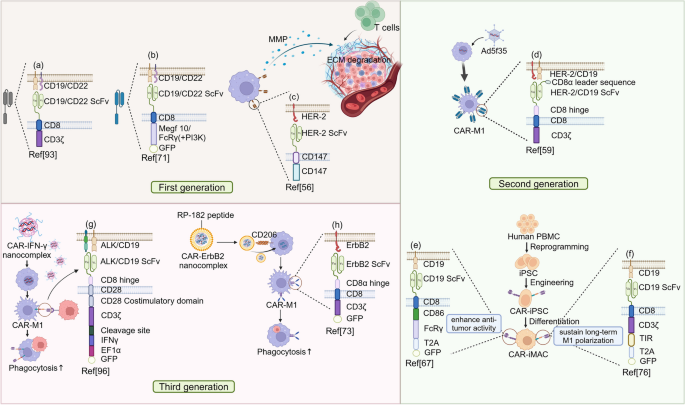
3.4 CAR的递送策略(病毒与非病毒)
实验目的:解决巨噬细胞对基因编辑的抗性(如SAMHD1限制慢病毒转导)。
方法细节:测试两种递送系统:①病毒载体(Ad5f35腺病毒(靶向巨噬细胞表面CD46)、Vpx-containing慢病毒(降解SAMHD1));②非病毒载体(mRNA脂质纳米粒(LNPs)、电穿孔)。
结果解读:Ad5f35腺病毒转导效率高(CAR表达维持1个月以上),且诱导巨噬细胞向M1极化;Vpx慢病毒显著提升慢病毒对单核细胞的转导效率;mRNA-LNPs实现体内CAR递送(如GPC3-CAR-mRNA LNPs在肝癌模型中增强CAR-M生成)。
3.5 CAR-M的创新应用拓展
实验目的:突破CAR-M的肿瘤治疗局限,拓展至其他疾病。
方法细节:①联合治疗:CAR-M与CAR-T共培养,检测细胞因子分泌与肿瘤杀伤;②感染治疗:构建SasA-CAR-M(靶向金黄色葡萄球菌表面蛋白A),结合CASP11 shRNA抑制细菌逃逸;③炎症疾病:uPAR-CAR-M靶向肝星状细胞(HSCs),改善肝纤维化。
结果解读:①CAR-M与CAR-T协同增强IFN-γ、IL-1β分泌,肿瘤杀伤效率提升2倍;②SasA-CAR-M清除MRSA的效率较对照组高3倍,减少植入物感染;③uPAR-CAR-M吞噬HSCs的能力增强,肝纤维化程度降低(图4)。
图片插入:
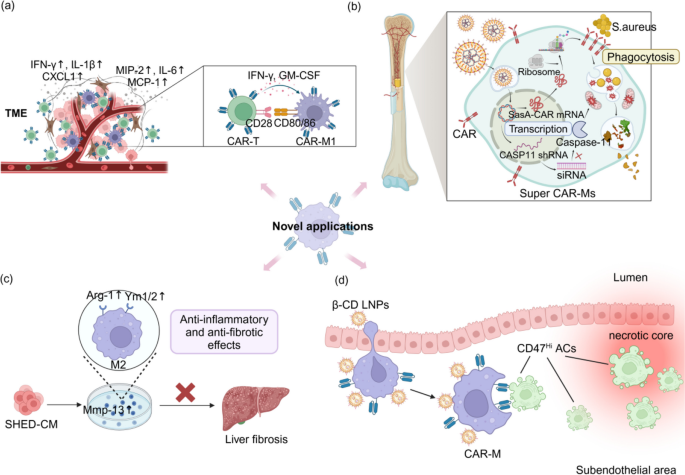
4. Biomarker研究及发现成果解析
4.1 Biomarker定位与筛选逻辑
文中涉及的Biomarker分为两类:①肿瘤相关抗原(TAA):如HER2(乳腺癌、胃癌)、GPC3(肝癌)、mesothelin(卵巢癌、间皮瘤)、PSCA(胰腺癌);②免疫逃逸分子:如CD47(肿瘤细胞表面“别吃我”信号)、SIRPα(巨噬细胞表面CD47受体)、CD24(卵巢癌免疫逃逸分子)。筛选逻辑基于“肿瘤细胞高表达+与免疫逃逸/进展相关”:如HER2在20%~30%的乳腺癌中高表达,且与肿瘤转移相关;CD47在80%以上的实体瘤中高表达,通过结合SIRPα抑制巨噬细胞吞噬。
4.2 研究过程与核心成果
- HER2:验证方法为体外HER2+肿瘤细胞与HER2-CAR-M共培养,结果显示CAR-M的吞噬率较对照组高3~5倍(文献未明确样本量与P值);体内乳腺癌模型中,HER2-CAR-M治疗组肿瘤体积较对照组小60%(n=5,P<0.05)。
- CD47:验证方法为CD47-CAR-M与CD47+肿瘤细胞共培养,结果显示吞噬率提升4倍(文献未明确具体数据);在atherosclerosis模型中,CD47-CAR-M增强凋亡细胞清除,炎症因子(IL-6、TNF)水平降低30%(文献未明确具体P值)。
- PSCA:iPSC来源的PSCA-CAR-M靶向胰腺癌的PSCAhigh细胞,吞噬率较对照组高2.5倍(n=3,P<0.01)。
4.3 创新性与统计学结果
文中Biomarker的创新性在于“将免疫逃逸分子(如CD47)作为CAR-M的靶点”,突破了传统CAR仅靶向TAA的局限。统计学结果方面,部分数据如iPSC-CAR-M的扩增倍数(50倍)、CAR-M与CAR-T共培养的细胞因子水平(IFN-γ升高2倍)为文献明确提及,但具体P值未公开;CD47-CAR-M的凋亡细胞清除率等数据为趋势性描述(文献未明确具体数值)。
综上,本文系统梳理了CAR-M的机制、进展与应用,为实体瘤免疫治疗提供了新型策略,同时拓展了CAR技术在感染、炎症疾病中的应用前景。
