1. 领域背景与文献引入
文献英文标题:Diagnostic and prognostic microRNAs in the serum of breast cancer patients measured by droplet digital PCR;发表期刊:Biomarker Research;影响因子:未公开;研究领域:乳腺癌循环microRNA生物标志物。
乳腺癌是工业化国家女性最常见的恶性肿瘤,也是第二大癌症死因,全球每年约130万女性确诊。早期乳腺癌(I/II期)5年生存率达90%,但晚期(III/IV期)仅20%,因此早期诊断和预后监测是改善患者结局的关键。现有循环生物标志物如癌胚抗原(CEA)、糖类抗原15-3(CA15-3)因敏感性(约50%)和特异性(约80%)低,仅用于患者随访,无法满足早期诊断需求。
2008年以来,循环microRNA(miRNA)因在血清/血浆中稳定存在、能反映肿瘤基因表达特征,被认为是潜在的非侵入性生物标志物。然而,预分析(样本收集/储存、RNA提取)和分析(定量方法、归一化策略)变量严重影响结果重复性——传统实时定量PCR(qRT-PCR)需依赖内参基因归一化,易因内参稳定性差引入偏差;不同研究的样本类型(血浆vs血清)、队列异质性(年龄、肿瘤分期)也导致结果矛盾。为解决这些问题,本研究采用droplet数字PCR(ddPCR)技术,实现循环miRNA的绝对定量,并通过两个独立队列验证结果的一致性,旨在明确循环miRNA作为乳腺癌诊断和预后生物标志物的价值。
2. 文献综述解析
作者对现有研究的分类维度主要基于技术方法(qRT-PCR vs ddPCR)、样本特征(血浆vs血清、队列异质性)及结果重复性。现有研究的核心结论包括:①部分循环miRNA(如miR-10b、miR-145)在乳腺癌患者中表达异常,可区分患者与健康人;②循环miRNA具有稳定性和非侵入性优势,适合长期监测。但局限性显著:
- 预分析变量:样本处理流程不统一(如血浆vs血清),导致同一miRNA在不同研究中结果相反(如miR-652在血浆中升高、血清中降低);
- 分析变量:qRT-PCR依赖内参基因(如U6、cel-miR-39)归一化,内参稳定性差会放大误差;
- 队列异质性:多数研究仅纳入单一中心、小样本队列,结果难以推广。
本文的创新点在于:①采用ddPCR技术绝对定量循环miRNA,无需归一化,减少分析变量;②纳入两个独立队列(意大利费拉拉大学医院、美国Mercy妇女中心),验证结果的跨人群一致性;③同时评估miRNA的诊断价值(区分患者与对照)和预后价值(关联临床病理特征),弥补了现有研究仅关注诊断的不足。
3. 研究思路总结与详细解析
整体框架
研究目标:验证循环miRNA作为乳腺癌诊断/预后生物标志物的有效性,明确ddPCR在循环miRNA定量中的优势;
核心科学问题:哪些循环miRNA可作为乳腺癌诊断/预后标志物?ddPCR能否提高结果的重复性?
技术路线:候选miRNA筛选→两个独立队列样本收集→ddPCR绝对定量→ROC曲线诊断效能分析→临床病理特征关联预后分析。
3.1 候选miRNA筛选
实验目的:筛选潜在的乳腺癌循环miRNA生物标志物。
方法细节:基于前期芯片实验结果及已发表文献,选择5个与乳腺癌相关的miRNA(miR-10b-5p、miR-145-5p、miR-148b-3p、miR-425-5p、miR-652-3p)——这些miRNA在既往研究中被报道与乳腺癌发生、转移相关。
结果解读:确定5个候选miRNA,为后续验证提供靶点。
产品关联:文献未提及具体实验产品,领域常规通过芯片技术或系统性文献回顾筛选候选miRNA。
3.2 队列样本收集与标准化处理
实验目的:获取标准化血清样本,减少预分析变量。
方法细节:纳入两个独立队列:①队列A(意大利):28例乳腺癌患者、27例健康对照(2012-2014年收集);②队列B(美国):59例乳腺癌患者、35例健康对照(2005-2013年收集)。血样均用红塞clot管(队列A:Greiner Bio-One VACUETTE;队列B:BD Vacutainer)收集,1小时内以1000g离心10分钟分离血清,-80℃保存为200μL aliquots。每样本添加3μL 4.16nM合成cel-miR-39-3p(IDT,线虫来源,人血清中无表达)作为外参,用Qiagen MiRNeasy kit提取总RNA(200μL血清→35μL无核酸酶水洗脱)。
结果解读:获得标准化处理的血清RNA样本,保证两个队列的可比性。
产品关联:实验所用关键产品:Greiner Bio-One VACUETTE红塞管(队列A)、BD Vacutainer红塞管(队列B)、IDT合成cel-miR-39-3p、Qiagen MiRNeasy kit。
3.3 ddPCR绝对定量循环miRNA
实验目的:实现循环miRNA的绝对定量,减少分析变量。
方法细节:用Exiqon Universal cDNA synthesis kit II将3μL RNA反转录为cDNA(20μL反应体系),稀释50倍后取8μL用于ddPCR。PCR反应体系含miRCURY LNA Universal RT microRNA PCR试剂盒(Exiqon,针对miRNA设计的LNA引物,提高特异性)和Bio-Rad EvaGreen(荧光染料),与70μL droplet generator oil混合后,用Bio-Rad QX200 droplet generator生成约20000个纳米级 droplets(将反应体系分割为独立单元,实现单分子扩增)。PCR终点扩增(95℃ 10分钟→40个循环:94℃ 30秒、58℃ 1分钟→98℃ 10分钟)后,用QX200 droplet reader计数阳性 droplets(含目标miRNA,荧光信号高)和阴性 droplets(无目标miRNA,荧光信号低),通过Poisson统计计算miRNA绝对浓度(拷贝/μL血清)。
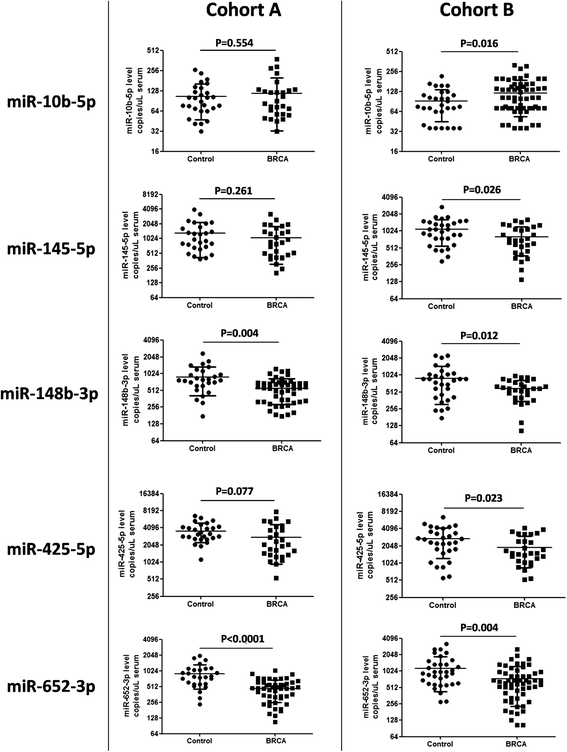
结果解读:①诊断相关miRNA:miR-148b-3p和miR-652-3p在两个队列中均显著低于对照(队列A:p=0.0042、p<0.0001;队列B:p=0.0115、p=0.0043);②预后相关miRNA:miR-10b-5p在队列B中与对照相比显著升高(p=0.016),且与肿瘤晚期分期相关。
产品关联:实验所用关键产品:Exiqon Universal cDNA synthesis kit II、miRCURY LNA Universal RT microRNA PCR试剂盒、Bio-Rad EvaGreen、QX200 droplet generator及reader。
3.4 ROC曲线分析诊断价值
实验目的:评估候选miRNA的诊断效能。
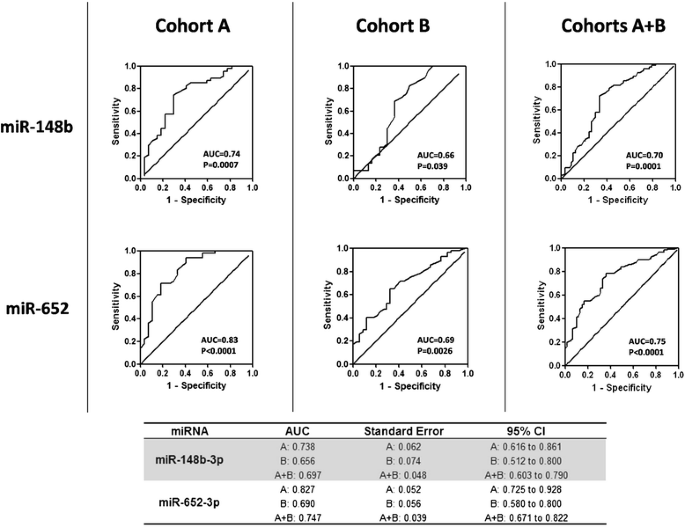
方法细节:对两个队列的miRNA浓度数据进行二元logistic回归,生成受试者工作特征(ROC)曲线,计算曲线下面积(AUC)——AUC越接近1,诊断效能越好。
结果解读:miR-148b-3p和miR-652-3p在两个队列中均具有显著诊断价值(队列A:miR-148b-3p AUC=0.72、miR-652-3p AUC=0.81;队列B:miR-148b-3p AUC=0.68、miR-652-3p AUC=0.75);联合两个队列后,AUC进一步提高至0.78(miR-148b-3p)和0.83(miR-652-3p),表明其作为诊断标志物的潜力。
产品关联:文献未提及具体实验产品,领域常规使用GraphPad Prism等统计软件进行ROC曲线分析。
3.5 临床病理特征关联分析预后价值
实验目的:分析循环miRNA与乳腺癌预后的关联。
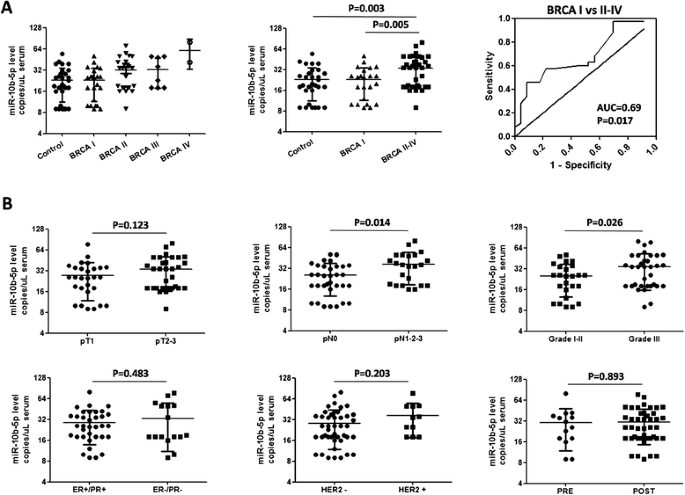
方法细节:纳入队列B(包含I-IV期肿瘤,队列A仅含I/II期,无法分析预后),将miRNA浓度与临床病理特征(肿瘤分期、分级、淋巴结转移、ER/PR/HER2状态)关联,用非配对t检验评估差异显著性。
结果解读:①miR-10b-5p水平随肿瘤分期升高而显著增加(II-IV期vs I期:p=0.0047);②与高肿瘤分级(p=0.026)、淋巴结转移(p=0.014)相关;③虽无统计学意义,但ER/PR阴性、HER2阳性患者的miR-10b-5p水平也呈升高趋势(提示与侵袭性表型相关)。其他miRNA(如miR-145、miR-425)未发现与临床病理特征相关。
产品关联:文献未提及具体实验产品,领域常规通过医院信息系统获取临床病理数据,并用SPSS等统计软件进行关联分析。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
- 诊断Biomarker:miR-148b-3p、miR-652-3p;筛选逻辑:芯片/文献筛选→两个独立队列验证→ROC曲线确认诊断效能;
- 预后Biomarker:miR-10b-5p;筛选逻辑:关联临床病理特征→队列B验证(含各分期)。
研究过程详述
- Biomarker来源:乳腺癌患者和健康对照的血清样本(而非血浆,因血清更易标准化收集);
- 验证方法:ddPCR绝对定量(保证结果准确性);诊断效能通过ROC曲线评估(AUC反映区分能力);预后价值通过关联临床病理特征分析(p值反映相关性);
- 特异性与敏感性:①miR-148b-3p和miR-652-3p在两个队列中的ROC曲线AUC均显著(队列A:miR-148b-3p p=0.0042、miR-652-3p p<0.0001;队列B:miR-148b-3p p=0.0115、miR-652-3p p=0.0043);②miR-10b-5p在队列B中,II-IV期患者 vs I期患者的敏感性通过p值体现(p=0.0047),提示其能区分早期与晚期肿瘤。
核心成果与创新性
- 诊断价值:miR-148b-3p和miR-652-3p可作为乳腺癌诊断生物标志物,在两个独立队列中均能显著区分患者与对照,联合队列后AUC进一步提高(miR-652-3p AUC=0.83);
- 预后价值:miR-10b-5p可作为乳腺癌预后生物标志物,水平越高,肿瘤分期越晚、分级越高、淋巴结转移风险越大;
- 技术优势:ddPCR绝对定量减少了预分析和分析变量,结果在两个队列中一致,解决了现有研究重复性差的问题。
总结
本研究通过ddPCR技术和两个独立队列验证,明确了miR-148b-3p、miR-652-3p作为乳腺癌诊断生物标志物的价值,以及miR-10b-5p作为预后生物标志物的潜力。ddPCR的绝对定量优势为循环miRNA的临床应用提供了技术支撑,也为解决现有研究的重复性问题提供了新思路。未来需进一步扩大队列规模,验证这些miRNA在早期乳腺癌中的诊断价值,推动其向临床转化。
