1. 领域背景与文献引入
文献英文标题:Machine learning-aided risk stratification in Philadelphia chromosome-positive acute lymphoblastic leukemia;发表期刊:Biomarker Research;影响因子:未公开;研究领域:血液系统恶性肿瘤(费城染色体阳性急性淋巴细胞白血病预后研究)。
费城染色体阳性急性淋巴细胞白血病(Ph+ ALL)是成人急性淋巴细胞白血病中预后较差的亚型,现有研究已识别出微小残留病(MRD)、染色体异常(如+der(22)t(9;22))、遗传病变等预后因素,但传统统计分析依赖人工变量选择,易遗漏潜在关联,且部分患者的高危群体仍未明确分层。此外,临床中常因样本量小难以开展精准预后研究,亟需更高效的方法挖掘关键因素。基于此,文献提出利用eXtreme Gradient Boosting(XGBoost)机器学习算法,从少样本数据中识别Ph+ ALL的关键预后特征,构建事件预测模型并优化风险分层,弥补传统分析的局限性,为临床精准治疗提供依据。
2. 文献综述解析
文献综述的核心评述逻辑为:作者先总结Ph+ ALL现有预后研究的核心结论——微小残留病、染色体异常、遗传病变是已知预后因素,但传统Cox比例风险模型存在“人工选变量”的偏倚,可能忽略非直观的关联;随后强调机器学习(尤其是可解释的XGBoost算法)的优势:能从复杂数据中提取潜在特征,且适用于小样本研究。
现有研究的局限性在于:① 未系统整合“诊断时的分子指标(如BCR-ABL PCR值)”与临床特征进行分层;② 传统分析难以从少样本中挖掘稳定的预后因素。文献的创新价值在于首次将XGBoost算法应用于Ph+ ALL预后研究,从59例患者的小样本数据中识别出“诊断时的BCR-ABL PCR值”这一传统分析中未被关注的新预后因素,并通过置换特征重要性验证其可靠性,为Ph+ ALL的风险分层提供了更精准的方法。
3. 研究思路总结与详细解析
整体框架:研究目标为建立Ph+ ALL事件(复发、死亡等)预测模型,识别关键预后因素并优化生存风险分层;核心科学问题是挖掘Ph+ ALL患者预后的关键特征,验证其对无事件生存(EFS)和总生存(OS)的分层能力;技术路线为“59例患者数据→80%训练集构建XGBoost模型→20%测试集验证→特征重要性分析→置换特征重要性确认→风险分层与生存分析”的闭环。
3.1 数据集与XGBoost模型构建
实验目的是利用小样本临床数据构建Ph+ ALL事件预测模型。方法细节为纳入59例成人Ph+ ALL患者(n=59)的基线数据,包括BCR-ABL谱系(单谱系/多谱系)、诊断时BCR-ABL聚合酶链反应(PCR)值、年龄、白细胞计数等,按8:2比例分为训练集(n=47)和测试集(n=12),使用XGBoost算法构建模型,评估指标包括准确率、精确率、召回率、F1-score及受试者工作特征曲线下面积(AUC)。
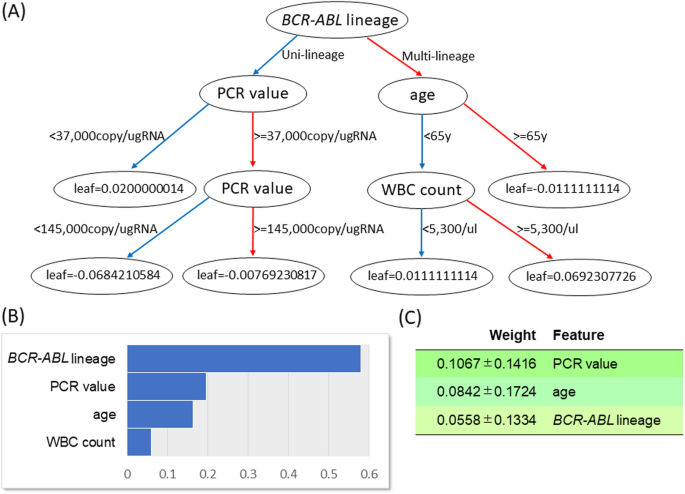
结果解读:训练集交叉验证准确率为0.66(标准差0.072),测试集平均准确率0.67,宏平均精确率0.71、召回率0.78、F1-score0.66,AUC为0.76;特征重要性得分显示,BCR-ABL谱系、诊断时BCR-ABL PCR值、年龄、白细胞计数是模型的关键特征(Fig.1a、b)。
实验所用关键产品:文献未提及具体实验产品,领域常规使用机器学习软件库(如XGBoost Python/R包)、统计分析工具(如R语言、Python的scikit-learn库)。
3.2 特征重要性验证
实验目的是确认关键特征对模型预测的可靠性。方法细节为使用测试集进行置换特征重要性分析(随机打乱单个特征的值,观察模型性能下降程度),评估特征的稳定度。
结果解读:置换特征重要性分析显示,BCR-ABL PCR值、年龄、BCR-ABL谱系仍是测试集预测的重要特征(Fig.1c),与训练集的特征重要性一致,说明这些特征的预测价值稳定,不受样本划分影响。
3.3 风险分层与生存分析
实验目的是基于关键特征构建风险分组,评估其对生存结局的分层能力。方法细节为根据XGBoost决策树的二分指数,将“BCR-ABL单谱系表达(uni-Ph)、诊断时BCR-ABL PCR值≥14500copies/μgRNA、年龄≥65岁、白细胞计数≥5300/μl”定义为风险因素,按风险因素数量将患者分为低风险组(≤2个因素)、中风险组(3个因素)、高风险组(4个因素),采用Kaplan-Meier法分析各组的EFS和OS。
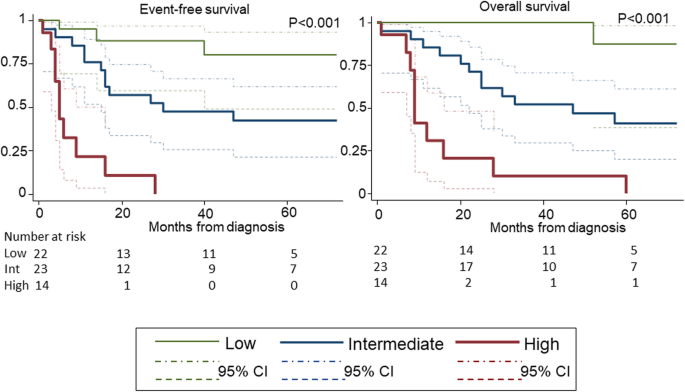
结果解读:4年时,低风险组EFS为80%(95%CI 49–93%)、OS为100%;中风险组EFS为42%(21–62%)、OS为47%(25–66%);高风险组EFS为0、OS为10%(0.6–37%),分层差异显著(Fig.2);测试集验证显示,低风险组4年EFS为100%,中风险组为80%(20–97%),高风险组为0%(P=0.046),进一步确认了分层的可靠性。
4. Biomarker研究及发现成果解析
Biomarker定位
文献涉及的Biomarker为“BCR-ABL谱系、诊断时BCR-ABL PCR值、年龄、白细胞计数”,属于“临床特征+分子指标”的联合Biomarker;筛选逻辑为“XGBoost模型特征重要性得分初步识别→置换特征重要性验证→生存分析确认分层能力”的完整链条,确保了Biomarker的稳定性与临床价值。
研究过程详述
Biomarker来源为59例成人Ph+ ALL患者的基线临床数据(年龄、白细胞计数)及诊断时的分子检测结果(BCR-ABL谱系、BCR-ABL PCR值);验证方法包括:① XGBoost模型的训练与测试(评估预测性能);② 置换特征重要性分析(验证特征稳定性);③ Kaplan-Meier生存分析(验证分层效果)。
特异性与敏感性数据:测试集AUC为0.76,使用XGBoost模型参数时AUC提升至0.77(标准误0.06),敏感性0.59,特异性0.89;传统Cox模型的AUC为0.72,显示机器学习模型的预测性能更优。
核心成果提炼
- 新预后因素的发现:诊断时的BCR-ABL PCR值是传统分析中未被关注的新预后因素(传统分析多关注治疗后的微小残留病,而非诊断时的PCR值),其与BCR-ABL谱系、年龄、白细胞计数联合,可有效分层患者的生存结局。
- 风险分层的临床价值:低风险组(≤2个因素)4年OS达100%(n=59),高风险组仅10%(n=59),分层差异显著;测试集验证显示,高风险组4年EFS为0%(P=0.046),说明该Biomarker组合能精准识别高危患者。
- 机器学习的优势:XGBoost算法从59例的小样本数据中提取了稳定的特征,减少了传统分析的人工变量选择偏倚,为小样本临床研究提供了新方法。
综上,该Biomarker组合为Ph+ ALL的风险分层提供了更精准的工具,其中“诊断时的BCR-ABL PCR值”的发现补充了传统预后研究的不足,具有重要的临床转化价值。
