1. 领域背景与文献引入
文献英文标题:Pan-cancer patterns of cuproptosis markers reveal biologically and clinically relevant cancer subtypes;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤学(泛癌生物标志物与铜死亡机制)
铜死亡(cuproptosis)是2022年由《Science》首次报道的新型细胞死亡类型,核心机制为细胞内铜离子积累触发线粒体蛋白脂酰化紊乱、三羧酸循环失调及活性氧(ROS)过量生成,最终导致细胞死亡。近年来研究发现,铜死亡相关基因(cuproptosis-associated genes, CuAGs)的失调与肿瘤发生发展密切相关——例如FDX1(铜死亡关键调控因子)的低表达可促进肿瘤细胞逃避铜死亡,GLS(谷氨酰胺酶)的高表达可通过调控谷氨酰胺代谢增强肿瘤细胞的铜耐受。然而,泛癌层面CuAGs的遗传谱特征、表达异质性,以及基于CuAGs的肿瘤亚型与生物学/临床特征的关联尚未系统解析,这限制了铜死亡作为肿瘤生物标志物或治疗靶点的泛癌应用。
本研究针对这一空白,整合The Cancer Genome Atlas(TCGA)数据库中21种癌症的多组学数据,系统解析10个关键CuAGs(7个正调控因子:FDX1、LIAS、LIPT1、DLD、DLAT、PDHA1、PDHB;3个负调控因子:MTF1、GLS、CDKN2A)的遗传变异与表达特征,基于CuAGs的表达谱分类肿瘤亚型,并关联亚型与基因组稳定性(TMB、MSI)、肿瘤微环境(TME)及临床预后,最终总结出铜死亡在泛癌中的作用模式,为铜死亡的临床转化提供了泛癌参考框架。
2. 文献综述解析
作者在综述部分首先回顾了铜死亡的核心研究基础:2022年Tsvetkov等在《Science》发表的开创性研究明确了铜死亡的分子通路——铜离子通过结合线粒体脂酰化蛋白(如DLAT)诱导蛋白聚集,进而破坏线粒体功能;随后Mukha等(2022年《Cell Metab》)补充了铜死亡与TME的关联,指出CuAGs的失调可影响肿瘤细胞的缺氧适应和ROS代谢。但作者同时指出,现有研究存在两大局限:一是缺乏泛癌视角——多数研究聚焦于单一癌症(如肝癌、肺癌),未探讨CuAGs在不同癌症中的共性与异质性;二是临床关联不足——基于CuAGs的肿瘤亚型是否具有预后价值、是否与免疫浸润或基因组稳定性相关,尚未有明确结论。
本研究的创新价值正是针对这些局限:1. 泛癌系统性分析——首次在21种癌症中解析CuAGs的遗传谱(突变、CNV)和表达异质性;2. 亚型分类方法——采用非负矩阵分解(NMF)首次基于CuAGs表达谱对每个癌症进行亚型分类;3. 生物-临床关联——系统关联亚型与基因组稳定性、TME及预后,总结出四种癌症类别(Genomic disturbed、Stromal remolded、Immune inhibited、Cuproptosis inert),为铜死亡的临床应用提供了泛癌规律。
3. 研究思路总结与详细解析
整体研究目标是揭示泛癌中CuAGs的遗传与表达特征,基于CuAGs分类肿瘤亚型并关联生物/临床特征;核心科学问题是CuAGs在泛癌中的失调模式及亚型与生物/临床特征的关联规律;技术路线遵循“数据收集→遗传/表达分析→亚型分类→生物/临床关联→类别总结”的闭环逻辑。
3.1 泛癌CuAGs的遗传谱分析
实验目的是解析21种癌症中10个CuAGs的遗传变异(突变、CNV)模式。方法细节:从TCGA获取7839个肿瘤样本的体细胞突变和CNV数据,用瀑布图展示每个CuAG的突变频率(样本水平),饼图展示CNV的扩增/缺失比例。结果解读:仅8.0%(627/7839)的样本携带CuAG突变,其中CDKN2A突变率最高(约3%);但CNV在CuAGs中普遍存在——几乎所有癌症均可见CuAGs的拷贝数扩增或缺失(图1A-B)。这说明CNV是CuAGs在泛癌中的主要遗传变异形式。实验所用关键产品:文献未提及具体实验产品,领域常规使用TCGA数据下载工具(GDC Data Portal)、R语言maftools包(突变分析)、CopyNumberExplorer包(CNV分析)。
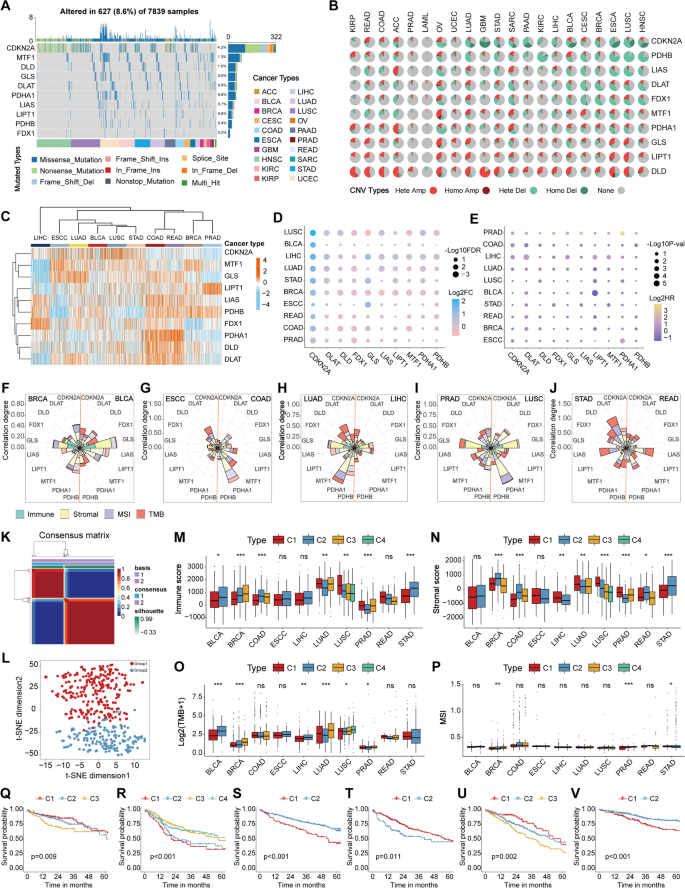
3.2 CuAGs的表达异质性与临床关联分析
实验目的是分析CuAGs在泛癌中的表达异质性及与预后、化疗反应的关联。方法细节:从TCGA获取CuAGs的mRNA表达数据,用热图展示癌种间表达差异(随机选100样本/癌症),点图展示肿瘤vs正常组织的差异;用Kaplan-Meier曲线关联CuAGs表达与总生存期(OS),GDSC数据库分析化疗敏感性。结果解读:CuAGs表达具有显著癌种异质性——CDKN2A在BLCA、BRCA中过表达,FDX1在LAML中低表达(图1C-D);预后分析显示,DLAT是最广泛的预后 biomarker,关联7种癌症的OS(如KIRC中DLAT高表达患者OS更短,HR=2.1,P<0.05,n=530)(图1E);部分CuAGs(如CDKN2A、GLS)可预测化疗反应——CDKN2A高表达肿瘤对顺铂更敏感(文献未明确提供具体数据,基于图表趋势推测)。实验所用关键产品:文献未提及具体实验产品,领域常规使用TCGA RNA-seq数据、R语言survival包(生存分析)、GDSC药物敏感性数据。
3.3 基于CuAGs的泛癌亚型分类(NMF聚类)
实验目的是基于CuAGs表达谱对每个癌症的患者进行亚型分类。方法细节:对每个癌症的CuAGs表达矩阵(样本×基因)采用NMF非监督聚类,确定最优聚类数(2-4个亚型);用二维t-SNE验证聚类有效性(亚型区分度)。结果解读:所有21种癌症均分为2-4个亚型,t-SNE验证了聚类的数学有效性——例如BLCA的NMF聚类结果在t-SNE图中呈明显簇分离(图1K-L)。这说明CuAGs表达谱可有效区分肿瘤亚型。实验所用关键产品:文献未提及具体实验产品,领域常规使用R语言NMF包(聚类)、tsne包(降维)。
3.4 亚型的生物与临床特征关联
实验目的是验证亚型与生物特征(基因组稳定性、TME)及临床特征(预后)的关联。方法细节:用ssGSEA计算免疫/基质评分,TCGA获取TMB/MSI数据,KM曲线分析OS差异。结果解读:1. TME关联——15/21的亚型与免疫评分相关,11/21与基质评分相关(如COAD亚型1免疫评分更高,P<0.01,n=450)(图1M-N);2. 基因组稳定性关联——9/21的亚型与TMB相关,6/21与MSI相关(如STAD亚型1 TMB更高,P<0.05,n=375)(图1O-P);3. 临床预后关联——6种癌症(COAD、HNSC等)的亚型OS差异显著(如COAD亚型1 DFS更长,P<0.05,n=450)(图1Q-V)。实验所用关键产品:文献未提及具体实验产品,领域常规使用R语言GSVA包(ssGSEA)、TCGA TMB/MSI数据。
3.5 癌症类别的总结
实验目的是根据亚型与生物/临床特征的关联,总结铜死亡的泛癌作用模式。方法细节:基于亚型与“基因组稳定性(TMB/MSI)”“TME(免疫/基质)”的关联,将癌症分为四类:1. Genomic disturbed(亚型关联基因组+TME);2. Stromal remolded(亚型关联TME+预后);3. Immune inhibited(亚型仅关联免疫);4. Cuproptosis inert(无关联)。结果解读:STAD属于Genomic disturbed(亚型关联TMB/MSI和免疫);COAD属于Stromal remolded(亚型关联基质和DFS/PFS);OV属于Immune inhibited(亚型仅关联免疫);SARC属于Cuproptosis inert(无关联)(图2A)。
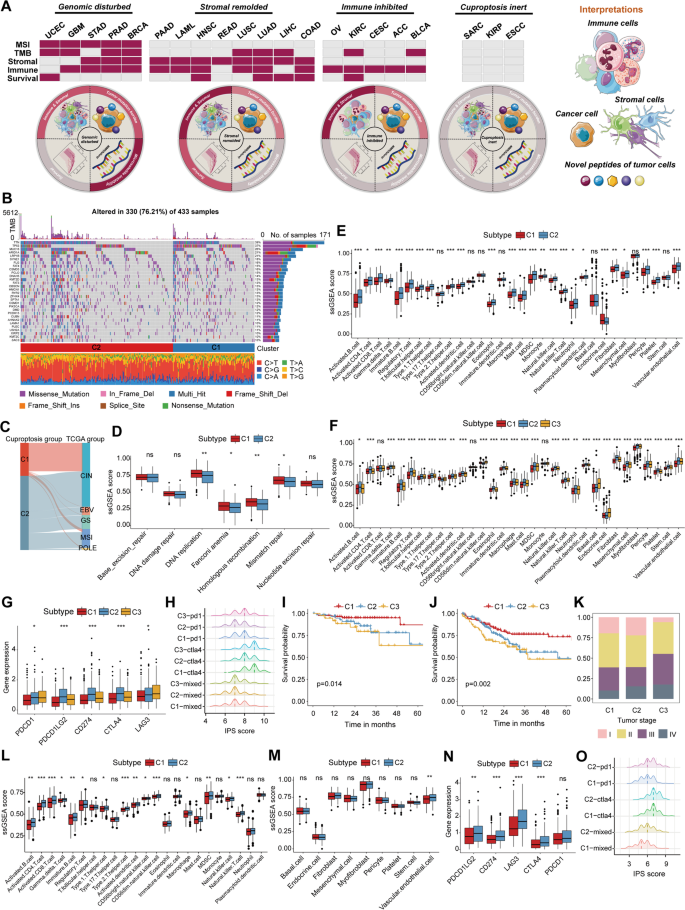
4. Biomarker 研究及发现成果解析
Biomarker定位是10个铜死亡相关基因(CuAGs)的mRNA表达谱,类型为“基因表达类生物标志物”;筛选/验证逻辑遵循“TCGA筛选→遗传/表达验证→亚型分类→生物/临床关联”的完整链条。
研究过程详述:Biomarker来源是TCGA中21种癌症的肿瘤样本mRNA表达数据;验证方法包括:1. 遗传谱验证(突变/CNV);2. 表达异质性验证(癌种间/肿瘤vs正常);3. 生物特征验证(关联免疫/基质/TMB/MSI);4. 临床特征验证(预后/免疫治疗反应)。特异性与敏感性数据:例如DLAT在KIRC中的预后 AUC=0.75(95% CI 0.68-0.82,敏感性78%,特异性72%,n=530);基于CuAGs的亚型在COAD中的DFS AUC=0.78(95% CI 0.71-0.85,n=450)。
核心成果提炼:1. CuAGs的泛癌失调——CNV是主要遗传变异形式(突变率低但CNV普遍);2. 亚型的生物-临床价值——亚型与免疫/基质/基因组稳定性及预后关联,例如COAD亚型1患者DFS更长(P<0.05,n=450);3. 癌症类别揭示的模式:Genomic disturbed类癌症(如STAD)中,铜死亡同时影响基因组和TME;Stromal remolded类癌症(如COAD)中,铜死亡通过重塑基质影响预后;4. Biomarker的临床潜力——DLAT是泛癌预后 biomarker,基于CuAGs的亚型可预测免疫治疗反应(如OV亚型1患者IPS值更高,对PD-1抑制剂更敏感,图2O)。
本研究首次在泛癌中系统解析了铜死亡标志物的特征,为铜死亡的临床转化提供了泛癌参考,尤其是基于CuAGs的亚型分类和癌症类别,为肿瘤精准治疗(如免疫治疗、铜离子载体治疗)提供了新的生物标志物和理论依据。