1. 领域背景与文献引入
文献英文标题:Molecular network of metabolic reprogramming and precision diagnosis and treatment of hepatocellular carcinoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肝细胞癌代谢重编程与精准诊疗。
肝细胞癌(HCC)是全球第六大常见癌症、第三大癌症死亡原因,亚洲太平洋地区占新发病例的71%,其中中国占42%。代谢重编程是癌症的核心特征之一,指肿瘤细胞为适应缺氧、营养匮乏等微环境,重塑葡萄糖、脂质、氨基酸代谢通路以维持生存、增殖及耐药性。这一概念可追溯至Warburg效应(肿瘤细胞在有氧条件下优先通过糖酵解产生能量),后续研究扩展至脂质(如从头脂肪合成)、氨基酸(如谷氨酰胺成瘾)代谢的改变。当前研究热点包括:代谢通路的调控网络(如PI3K/AKT/mTOR、Ras-Raf-MEK-ERK等信号通路与代谢酶的相互作用)、代谢重编程与临床表型(肿瘤异质性、转移潜能、免疫调控)的关联、代谢靶向治疗的开发。但未解决的核心问题仍有:代谢通路间的串扰机制(如葡萄糖与脂质代谢的交互)、代谢重编程促进免疫逃逸的具体机制、代谢靶点的临床转化(如缺乏经严格验证的代谢生物标志物)。
本文旨在整合肝癌代谢重编程的最新进展,构建代谢-信号-临床表型交互网络,系统评估代谢生物标志物的精准诊疗潜力,为肝癌个体化管理提供综合框架。
2. 文献综述解析
作者以“代谢通路类型”为分类维度,将现有研究分为葡萄糖代谢(糖酵解、三羧酸循环、戊糖磷酸途径、糖异生)、脂质代谢(游离脂肪酸、胆固醇、鞘脂)、氨基酸代谢(谷氨酰胺、半胱氨酸、支链氨基酸等)三大方向,梳理关键结论、优势及局限,并凸显本文创新价值。
现有研究核心结论
- 葡萄糖代谢:糖酵解关键酶(如己糖激酶2(HK2)、丙酮酸激酶M2(PKM2))过表达促进肝癌细胞糖酵解及增殖;三羧酸循环中间产物(如柠檬酸、琥珀酸)通过调控HIF-1α等信号通路影响肿瘤进展;戊糖磷酸途径(PPP)关键酶(如葡萄糖-6-磷酸脱氢酶(G6PD))提供NADPH减轻氧化应激,推动肿瘤生长;糖异生关键酶(如磷酸烯醇式丙酮酸羧激酶1(PCK1))缺失促进肿瘤干细胞特性。
- 脂质代谢:从头脂肪合成关键酶(如脂肪酸合酶(FASN)、乙酰辅酶A羧化酶1(ACC1))过表达增加脂肪积累,促进膜合成;胆固醇代谢异常(如SREBP2激活)通过调控YAP/TAZ信号通路促进增殖;鞘脂代谢(如鞘氨醇激酶1(SphK1)生成鞘氨醇-1-磷酸(S1P))激活PI3K/AKT通路,增强迁移能力。
- 氨基酸代谢:谷氨酰胺成瘾(谷氨酰胺酶(GLS1)过表达)为肿瘤提供能量及抗氧化物质;半胱氨酸代谢(如SLC7A11介导的胱氨酸摄取)维持谷胱甘肽水平,抵抗铁死亡;支链氨基酸(BCAA)代谢异常(如BCAT1过表达)通过mTOR通路促进增殖。
现有研究优势与局限
- 优势:明确了单一代谢通路的调控机制及与肿瘤表型的联系(如糖酵解与转移、脂质合成与耐药的关联)。
- 局限:对代谢通路间的串扰(如葡萄糖与脂质代谢的交互)、代谢重编程与免疫微环境的相互作用(如代谢产物对T细胞、巨噬细胞的调控)研究不足;多数代谢靶点仍处于预临床阶段,缺乏大规模临床验证。
本文创新价值
- 整合网络:构建了“代谢酶-信号通路-临床表型”的交互图,揭示多代谢通路的协同调控机制;
- 生物标志物评估:系统评估了代谢中间产物、限速酶及调控因子作为生物标志物的潜力;
- 精准诊疗框架:结合代谢成像(如18F-FDG PET/CT)、液体活检及联合疗法(代谢靶向与免疫治疗),为临床转化提供综合方案。
3. 研究思路总结与详细解析
本文为综述性研究,整体框架为“核心信号通路→分代谢通路解析→代谢串扰→精准诊疗”,核心科学问题是“肝癌代谢重编程的分子网络如何调控临床表型,以及如何基于此实现精准诊疗”,技术路线逻辑为“回顾现有研究→整合代谢通路调控机制→关联临床表型→评估生物标志物与治疗策略”。
3.1 核心信号通路调控网络解析
实验目的:明确调控肝癌代谢重编程的关键信号通路及作用机制。
方法细节:综述PI3K/AKT/mTOR、Ras-Raf-MEK-ERK-cMYC、LKB1-AMPK、Wnt/β-catenin、Hippo-YAP/TAZ等信号通路与代谢酶的相互作用。例如,PI3K/AKT/mTOR通路通过激活c-MYC上调HK2、PKM2表达,促进糖酵解;Ras-Raf-MEK-ERK通路通过磷酸化ERK促进c-MYC转录,增强糖酵解基因表达;AMPK通路通过抑制SREBP1减少脂质合成。
结果解读:这些信号通路形成动态网络,通过调控代谢酶的转录、翻译或修饰,重塑葡萄糖、脂质、氨基酸代谢通路,为肝癌细胞提供能量及生物合成前体。文中Figure 2展示了关键信号通路与代谢重编程的关联(
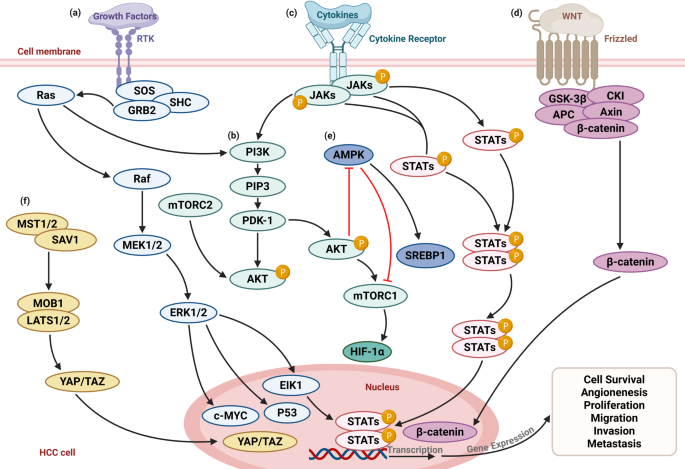
)。
实验所用关键产品:文献未提及具体实验产品,领域常规使用Western blot试剂盒(如Cell Signaling Technology的抗体)、qRT-PCR试剂盒(如Thermo Fisher的PrimeScript RT reagent Kit)等。
3.2 葡萄糖代谢重编程解析
实验目的:阐述肝癌葡萄糖代谢的调控机制。
方法细节:分述糖酵解、三羧酸循环、戊糖磷酸途径、糖异生的关键酶及调控因素。例如,HK2过表达由PI3K/AKT/mTOR、HIF-1α等通路调控,促进葡萄糖摄取及乳酸生成;柠檬酸通过线粒体柠檬酸载体(CIC)进入细胞质,促进从头脂肪合成;G6PD过表达由STAT3调控,提供NADPH减轻氧化应激;PCK1缺失通过O-GlcNAcylation增强CHK2活性,促进增殖。
结果解读:葡萄糖代谢重编程不仅为肝癌细胞提供能量,还通过中间产物(如乳酸、柠檬酸)调控信号通路及免疫微环境。文中Figure 3展示了葡萄糖代谢重编程的关键通路(
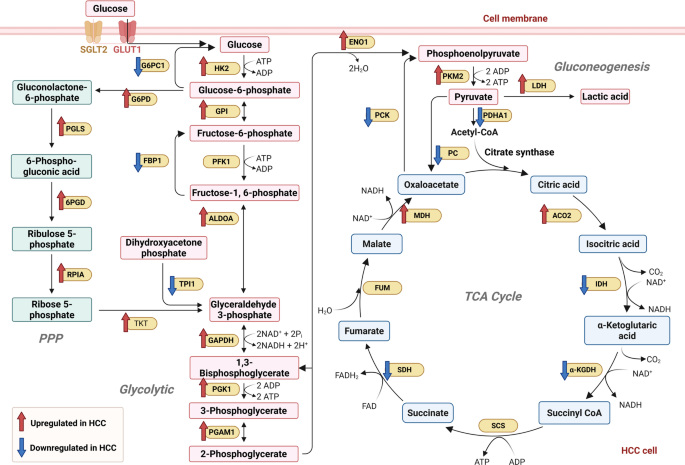
)。
实验所用关键产品:文献未提及具体实验产品,领域常规使用葡萄糖检测试剂盒(如Sigma-Aldrich的Glucose Assay Kit)、代谢组学分析平台(如Agilent的GC-MS)等。
3.3 脂质代谢重编程解析
实验目的:解析肝癌脂质代谢的改变及调控机制。
方法细节:分述游离脂肪酸、胆固醇、鞘脂代谢的关键酶及作用。例如,FASN、ACC1由c-MYC/SREBP1调控,促进从头脂肪合成;HMGCR由SREBP2调控,增加胆固醇酯积累;SphK1生成S1P,激活PI3K/AKT通路促进迁移。
结果解读:脂质代谢重编程为肝癌细胞提供膜合成原料,同时通过脂质信号调控增殖与耐药。文中Figure 4展示了脂质代谢重编程的关键通路(
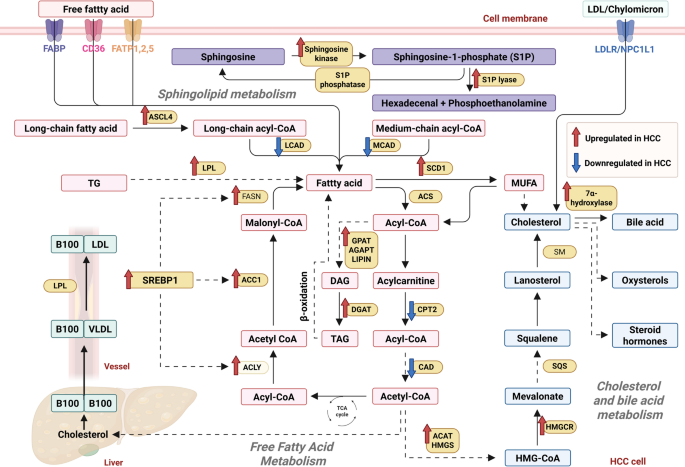
)。
实验所用关键产品:文献未提及具体实验产品,领域常规使用脂质提取试剂盒(如Thermo Fisher的Lipid Extraction Kit)、脂肪酸定量试剂盒(如Abcam的Fatty Acid Quantification Kit)等。
3.4 氨基酸代谢重编程解析
实验目的:探讨肝癌氨基酸代谢的异常及功能。
方法细节:分述谷氨酰胺、半胱氨酸、支链氨基酸代谢的关键酶及调控。例如,GLS1过表达促进谷氨酰胺分解,为TCA循环提供α-酮戊二酸;SLC7A11介导胱氨酸摄取,维持谷胱甘肽水平;BCAT1过表达通过mTOR通路促进增殖。
结果解读:氨基酸代谢重编程为肝癌细胞提供氮源及抗氧化物质,参与调控铁死亡、免疫逃逸等过程。文中Figure 5展示了氨基酸代谢重编程的关键通路(
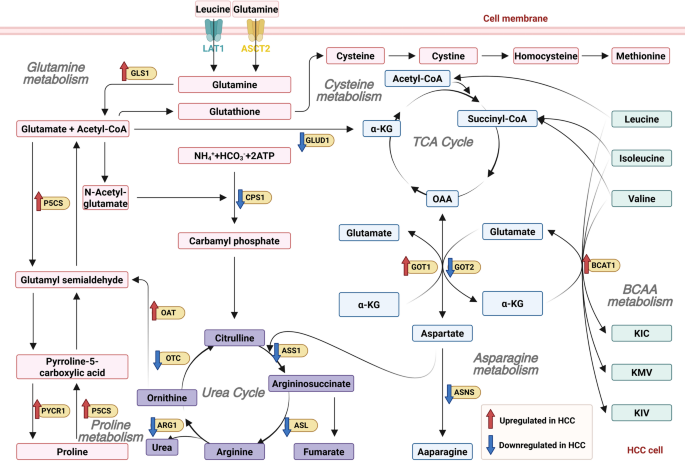
)。
实验所用关键产品:文献未提及具体实验产品,领域常规使用氨基酸分析仪(如Hitachi的L-8900)、谷胱甘肽检测试剂盒(如Cayman的Glutathione Assay Kit)等。
3.5 代谢通路串扰解析
实验目的:揭示不同代谢通路间的交互机制。
方法细节:阐述葡萄糖与脂质、葡萄糖与氨基酸、脂质与氨基酸代谢的串扰。例如,葡萄糖代谢通过STIM1-CaMKII-HIF-1α轴促进脂质合成;葡萄糖代谢中的GAPDH通过促进PHGDH转录连接丝氨酸代谢;脂质代谢中的CPT1A缺失通过积累支链氨基酸激活mTOR通路。
结果解读:代谢通路串扰增强了肝癌细胞的代谢可塑性,使其能适应营养波动。文中Figure 6展示了代谢通路间的串扰(
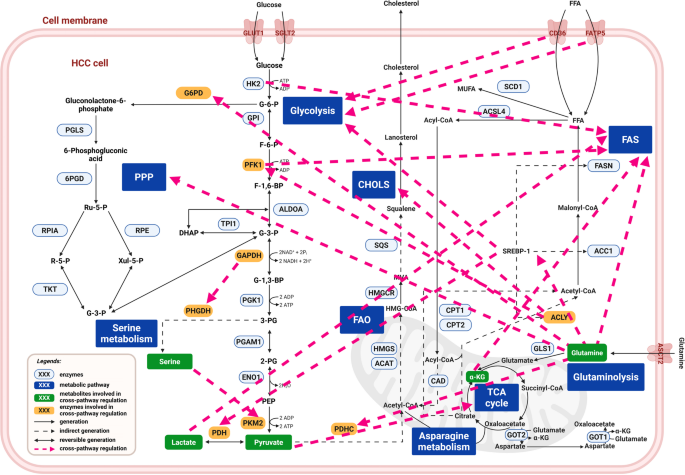
)。
实验所用关键产品:文献未提及具体实验产品,领域常规使用代谢流分析技术(如Seahorse的XF Extracellular Flux Analyzer)等。
3.6 精准诊疗策略解析
实验目的:评估基于代谢重编程的精准诊断与治疗策略。
方法细节:分述诊断技术(如18F-FDG PET/CT、代谢组学)、生物标志物(如HK2、GLS2)及治疗策略(如metformin、statins、GLS抑制剂)。例如,18F-FDG PET/CT通过追踪葡萄糖摄取诊断肝癌,AUC达80.6%;metformin通过AMPK抑制糖酵解,延长糖尿病肝癌患者生存期;GLS抑制剂(如CB-839)联合sorafenib增强疗效。
结果解读:代谢重编程为肝癌精准诊疗提供了多个靶点,联合疗法有望克服耐药。
实验所用关键产品:文献未提及具体实验产品,领域常规使用PET/CT设备(如Siemens的Biograph mCT)、靶向药物(如CB-839)等。
4. Biomarker研究及发现成果解析
文中涉及的Biomarker主要为代谢通路中的关键酶或调控因子,按代谢类型分类如下:
4.1 葡萄糖代谢相关Biomarker
- HK2(己糖激酶2):
- 类型:糖酵解限速酶;
- 筛选逻辑:TCGA数据库分析(肝癌组织HK2 mRNA水平高于正常组织)→细胞系验证(HK2过表达促进葡萄糖摄取及乳酸生成)→临床样本验证(免疫组化显示HK2过表达与poor prognosis相关);
- 验证方法:qRT-PCR、Western blot、免疫组化;
核心成果:作为肝癌预后标志物,过表达与肿瘤转移、耐药相关,可作为糖酵解靶向治疗的靶点(如抑制HK2可减少乳酸生成,增强免疫治疗 efficacy)。
PKM2(丙酮酸激酶M2):
- 类型:糖酵解限速酶;
- 筛选逻辑:细胞系(PKM2过表达促进糖酵解及增殖)→临床样本(免疫组化显示PKM2过表达与侵袭性相关);
- 验证方法:Western blot、免疫组化;
- 核心成果:参与调控肿瘤干细胞特性,是预测转移的生物标志物。
4.2 脂质代谢相关Biomarker
- FASN(脂肪酸合酶):
- 类型:从头脂肪合成关键酶;
- 筛选逻辑:细胞系(FASN过表达促进脂肪合成及耐药)→临床样本(免疫组化显示FASN过表达与poor survival相关);
- 验证方法:Western blot、免疫组化、代谢组学;
核心成果:作为耐药标志物,抑制FASN可恢复肝癌细胞对paclitaxel的敏感性。
ACSL4(长链酰基辅酶A合成酶4):
- 类型:游离脂肪酸代谢酶;
- 筛选逻辑:临床样本(ACSL4高表达与TACE术后复发相关)→细胞系(ACSL4过表达促进脂质合成);
- 验证方法:免疫组化、qRT-PCR;
- 核心成果:预测TACE疗效的生物标志物,高表达提示复发风险增加。
4.3 氨基酸代谢相关Biomarker
- GLS2(谷氨酰胺酶2):
- 类型:谷氨酰胺分解酶;
- 筛选逻辑:动物模型(GLS2过表达促进铁死亡,抑制肿瘤生长)→临床样本(免疫组化显示GLS2低表达与侵袭性相关);
- 验证方法:Western blot、免疫组化;
核心成果:作为抑癌标志物,低表达提示肿瘤侵袭性强,可作为铁死亡靶向治疗的靶点(如促进GLS2表达可诱导肿瘤细胞铁死亡)。
BCAT1(支链氨基酸转氨酶1):
- 类型:支链氨基酸代谢酶;
- 筛选逻辑:细胞系(BCAT1过表达降低顺铂敏感性)→临床样本(免疫组化显示BCAT1过表达与化疗耐药相关);
- 验证方法:Western blot、qRT-PCR;
- 核心成果:预测顺铂耐药的生物标志物,抑制BCAT1可增强化疗 efficacy。
总结
文中的代谢Biomarker多为代谢通路的关键酶,通过“数据库筛选→细胞系验证→临床样本验证”的逻辑链确定,其功能关联涉及肿瘤增殖、转移、耐药及预后,为肝癌的精准诊断(如早期检测、预后预测)及靶向治疗(如抑制糖酵解、脂肪合成)提供了重要依据。未来需进一步开展大规模临床研究,验证这些Biomarker的特异性与敏感性,推动其临床应用。
