1. 领域背景与文献引入
文献英文标题:RNA demethylase ALKBH5 promotes tumorigenesis of t (8;21) acute myeloid leukemia via ITPA m6A modification;发表期刊:Biomarker Research;影响因子:未公开;研究领域:t(8;21)急性髓系白血病(AML)的m6A甲基化调控机制及白血病干/起始细胞(LSCs/LICs)功能调控。
t(8;21)是AML中常见的染色体易位亚型,尽管被归为“好风险”类别,但仅约60%患者在诊断后存活超过5年,复发和化疗耐药仍是未解决的核心问题。近年来,N6-甲基腺苷(m6A)RNA甲基化修饰作为可逆表观遗传调控方式,在白血病发生中的作用备受关注。RNA去甲基化酶ALKBH5可通过调控靶基因m6A水平影响肿瘤细胞增殖、凋亡及干细胞自我更新,其在AML中的促癌作用已被报道(如调控TACC3或AXL),但在t(8;21)AML中的具体分子机制、临床意义及上游调控因素尚未阐明。此外,LSCs/LICs是AML复发和耐药的根源,其自我更新能力与转录因子密切相关。TCF15作为参与造血干细胞(HSC)静息和长期自我更新的转录因子,其在AML中的功能及对ALKBH5的调控作用仍不清楚。
针对“ALKBH5在t(8;21)AML中的分子机制及临床意义”“TCF15对ALKBH5的转录调控作用”两个核心问题,本研究通过整合临床样本分析、细胞功能实验、动物模型及多组学技术,揭示了TCF15/ALKBH5/ITPA轴在t(8;21)AML发生中的关键作用,为该亚型AML的靶向治疗提供了新理论依据。
2. 文献综述解析
作者围绕“m6A修饰与ALKBH5的功能”“LSCs/LICs的调控”“转录因子TCF15的作用”三个维度综述现有研究,旨在明确ALKBH5在t(8;21)AML中的研究空白。
现有研究的关键结论:ALKBH5作为m6A去甲基化酶,在乳腺癌、肺癌等多种癌症中通过调控靶基因m6A水平影响细胞增殖、侵袭及凋亡;在AML中,ALKBH5可促进白血病发生,但对正常造血无显著影响。LSCs/LICs因具有异常自我更新能力,是AML复发和耐药的关键驱动因素。TCF15在HSC的静息状态维持和长期自我更新中发挥重要作用,但在AML中的功能及调控机制尚未报道。
现有研究的局限性:尽管ALKBH5在AML中的作用已有研究,但针对t(8;21)这一特定亚型的机制研究缺失;ALKBH5在t(8;21)AML中的上游转录调控因素(如TCF15)及下游功能靶基因(非TACC3/AXL)尚不明确;TCF15在LSCs/LICs中的作用及与ALKBH5的关系未阐明。
本研究的创新价值:首次揭示TCF15作为ALKBH5的上游转录因子,通过调控ALKBH5启动子活性促进其表达;明确ITPA是ALKBH5在t(8;21)AML中的功能靶基因,ALKBH5通过去甲基化ITPA mRNA增加其稳定性;建立了“TCF15→ALKBH5→ITPA”的调控轴,解释了t(8;21)AML中ALKBH5高表达的原因及促癌机制。
3. 研究思路总结与详细解析
本研究以“ALKBH5在t(8;21)AML中的作用及机制”为核心,采用“表达分析→功能验证→靶点筛选→机制探究→轴功能验证”的闭环技术路线,整合临床样本、细胞模型、动物模型及多组学方法,系统解析TCF15/ALKBH5/ITPA轴的功能。
3.1 ALKBH5在t(8;21)AML中的表达及临床意义验证
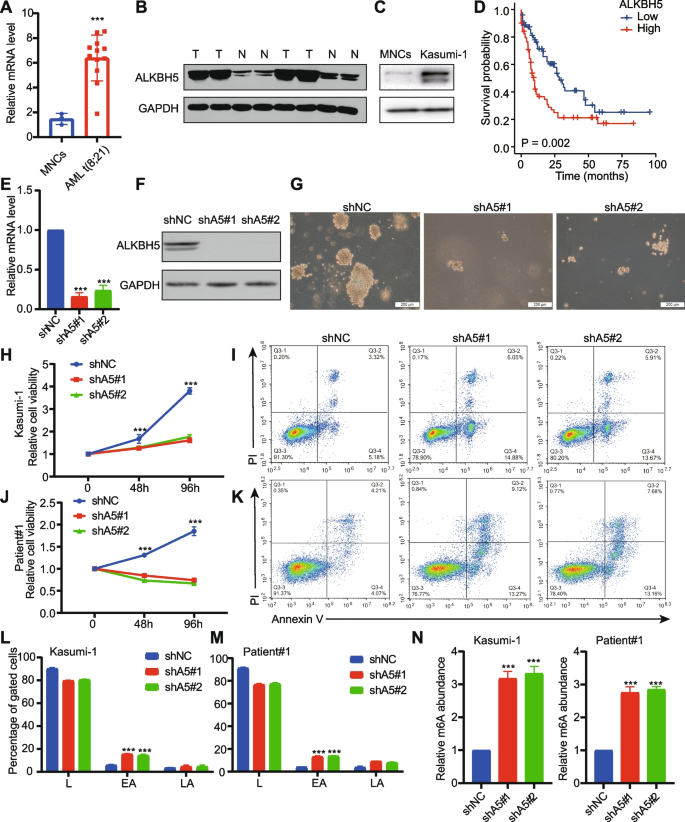
实验目的:检测ALKBH5在t(8;21)AML患者及细胞系中的表达水平,分析其与患者预后的关系。
方法细节:收集12例t(8;21)AML患者及3例正常对照的骨髓单个核细胞(BMMNCs),通过qRT-PCR和蛋白质免疫印迹(western blot)检测ALKBH5的mRNA及蛋白表达;采用t(8;21)AML细胞系Kasumi-1验证表达差异;利用TCGA-LAML队列分析ALKBH5表达与总生存期(OS)的关系。
结果解读:t(8;21)AML患者BMMNCs中ALKBH5的mRNA水平显著高于正常对照(n=12 vs n=3,P<0.05),蛋白水平亦呈现高表达;Kasumi-1细胞中ALKBH5蛋白水平高于正常BMMNCs;TCGA-LAML队列中,高ALKBH5表达患者的OS显著短于低表达患者(P<0.05,以ALKBH5表达中位数为cutoff)。
产品关联:实验所用关键产品包括Abcam的ALKBH5抗体、Takara的qRT-PCR试剂(Primescript RT Reagent、SYBR®Premix Ex Taq™)、Keygentec的总蛋白提取试剂盒、Pierce的BCA蛋白定量试剂盒、Cell Signaling Technology的二抗。
3.2 ALKBH5对t(8;21)AML细胞及动物模型的功能验证
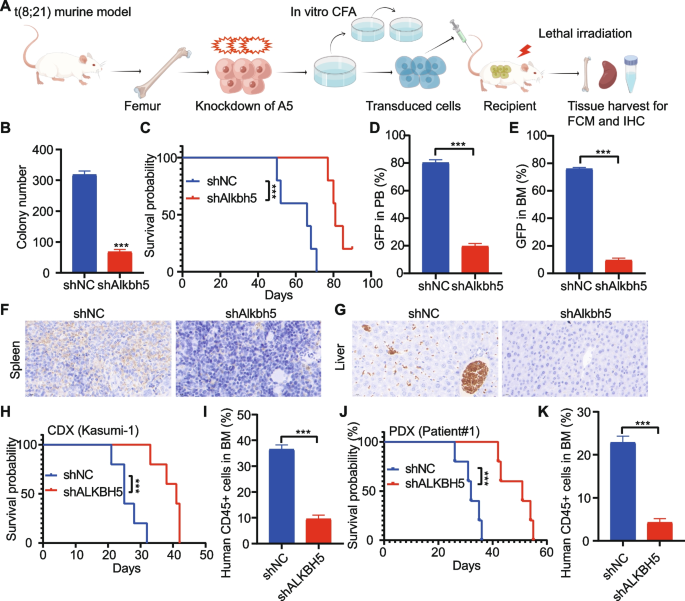
实验目的:验证ALKBH5对t(8;21)AML细胞增殖、凋亡及体内白血病发生的影响。
方法细节:构建ALKBH5 shRNA敲低的Kasumi-1细胞模型(shALKBH5#1、shALKBH5#2),通过CCK-8实验检测细胞增殖、集落形成实验检测自我更新能力、流式细胞术(Annexin V/PI双染)检测凋亡;建立t(8;21)小鼠模型(RUNX1-RUNX1T1+KITN822K突变)、人源肿瘤异种移植(CDX)模型(Kasumi-1细胞移植NSG小鼠)及患者来源异种移植(PDX)模型(患者来源细胞移植NSG小鼠),检测敲低ALKBH5对体内白血病进展的影响。
结果解读:敲低ALKBH5显著抑制Kasumi-1细胞增殖(48h增殖率下降约30%,n=3,P<0.05)、减少集落形成数(第7天集落数减少约40%,n=3,P<0.05),并促进细胞凋亡(早期凋亡率从5%升至15%,n=3,P<0.05);在t(8;21)小鼠模型中,敲低Alkbh5显著延长受体小鼠的OS(中位OS:shNC组35天vs shAlkbh5组50天,n=5,P<0.05),抑制白血病细胞在骨髓(BM)及外周血(PB)中的植入,减少脾脏、肝脏的白血病浸润;CDX模型中,敲低ALKBH5的Kasumi-1细胞移植小鼠的OS显著延长(shNC组40天vs shALKBH5组60天,n=5,P<0.05),骨髓中人类CD45+细胞比例降低;PDX模型中,敲低ALKBH5的患者来源细胞移植小鼠的OS延长(shNC组38天vs shALKBH5组55天,n=5,P<0.05),骨髓中CD45+细胞比例降低。
产品关联:实验所用关键产品包括Dojindo的CCK-8试剂盒、KeyGEN BioTECH的Annexin V-FITC/PI凋亡检测试剂盒、StemCell Technologies的MethoCult H4434培养基、eBioscience的流式染色缓冲液及抗小鼠CD16/32抗体、BD FACS FortessaX-20流式细胞仪。
3.3 ALKBH5靶基因ITPA的筛选与功能验证
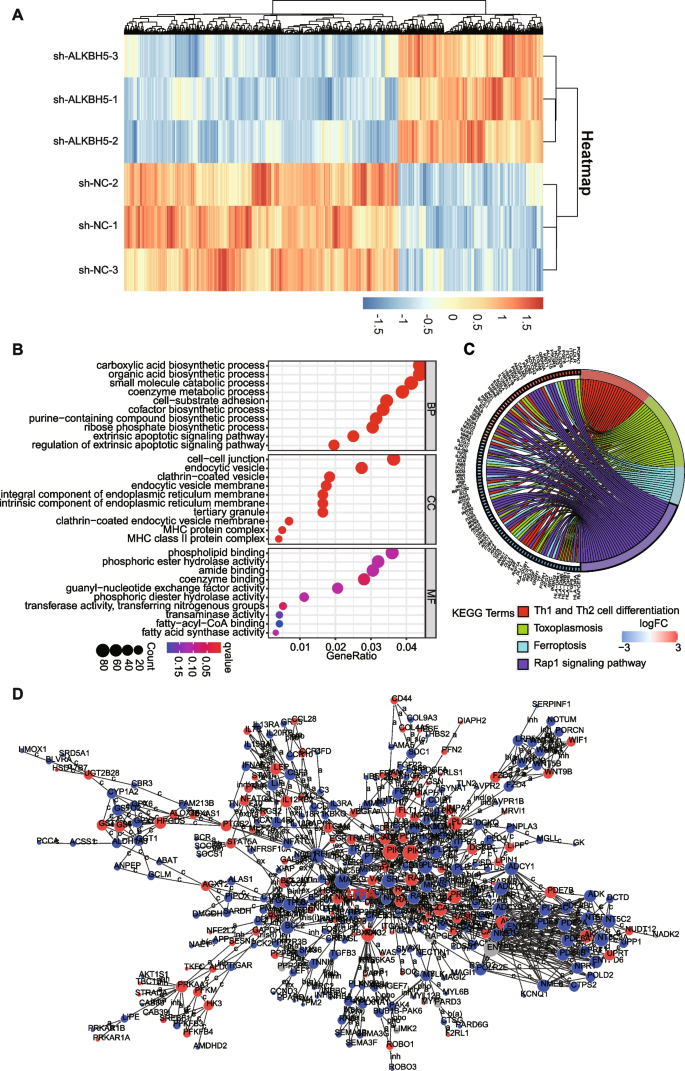
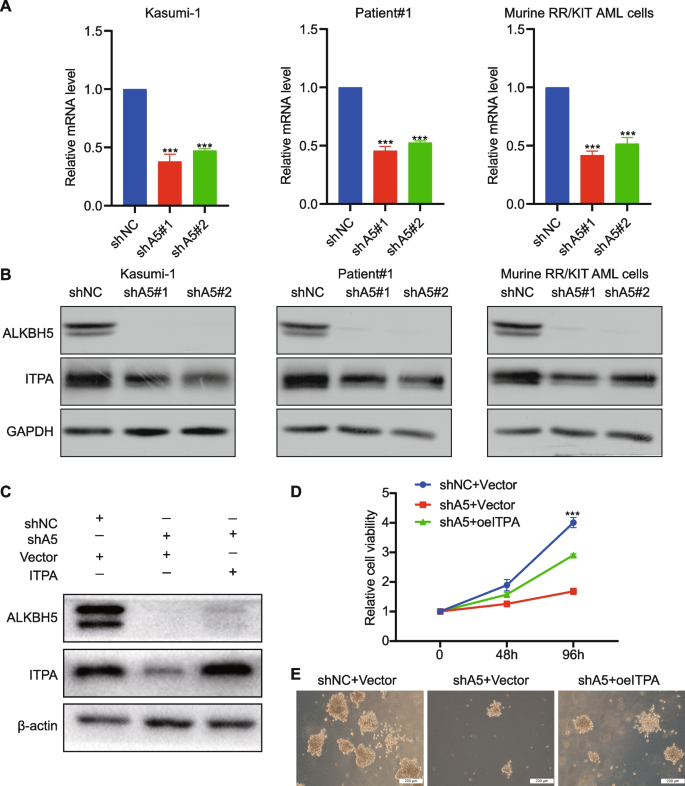
实验目的:筛选ALKBH5在t(8;21)AML中的功能靶基因,并验证其对ALKBH5功能的介导作用。
方法细节:对敲低ALKBH5的Kasumi-1细胞进行RNA测序(RNA-seq),筛选差异表达基因(DEGs);通过GO和KEGG富集分析DEGs的功能通路;结合TCGA-LAML队列的共表达分析及预后分析,确定候选靶基因ITPA;检测敲低ALKBH5后,Kasumi-1细胞、患者来源细胞及小鼠RR/KIT AML细胞中ITPA的mRNA及蛋白表达;构建“ALKBH5敲低+ITPA过表达”的rescue细胞模型,通过CCK-8、集落形成实验验证细胞增殖能力。
结果解读:RNA-seq共鉴定2326个DEGs(1533个下调,793个上调),GO富集分析显示DEGs参与凋亡调控等通路;TCGA-LAML队列中,ITPA与ALKBH5呈正相关(R=0.3,P<0.05),且高ITPA表达患者的OS显著缩短(P<0.05);敲低ALKBH5后,Kasumi-1细胞、患者来源细胞及小鼠RR/KIT AML细胞中ITPA的mRNA及蛋白水平均显著降低(P<0.05);rescue实验显示,过表达ITPA可显著恢复敲低ALKBH5对Kasumi-1细胞增殖(shALKBH5+ITPA组增殖率较shALKBH5+空载体组升高约40%,n=3,P<0.05)及集落形成(集落数增加约50%,n=3,P<0.05)的抑制作用。
产品关联:RNA-seq由Personalbio Biotechnology完成,实验所用关键产品包括GenePharma的shRNA及过表达载体、Lipofectamine™ 3000转染试剂、Dojindo的CCK-8试剂盒、StemCell Technologies的MethoCult H4434培养基。
3.4 ALKBH5调控ITPA的m6A机制探究
实验目的:探究ALKBH5调控ITPA的分子机制(是否通过m6A去甲基化作用)。
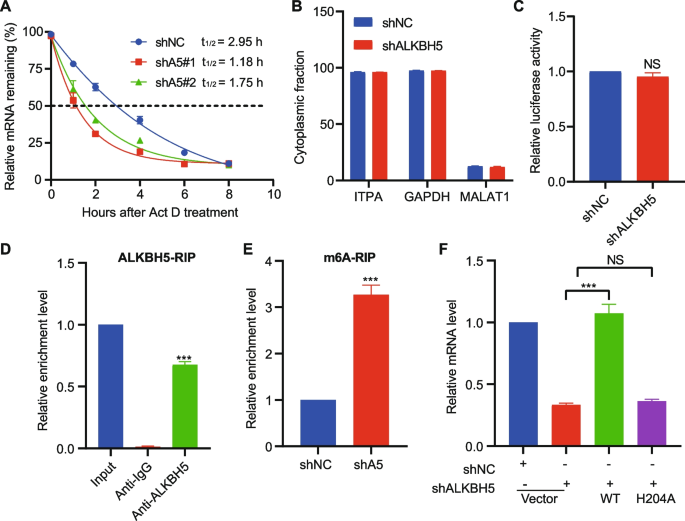
方法细节:通过RNA免疫沉淀(RIP)结合qPCR验证ALKBH5与ITPA mRNA的结合;采用甲基化RNA免疫沉淀(MeRIP)结合qPCR检测敲低ALKBH5后ITPA mRNA的m6A水平;通过放线菌素D处理(5μg/ml)检测ITPA mRNA的稳定性;构建野生型ALKBH5(wt-ALKBH5)及催化失活突变体(ALKBH5 H204A)的过表达载体,转染敲低ALKBH5的Kasumi-1细胞,检测ITPA的mRNA表达。
结果解读:RIP-qPCR显示,抗ALKBH5抗体对ITPA mRNA的富集效率显著高于IgG抗体(fold enrichment=3.2,n=3,P<0.05);敲低ALKBH5后,ITPA mRNA的m6A水平显著升高(fold change=1.8,n=3,P<0.05);放线菌素D处理后,敲低ALKBH5的Kasumi-1细胞中ITPA mRNA的半衰期从4h缩短至2h(P<0.05);过表达wt-ALKBH5可恢复ITPA的mRNA水平,而ALKBH5 H204A突变体无此作用。
产品关联:实验所用关键产品包括Millipore的Magna RIP™ kit及Magna MeRIP m6A Kit、Sigma-Aldrich的放线菌素D、Promega的双荧光素酶报告系统、QIAGEN的RNeasy试剂盒。
3.5 TCF15对ALKBH5的转录调控及轴功能验证
实验目的:探究ALKBH5的上游转录调控因子TCF15,并验证TCF15/ALKBH5/ITPA轴的功能。
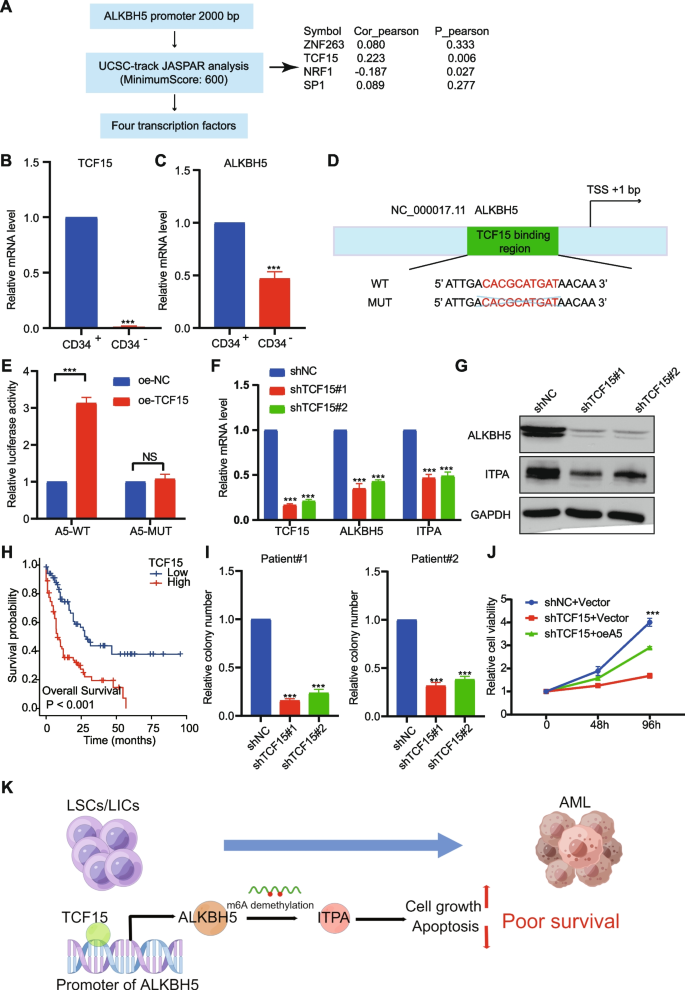
方法细节:通过UCSC JASPAR数据库分析ALKBH5启动子区的转录因子结合位点,筛选候选因子TCF15;检测t(8;21)AML患者CD34+ LSCs/LICs与CD34- bulk AML细胞中TCF15、ALKBH5的mRNA表达;构建ALKBH5启动子野生型及TCF15结合位点突变型的荧光素酶报告质粒,转染CD34+ LSCs/LICs,检测荧光素酶活性;构建TCF15 shRNA敲低的LSCs模型,检测ALKBH5、ITPA的mRNA及蛋白表达;构建“TCF15敲低+ALKBH5过表达”的rescue细胞模型,通过集落形成实验验证细胞自我更新能力。
结果解读:TCF15在CD34+ LSCs/LICs中的mRNA水平显著高于CD34- bulk AML细胞(n=5,P<0.05),ALKBH5在CD34+ LSCs/LICs中亦呈高表达;荧光素酶报告实验显示,TCF15过表达可增强ALKBH5启动子的活性(fold change=2.5,n=3,P<0.05),而TCF15结合位点突变后活性丧失;敲低TCF15后,LSCs中ALKBH5、ITPA的mRNA及蛋白水平显著降低(P<0.05);rescue实验显示,过表达ALKBH5可恢复敲低TCF15对LSCs集落形成的抑制作用(集落数增加约60%,n=3,P<0.05)。
产品关联:实验所用关键产品包括GeneScript的荧光素酶报告质粒、eBioscience的CD34抗体、StemCell Technologies的MethoCult H4434培养基。
4. Biomarker研究及发现成果解析
本研究围绕“ALKBH5、ITPA作为t(8;21)AML的Biomarker”展开,通过临床样本分析、多组学验证及功能实验,明确其作为诊断、预后Biomarker的潜力及调控机制。
Biomarker定位与筛选逻辑
本研究涉及的Biomarker包括“RNA去甲基化酶ALKBH5”“嘌呤核苷酸代谢酶ITPA”“转录因子TCF15”,其筛选/验证逻辑为“临床样本表达分析→功能实验验证→多组学机制探究→预后价值评估”:ALKBH5通过患者样本及细胞系验证表达差异,TCGA队列验证预后价值;ITPA通过RNA-seq筛选,RIP/MeRIP验证m6A机制,rescue实验验证功能介导;TCF15通过启动子分析验证转录调控,敲低实验验证轴功能。
研究过程与核心数据
ALKBH5的来源为t(8;21)AML患者BMMNCs及细胞系,通过qRT-PCR、western blot验证其mRNA及蛋白水平显著高于正常对照(n=12 vs n=3,P<0.05);TCGA-LAML队列中,高ALKBH5表达患者的OS显著短于低表达患者(P<0.05)。ITPA的来源为ALKBH5的靶基因,RIP-qPCR显示ALKBH5与ITPA mRNA显著结合(fold enrichment=3.2,n=3,P<0.05);MeRIP-qPCR显示敲低ALKBH5后ITPA mRNA的m6A水平升高1.8倍(n=3,P<0.05);rescue实验显示ITPA可恢复ALKBH5敲低的抑制作用(增殖率升高40%,n=3,P<0.05)。TCF15的来源为CD34+ LSCs/LICs,其mRNA水平显著高于CD34- bulk AML细胞(n=5,P<0.05);荧光素酶报告实验显示TCF15可增强ALKBH5启动子活性2.5倍(n=3,P<0.05);敲低TCF15后,ALKBH5、ITPA的mRNA及蛋白水平显著降低(P<0.05)。
核心成果与创新性
- ALKBH5作为t(8;21)AML的促癌Biomarker:其高表达与患者不良预后相关,通过m6A去甲基化作用增加ITPA mRNA稳定性,促进细胞增殖。
- ITPA作为ALKBH5的功能靶标:其表达水平与ALKBH5正相关,高表达患者OS缩短(TCGA队列,P<0.05),是ALKBH5促癌功能的关键介导因子。
- TCF15/ALKBH5/ITPA轴的发现:TCF15作为ALKBH5的上游转录因子,仅在CD34+ LSCs/LICs中表达,通过促进ALKBH5启动子活性调控其表达,最终驱动t(8;21)AML发生。
本研究首次揭示了TCF15对ALKBH5的转录调控机制及ITPA的m6A修饰功能,为t(8;21)AML的靶向治疗(如抑制ALKBH5的去甲基化活性、阻断TCF15的转录调控)提供了新靶点,具有重要的临床转化价值。