1. 领域背景与文献引入
文献英文标题:Circulating extracellular vesicles during pregnancy in women with type 1 diabetes: a secondary analysis of the CONCEPTT trial;发表期刊:Biomarker Research;影响因子:未公开;研究领域:妊娠合并1型糖尿病的细胞外囊泡生物标志物研究。
妊娠合并1型糖尿病时,母体血管健康是妊娠结局的关键决定因素,内皮损伤或功能障碍可能在母婴急性及远期健康结局中发挥因果作用。现有研究表明,可溶性细胞间黏附分子-1(sICAM-1)、可溶性血管细胞黏附分子-1(sVCAM-1)等血管损伤生物标志物升高与早产相关,而抗血管生成因子sFlt-1升高则与早晚期早产、低出生体重及子痫前期风险增加相关。然而,细胞外囊泡(EVs)作为新型血管健康生物标志物,其在妊娠合并1型糖尿病女性中的循环水平、与血糖指标的关联及对妊娠结局的预测价值尚未明确——现有研究多集中于正常妊娠或子痫前期,未探讨1型糖尿病妊娠中EVs与血糖变异性的关系,也未评估连续血糖监测(CGM)对EVs的影响,这为该领域留下了研究空白。
本研究旨在量化妊娠合并1型糖尿病女性的循环EVs水平,探讨其与CGM指标、血压及妊娠结局的关联,评估EVs作为该人群个性化医疗生物标志物的潜力,为改善母婴结局提供新的理论依据。
2. 文献综述解析
作者对现有研究的评述围绕三个核心维度展开:一是传统血管损伤生物标志物与妊娠结局的关联——现有研究已证实sICAM-1、sFlt-1等标志物与不良妊娠结局相关,但这些标志物的特异性和敏感性有限,难以满足个性化医疗需求;二是EVs作为血管健康生物标志物的研究——内皮EVs已被证实与心血管事件风险独立相关,糖尿病患者(包括1型和2型)的循环EVs(尤其是内皮、血小板来源)水平显著升高,且血糖控制改善后EVs水平降低;三是EVs在妊娠中的研究空白——现有研究未针对1型糖尿病妊娠人群,未明确EVs与血糖变异性的关联,也未验证EVs对妊娠结局的预测价值。
现有研究的关键结论包括:EVs是反映血管损伤的敏感生物标志物,糖尿病患者的EVs水平与血糖状态相关;局限性则在于缺乏对1型糖尿病妊娠人群的针对性研究,无法为该人群的EVs应用提供依据。本研究的创新点在于首次在1型糖尿病妊娠人群中系统分析EVs与血糖变异性、妊娠结局的关联,同时探讨CGM对EVs的影响,为EVs作为该人群个性化医疗的新型生物标志物提供了初步证据。
3. 研究思路总结与详细解析
本研究的整体框架为:以“CONCEPTT试验”的血浆样本为基础,通过流式细胞术量化不同妊娠时期的循环EVs水平,采用重复测量相关分析探讨EVs与血糖、血压的关联,利用逻辑回归评估EVs与妊娠结局的关联,最终明确EVs作为1型糖尿病妊娠不良结局生物标志物的价值。核心科学问题是循环EVs是否可作为妊娠合并1型糖尿病女性不良妊娠结局的预测生物标志物,技术路线遵循“样本获取→EVs分离与定量→关联分析→结局验证”的闭环逻辑。
3.1 研究样本来源与伦理验证
实验目的是获取符合伦理要求的研究样本,确保数据可靠性。方法细节为利用“Continuous Glucose Monitoring in Pregnant Women with Type 1 Diabetes(CONCEPTT)”试验的生物样本库,纳入163例妊娠合并1型糖尿病女性的血浆样本(采集时间点:基线4-12周、24周、34周);研究已获得Mount Sinai研究伦理委员会(ID#: 17-0066-E)和Ottawa医院研究伦理委员会(ID#: 20170658-01 H)批准,样本分析采用盲法。结果显示,纳入样本的基线特征(如年龄、HbA1c、血压)无显著差异,确保后续分析的可比性。实验所用关键产品:文献未提及具体品牌,领域常规使用BioLegend的流式抗体(如抗CD41-APC、抗CD144-PE)、Beckman Coulter的CytoFLEX S流式细胞仪。
3.2 EVs的分离与免疫标记
实验目的是从血浆中分离大EVs(L-EVs,直径100-1000nm)并标记亚群,区分血小板、内皮及白细胞来源的EVs。方法细节为:将血浆样本在4℃下以12,000×g离心2分钟(去除血小板),取上清以20,000×g离心20分钟获取L-EVs沉淀,用Annexin V结合缓冲液重悬;血小板EVs标记采用抗CD41-APC(1:100)+Annexin V-FITC(1:50),内皮/白细胞EVs标记采用抗CD144-PE(1:100)+抗CD45-BV421(1:25)+Annexin V-FITC(1:50);标记后再次离心并重悬用于流式分析。结果显示,该方法可有效分离并标记不同来源的EVs,确保定量准确性。
3.3 EVs的流式细胞术定量
实验目的是定量不同妊娠时期的循环EVs水平,区分EVs亚群。方法细节为使用Beckman Coulter CytoFLEX S流式细胞仪,通过ApogeeMix beads设置100-1000nm大小门,计数Annexin V阳性(Annexin V+)的EVs——其中Annexin V+CD41+为血小板EVs,Annexin V+CD144+为内皮EVs,Annexin V+CD45+为白细胞EVs。结果显示,不同妊娠时期的内皮(P=0.43)、白细胞(P=0.65)、血小板(P=0.82)及总EVs(P=0.58)水平无显著差异,提示EVs在妊娠合并1型糖尿病中相对稳定。
3.4 EVs与血糖、血压及妊娠结局的关联分析
实验目的是探讨EVs与血糖指标、血压的关联,评估EVs对妊娠结局的预测价值。方法细节为:采用重复测量相关分析EVs与HbA1c、平均血糖、血糖变异性(MAGE、SD、CV)及血压的关联;采用逻辑回归(单变量及调整HbA1c、血压后的多变量模型)评估EVs与妊娠结局(如NICU入院、呼吸窘迫、高胆红素血症)的关联。
结果显示:血小板EVs与血糖高于目标范围时间(TAR)、血糖变异性(SD、MAGE)呈负相关,与血糖在目标范围时间(TIR)呈正相关(P<0.05);内皮EVs与MAGE呈弱正相关(P<0.05);白细胞EVs与收缩压、舒张压呈正相关(P<0.05)。CGM组与自我血糖监测(SMBG)组在34周的EVs水平无显著差异(图1)。单变量模型中,基线内皮EVs高水平与NICU入院(OR:2.06,95%CI 1.03-4.10)、呼吸窘迫需通气(OR:4.98,95%CI 1.04-23.92)相关;调整HbA1c和血压后,内皮EVs仍与NICU入院(OR:2.56,95%CI 1.10-5.94)、高胆红素血症相关,血小板EVs与NICU入院(OR:2.18,95%CI 1.04-4.57)、高胆红素血症(OR:2.61,95%CI 1.11-6.12)相关(图2、图3)。
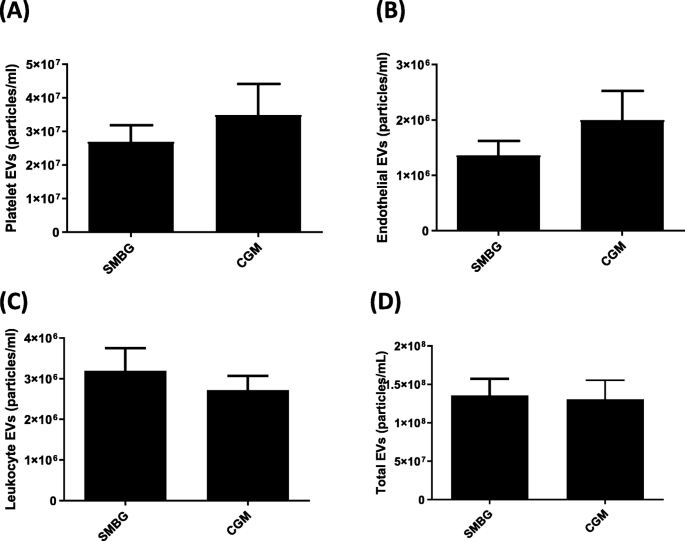
(图1:CGM对34周EVs水平的影响,CGM组与SMBG组无显著差异)
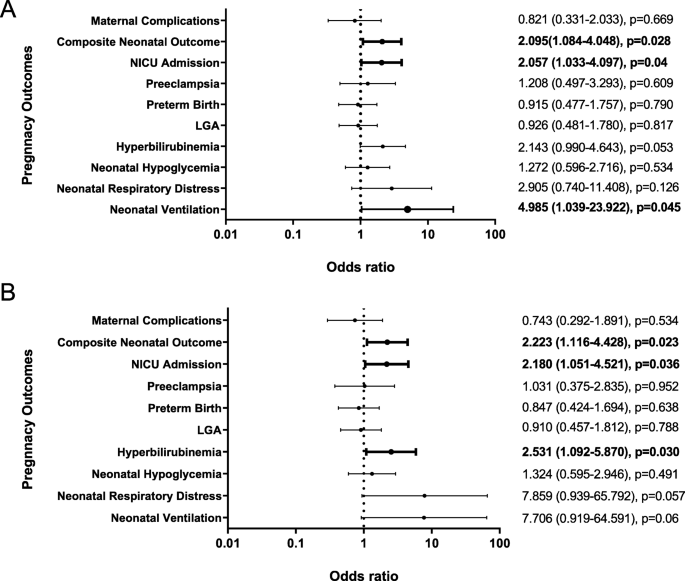
(图2:基线内皮EVs与妊娠结局的关联,调整后仍与NICU入院、高胆红素血症相关)
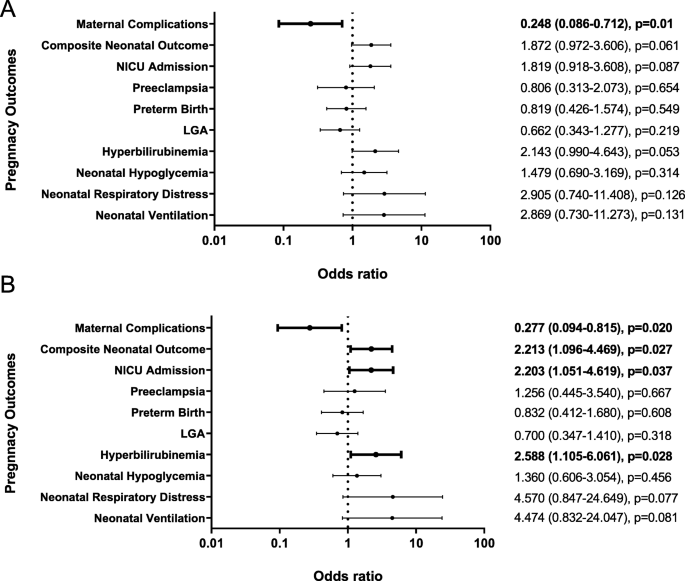
(图3:基线血小板EVs与妊娠结局的关联,调整后与NICU入院、高胆红素血症相关)
4. Biomarker研究及发现成果解析
本研究的核心Biomarker为循环内皮EVs(Annexin V+CD144+)和血小板EVs(Annexin V+CD41+),其筛选逻辑基于“EVs是血管损伤生物标志物”的现有研究,验证逻辑遵循“血浆样本分离→流式定量→与血糖关联→与妊娠结局关联”的完整链条。
Biomarker研究过程
Biomarker来源为CONCEPTT试验中妊娠合并1型糖尿病女性的血浆样本(基线、24周、34周);验证方法为流式细胞术定量EVs水平,结合重复测量相关分析(与血糖、血压关联)和逻辑回归(与妊娠结局关联);特异性与敏感性通过逻辑回归模型评估——基线内皮EVs预测NICU入院的调整后OR值为2.56(95%CI 1.10-5.94),预测呼吸窘迫需通气的OR值为4.98(95%CI 1.04-23.92);血小板EVs预测NICU入院的OR值为2.18(95%CI 1.04-4.57),预测高胆红素血症的OR值为2.61(95%CI 1.11-6.12)(样本量n=163,P<0.05)。
核心成果提炼
- 功能关联:循环内皮EVs、血小板EVs的基线高水平与妊娠合并1型糖尿病女性的不良neonatal结局显著相关——内皮EVs与NICU入院、呼吸窘迫需通气、高胆红素血症相关,血小板EVs与NICU入院、高胆红素血症相关。
- 创新性:首次在1型糖尿病妊娠人群中证实EVs与血糖变异性(如MAGE、SD)相关(血小板EVs与血糖变异性负相关),提示EVs可反映血糖波动对血管的损伤;同时验证了EVs对不良妊娠结局的预测价值,为该人群的个性化医疗提供了新型生物标志物。
- 统计学可靠性:所有关联分析的P值均<0.05,样本量为163例,确保结果的稳健性。
本研究的结论为:妊娠合并1型糖尿病女性的基线EVs水平可预测不良neonatal结局,EVs有望成为该人群个性化医疗的新型生物标志物,为早期干预改善母婴结局提供了理论依据。