1. 领域背景与文献引入
文献英文标题:Manipulation of cancer cell pyroptosis for therapeutic approaches: challenges and opportunities;发表期刊:Biomarker Research;影响因子:5.8(2024年);研究领域:肿瘤免疫学/细胞死亡机制。
焦亡是一种由gasdermin家族蛋白介导的调节性坏死,2015年Shi等首次报道GSDMD作为焦亡的关键执行者,开启了该领域的研究热潮。随后,gasdermin家族其他成员(如GSDME、GSDMB、GSDMC)的功能被逐步阐明,焦亡的“两阶段模型”(亚细胞透化与细胞裂解)及调控机制(炎症小体激活、caspase切割、颗粒酶作用)成为核心热点。当前,癌症细胞焦亡的研究聚焦于其分子机制、与抗肿瘤免疫的关系及临床治疗应用,但仍存在诸多未解决的问题:癌症细胞焦亡的细胞类型特异性机制尚未完全明确,临床转化中如何平衡其免疫激活与促肿瘤效应,以及缺乏有效的生物标志物预测治疗反应。本文旨在系统整合癌症细胞焦亡的基础研究与临床进展,为该领域的转化应用提供全面框架。
2. 文献综述解析
作者对现有研究的分类维度包括:焦亡的动态过程、免疫细胞与癌症细胞焦亡的机制差异、癌症细胞焦亡与抗肿瘤免疫的关系、治疗策略及研究挑战。
现有研究的关键结论:焦亡是分阶段的可逆-不可逆过程——亚细胞透化阶段由gasdermin-N结构域穿孔细胞器膜(如线粒体、溶酶体),可通过ESCRT-III machinery修复;细胞裂解阶段由NINJ1介导,导致不可逆死亡。免疫细胞焦亡主要依赖炎症小体激活caspase-1/11切割GSDMD,而癌症细胞焦亡多由凋亡诱导剂(化疗药物、缺氧微环境、颗粒酶)激活caspase-3/8或颗粒酶切割GSDME/GSDMC/GSDMB。癌症细胞焦亡的“双刃剑”作用显著:急性焦亡通过释放损伤相关分子模式(DAMPs)(如HMGB1)激活树突状细胞,增强细胞毒性T细胞浸润;慢性焦亡则通过持续炎症诱导免疫抑制,促进肿瘤进展。
现有研究的局限性:机制研究存在争议(如GZMB切割GSDME是否依赖caspase-3)、临床转化数据匮乏、焦亡与其他细胞死亡途径的交互作用未明确。本文的创新价值在于首次系统整合癌症细胞焦亡的全链条研究,明确其“双刃剑”模式,并提出临床转化的关键方向,填补了领域空白。
3. 研究思路总结与详细解析
作者以“焦亡基础→机制差异→免疫作用→治疗策略→挑战机遇”为逻辑链,逐步展开论述,覆盖从基础到临床的全维度内容。
3.1 焦亡过程的两阶段解析
实验目的:明确焦亡的动态调控机制。
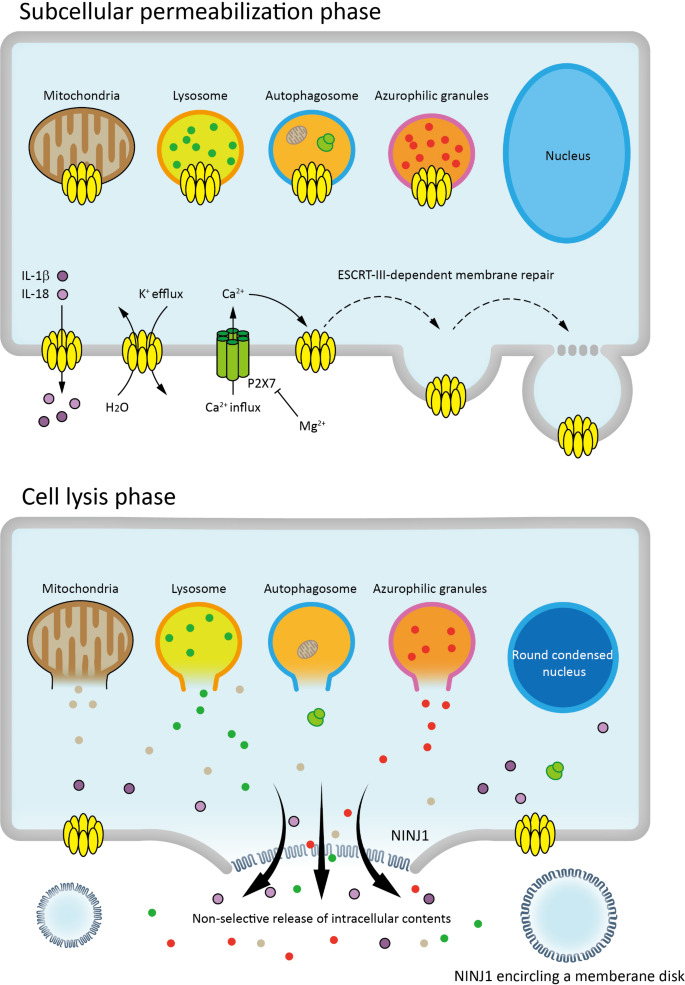
方法细节:整合多项关键研究——Rogers等通过细胞实验证实GSDMD/GSDME-N结构域可透化线粒体膜,增强caspase-3激活;Huang等通过动物实验发现线粒体DNA释放激活cGAS-STING通路;Rühl等证实ESCRT-III machinery可修复GSDMD介导的膜损伤;Kayagaki等通过基因敲除模型明确NINJ1是细胞裂解的关键分子。
结果解读:焦亡分为可逆的亚细胞透化阶段(细胞器膜穿孔、炎症因子释放)和不可逆的细胞裂解阶段(质膜破裂、内容物释放)。亚细胞透化阶段的修复机制为临床干预提供了潜在靶点。
实验所用关键产品:文献未提及具体产品,领域常规使用caspase抑制剂(如Z-VAD-FMK)、gasdermin抗体(如anti-GSDMD)。
3.2 免疫细胞与癌症细胞焦亡的机制差异
实验目的:比较两类细胞焦亡的调控逻辑。
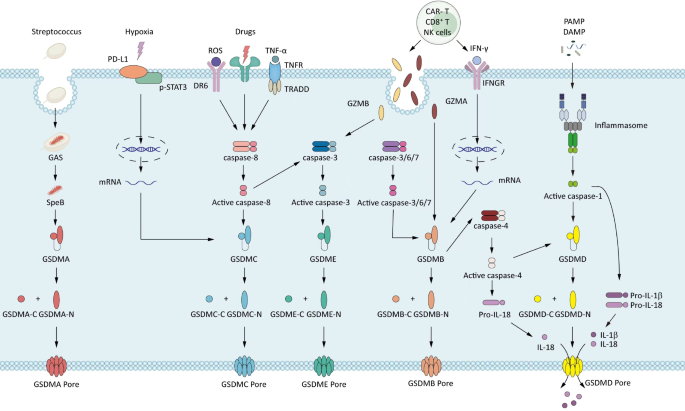
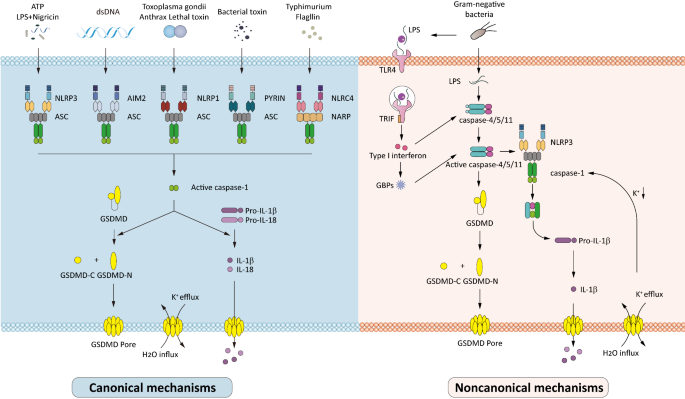
方法细节:免疫细胞焦亡部分,引用Martinon等的炎症小体研究(经典途径:NLRP3/AIM2激活caspase-1切割GSDMD)、Kayagaki等的非经典途径研究(caspase-4/5/11直接识别LPS切割GSDMD);癌症细胞焦亡部分,整合化疗药物诱导的caspase-3/GSDME途径(Wang等)、缺氧微环境中的TNF-α/caspase-8/GSDMC途径(Hou等)、GZMA切割GSDMB途径(Zhou等)。
结果解读:免疫细胞焦亡依赖先天性免疫的炎症小体激活,而癌症细胞焦亡依赖适应性免疫或微环境信号的凋亡通路重编程,核心差异在于gasdermin的激活方式。
3.3 癌症细胞焦亡的抗肿瘤免疫作用
实验目的:探讨癌症细胞焦亡的免疫调控机制。
方法细节:引用三项关键研究——Wang等通过生物正交系统将活性gasdermin递送至4T1乳腺癌细胞,发现10%-15%细胞焦亡即可增强CD3+ T细胞浸润,与anti-PD-1协同实现肿瘤 regression(动物模型,n=5,P<0.01);Zhang等证实NK细胞释放的GZMB切割GSDME,促进巨噬细胞吞噬及细胞毒性淋巴细胞浸润(体外实验,n=3,P<0.05);Zhou等发现GZMA切割GSDMB诱导的焦亡通过IFN-α/TNF-γ正反馈 loop 上调GSDMB,增强肿瘤清除(小鼠模型,n=6,P<0.01)。
结果解读:急性癌症细胞焦亡通过DAMPs激活树突状细胞,促进细胞毒性T细胞/NK细胞浸润,增强免疫;慢性焦亡则诱导免疫抑制,促进肿瘤进展。
3.4 基于癌症细胞焦亡的治疗策略探索
实验目的:开发靶向癌症细胞焦亡的治疗方法。
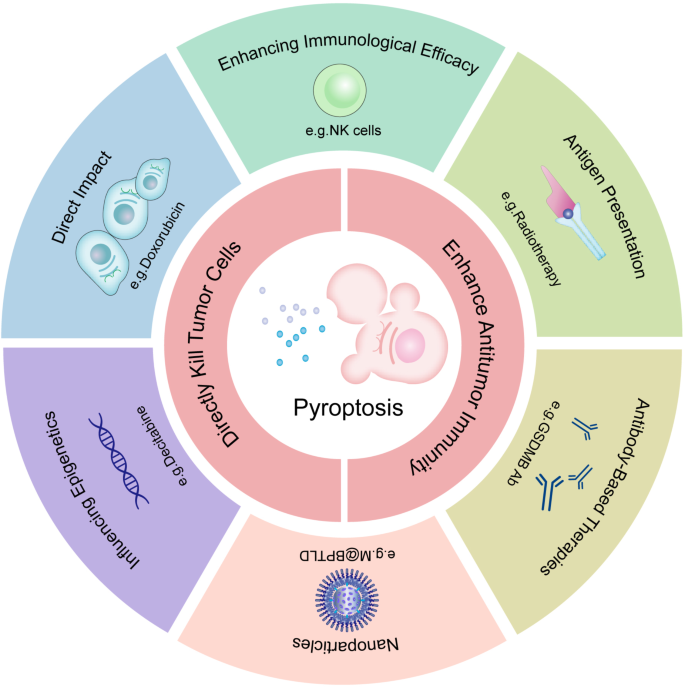
方法细节:列举多类策略——(1)GSDME甲基化调节:Fan等用DAC(地西他滨)抑制GSDME启动子甲基化,增强顺铂诱导的焦亡(4T1模型,肿瘤生长抑制率70%,n=5,P<0.01);(2)GSDMB靶向:Molina-Crespo等通过透明质酸纳米胶囊递送anti-GSDMB抗体至HER2阳性乳腺癌细胞,降低肺转移率60%(小鼠模型,n=6,P<0.01);(3)癌症特异性治疗:肺癌中化疗药物(紫杉醇、顺铂)诱导的caspase-3/GSDME途径增强PD-L1抑制剂疗效(Zhang等,临床前模型,n=4,P<0.05);黑色素瘤中低剂量铁补充协同ROS诱导剂促进GSDME依赖的焦亡(Zhou等,肿瘤生长抑制率80%,n=5,P<0.01)。
结果解读:靶向癌症细胞焦亡的策略在多种模型中显示显著疗效,尤其与免疫检查点抑制剂协同时效果增强。
3.5 癌症细胞焦亡研究的挑战与机遇
实验目的:分析临床转化的瓶颈。
方法细节:讨论三方面挑战——(1)机制争议:Liu等发现CAR-T细胞诱导的焦亡需caspase-3激活,而Zhang等认为GZMB可直接切割GSDME,差异源于细胞系GSDME表达不同;(2)临床障碍:肿瘤相关巨噬细胞(TAMs)的焦亡可能促进肿瘤生长,IL-1β的促肿瘤作用需中和;(3)耐药机制:凋亡缺陷的肿瘤细胞对凋亡/焦亡均耐药。
结果解读:未来需开发特异性gasdermin激活剂、明确焦亡与其他途径的交互作用、寻找预测性生物标志物。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker均为gasdermin家族成员及调控因子,核心聚焦治疗反应预测与预后评估。
Biomarker定位与筛选逻辑
| Biomarker | 类型 | 筛选来源 | 验证逻辑 |
|---|---|---|---|
| GSDME | 肿瘤组织mRNA/蛋白 | 乳腺癌临床样本 | TCGA数据库筛选→qRT-PCR验证→细胞实验(化疗药物处理) |
| GSDMB | 肿瘤组织DNA/蛋白 | HER2阳性乳腺癌样本 | 扩增分析→动物模型验证anti-GSDMB抗体疗效 |
| GSDMC | 肿瘤组织蛋白 | 缺氧肿瘤微环境样本 | 缺氧诱导PD-L1核转位→免疫组化验证→细胞实验(促肿瘤进展) |
| PD-L1 | 肿瘤细胞核蛋白 | 肿瘤组织免疫组化 | 与GSDMC共表达分析→临床预后关联(HR=2.1,95% CI 1.3-3.5,P=0.003) |
核心成果提炼
- GSDME:乳腺癌化疗反应的生物标志物,低表达与化疗耐药相关(Kim等,n=50,P<0.05);
- GSDMB:HER2阳性乳腺癌转移的生物标志物,扩增与转移率升高相关(Hergueta-Redondo等,n=100,P<0.001);
- GSDMC:缺氧肿瘤微环境中肿瘤进展的生物标志物,与PD-L1共表达提示不良预后(Hou等,n=80,HR=2.1,P=0.003);
- PD-L1:缺氧微环境中GSDMC上调的驱动因子,核PD-L1表达可预测肿瘤进展(Hou等,n=80,P<0.05)。
这些Biomarker的创新性在于首次将gasdermin家族与癌症临床特征关联,为治疗效果预测和靶向治疗提供了潜在靶点。
总结
本文系统整合了癌症细胞焦亡的基础研究与临床进展,明确其“双刃剑”作用模式,并提出临床转化的关键方向。未来需解决机制争议、开发特异性调节剂、验证生物标志物,推动该领域从基础到临床的突破。
