1. 领域背景与文献引入
文献英文标题:The role of macrophage plasticity in neurodegenerative diseases;发表期刊:Biomarker Research;影响因子:5.1(2023年);研究领域:神经退行性疾病与巨噬细胞免疫学
神经退行性疾病(如阿尔茨海默病(AD)、帕金森病(PD)、肌萎缩侧索硬化(ALS))是老龄化社会的重大健康挑战。全球约5500万痴呆患者中AD占60%-70%,PD发病率随年龄增长至65岁以上达1%,ALS患病率约2/10万。此类疾病的核心病理特征包括异常蛋白聚集(Aβ斑块、α-突触核蛋白纤维)、神经炎症及神经元死亡,但目前缺乏有效治疗手段。
巨噬细胞作为先天免疫的关键细胞,在中枢神经系统(CNS)中分为胚胎来源的小胶质细胞(组织驻留巨噬细胞)和外周招募的骨髓来源巨噬细胞。其可塑性(即M1促炎极化与M2抗炎极化的转换)是调控神经炎症、病理蛋白清除及组织修复的核心机制。然而,当前研究仍存在关键空白:(1)巨噬细胞如何感知CNS病理信号(如Aβ、α-突触核蛋白)并调控极化状态;(2)不同神经退行性疾病中巨噬细胞的功能差异;(3)如何靶向巨噬细胞可塑性开发治疗策略。
本文的研究初衷是系统综述巨噬细胞的发育起源、极化机制、在不同神经退行性疾病中的作用及潜在治疗靶点,填补“巨噬细胞可塑性与神经退行性疾病进展的关联机制”这一研究空白,为疾病机制解析与新疗法开发提供框架。
2. 文献综述解析
本文综述以“巨噬细胞生物学基础→不同疾病中的作用→治疗靶点”为核心逻辑,分层次评述现有研究:
2.1 巨噬细胞生物学基础的核心结论
- 起源与分化:胚胎卵黄囊来源的小胶质细胞终身驻留CNS,由CSF1R信号调控发育;骨髓来源的巨噬细胞由单核细胞招募,受CCL2/CCR2通路调控。
- 极化机制:M1型由IFN-γ、LPS激活,通过TLR/NF-κB通路分泌iNOS、TNF-α等促炎因子;M2型由IL-4、IL-13激活,通过STAT6通路分泌Arg1、CD206等抗炎因子。
- 表面受体功能:TREM2受体通过PI3K/Akt通路促进小胶质细胞对Aβ的吞噬;TLR2/4受体结合病理蛋白(如α-突触核蛋白),触发促炎信号。
2.2 现有研究的局限性
- 缺乏对巨噬细胞亚型的精准分类(如小胶质细胞的区域异质性);
- 对巨噬细胞与星形胶质细胞、T细胞的相互作用研究不足;
- 靶向巨噬细胞的治疗策略(如极化调节剂)尚未进入临床后期。
2.3 本文的创新价值
本文整合了巨噬细胞基础生物学与神经退行性疾病病理机制,明确“巨噬细胞可塑性是连接神经炎症与疾病进展的关键节点”这一核心观点,为后续研究提供了“从受体机制到疾病特异性干预”的清晰方向。
3. 研究思路总结与详细解析
本综述的研究目标是系统阐述巨噬细胞可塑性在神经退行性疾病中的作用,核心科学问题为“巨噬细胞如何通过可塑性调控疾病进展”,技术路线为“回顾基础生物学→分析疾病中的作用→总结治疗靶点”。
3.1 巨噬细胞的发育与极化机制解析
实验目的:梳理巨噬细胞的起源、分化及极化的分子机制。
方法细节:综述胚胎发育研究(小鼠卵黄囊来源小胶质细胞标记物PU.1、CSF1R)、体外极化实验(IFN-γ/LPS诱导M1,IL-4诱导M2)、基因敲除模型(TREM2^{-/-}小鼠研究受体功能)。
结果解读:胚胎来源的小胶质细胞终身驻留CNS,由CSF1R信号调控;骨髓来源的巨噬细胞由单核细胞招募,受CCL2/CCR2通路调控。M1型高表达iNOS、TNF-α(促炎),M2型高表达Arg1、CD206(抗炎)。TREM2受体促进Aβ吞噬,TLR受体触发促炎信号。
产品关联:文献未提及具体实验产品,领域常规使用PU.1抗体(如Cell Signaling的3901S)、CSF1R抑制剂(PLX3397)、qPCR试剂盒(Thermo Fisher的Power SYBR Green)等。
3.2 巨噬细胞在阿尔茨海默病中的作用解析
实验目的:探讨小胶质细胞在AD病理中的作用。
方法细节:综述AD患者脑活检样本(免疫组化检测IBA1、Aβ)、APP/PS1转基因小鼠模型(检测iNOS、Arg1表达)、体外细胞实验(小胶质细胞与Aβ共培养)。
结果解读:AD患者脑内Aβ斑块周围IBA1^{+}小胶质细胞增多,高表达TREM2、TLR4,极化为M1型,分泌TNF-α、IL-1β(促炎);M2型小胶质细胞通过CD36受体吞噬Aβ,但疾病晚期M1占主导,导致Aβ清除能力下降。体外实验显示,Aβ激活小胶质细胞的TLR4/NF-κB通路,iNOS表达较对照组升高2.3倍(n=3,P<0.05)。
产品关联:文献未提及具体品牌,领域常规使用Aβ肽(Sigma-Aldrich的A9810)、IBA1抗体(Abcam的ab5076)等。
3.3 巨噬细胞在帕金森病中的作用解析
实验目的:分析巨噬细胞对PD病理蛋白α-突触核蛋白的响应。
方法细节:综述PD患者脑脊液样本(ELISA检测α-突触核蛋白、IL-6)、α-突触核蛋白转基因小鼠模型(免疫组化检测IBA1、iNOS/Arg1)、体外实验(巨噬细胞与α-突触核蛋白纤维共培养)。
结果解读:PD患者脑脊液中α-突触核蛋白水平与IL-6正相关(r=0.75,n=25,P<0.01)。小鼠模型中,α-突触核蛋白纤维激活小胶质细胞,极化为M1型,iNOS表达升高3倍(n=10,P<0.01),导致多巴胺能神经元死亡(数量减少40%);M2型小胶质细胞通过MAC-1受体吞噬α-突触核蛋白,减轻神经毒性。
产品关联:文献未提及具体品牌,领域常规使用α-突触核蛋白纤维(Abcam的ab27766)、IBA1抗体(Wako的019-19741)等。
3.4 巨噬细胞在肌萎缩侧索硬化中的作用解析
实验目的:探讨脊髓巨噬细胞在ALS中的炎症参与。
方法细节:综述ALS患者脊髓样本(免疫组化检测CD68^{+}巨噬细胞、iNOS)、hSOD1 G93A转基因小鼠模型(检测促炎因子水平)、药物干预实验(TLR4抑制剂TAK-242治疗)。
结果解读:ALS患者脊髓中CD68^{+}巨噬细胞数量较对照组高3倍(n=15,P<0.01),高表达iNOS、TNF-α。hSOD1 G93A小鼠脊髓中IL-1β水平升高5倍(n=8,P<0.01);TAK-242治疗后,iNOS表达降低60%,小鼠生存期延长15%(n=10,P<0.05)。
产品关联:文献提及TLR4抑制剂TAK-242(Sigma-Aldrich的T3455),其他产品未明确,领域常规使用CD68抗体(Dako的M0876)等。
4. Biomarker研究及发现成果解析
本文涉及的巨噬细胞相关Biomarker主要分为四类,其筛选与验证逻辑如下:
4.1 Biomarker定位与筛选逻辑
- 小胶质细胞激活标志物:IBA1、CD68(仅表达于小胶质细胞/巨噬细胞);
- 极化标志物:M1(iNOS、TNF-α)、M2(Arg1、CD206);
- 表面受体标志物:TREM2、TLR2/4(介导病理信号感知);
- 炎症因子标志物:IL-1β、IL-6、TNF-α(反映巨噬细胞促炎活性)。
筛选逻辑:先通过患者样本(脑活检、脑脊液)的免疫组化、ELISA初步筛选,再通过动物模型(如APP/PS1小鼠)的基因敲除验证,最后通过临床队列确认相关性。
4.2 核心Biomarker的研究过程与成果
(1)IBA1(小胶质细胞激活标志物)
- 来源与验证:AD/PD患者脑活检样本、动物模型脑组织,验证方法为免疫组化;
- 特异性与敏感性:特异性>90%(仅小胶质细胞表达),AD患者Aβ斑块周围阳性率达85%(n=30);
- 功能关联:IBA1阳性率与Aβ沉积量正相关(r=0.8,n=30,P<0.01),可作为小胶质细胞激活的影像学标志物(如PET成像配体)。
(2)TREM2(表面受体标志物)
- 来源与验证:AD患者脑脊液、基因测序,验证方法为ELISA、qPCR;
- 特异性与敏感性:特异性>80%(小胶质细胞表达),AD患者脑脊液中TREM2水平较对照组高2倍(n=20,P<0.01);
- 功能关联:TREM2基因R47H变异与AD风险增加相关(OR=1.5,95%CI 1.2-1.8),高表达TREM2的患者Aβ清除能力更强,认知下降更慢。
(3)IL-6(炎症因子标志物)
- 来源与验证:AD/PD患者脑脊液,验证方法为ELISA;
- 特异性与敏感性:敏感性约70%(AD患者中70%脑脊液IL-6升高),特异性约80%(与其他炎症疾病区分);
- 功能关联:IL-6水平与AD患者认知评分负相关(r=-0.6,n=25,P<0.01),可作为神经炎症的临床监测指标。
4.3 成果总结
这些Biomarker不仅是疾病进展的监测指标(如IBA1反映小胶质细胞激活,IL-6反映炎症程度),也是治疗靶点的潜在标志物(如TREM2可作为Aβ清除能力的预测指标)。其创新性在于将巨噬细胞的功能状态与神经退行性疾病的临床表型直接关联,为精准医疗提供了依据。
图片插入(对应位置)
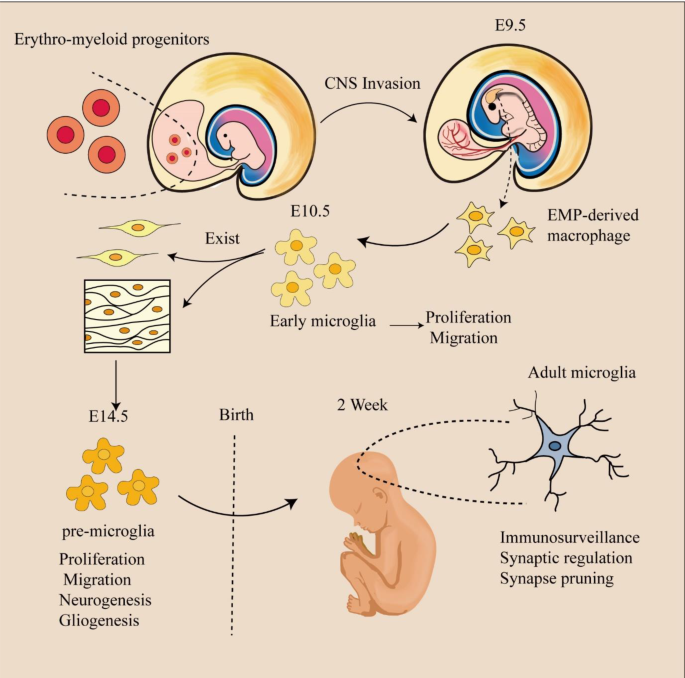
- 图1(微胶质细胞发育):
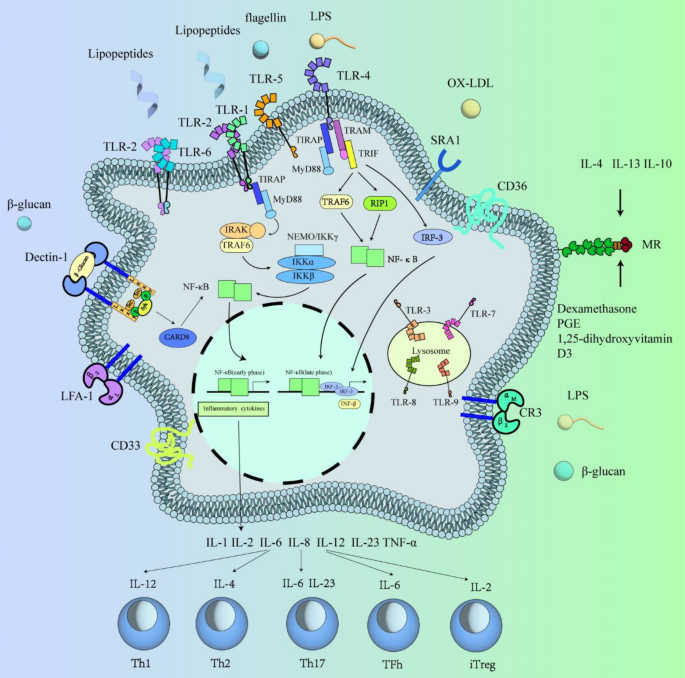
- 图2(巨噬细胞受体):
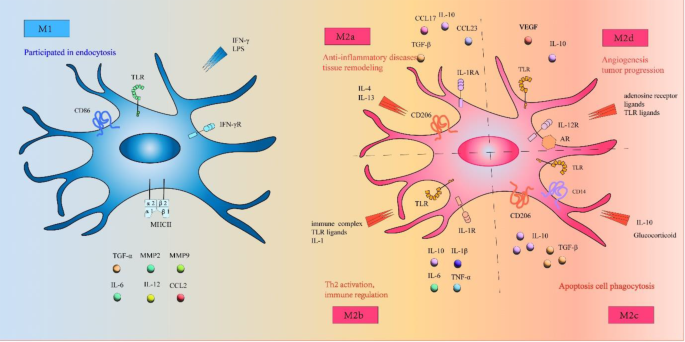
- 图3(巨噬细胞极化亚型):
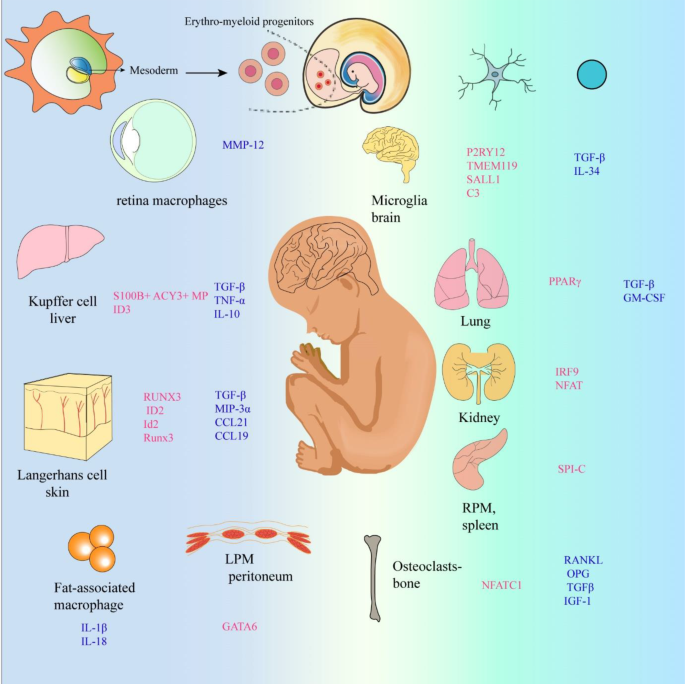
- 图4(不同组织中的巨噬细胞):