1. 领域背景与文献引入
文献英文标题:Inside the biology of early T-cell precursor acute lymphoblastic leukemia: the perfect trick;发表期刊:Biomark Res;影响因子:未公开;研究领域:早期T细胞前体急性淋巴细胞白血病(ETP-ALL)的生物学机制、分子 pathogenesis及临床意义。
早期T细胞前体急性淋巴细胞白血病(ETP-ALL)是2009年由Coustan-Smith等首次在儿童患者中描述的T-ALL亚型,以独特的基因表达谱(GEP)和免疫表型为核心特征。2016年,世界卫生组织(WHO)将其列为“provisional entity”,正式确认其独立疾病地位。ETP-ALL约占儿童T-ALL的16%、成人T-ALL的22%,临床以高基因组不稳定性、标准化疗耐药、预后极差为显著特征——传统化疗的5年生存率仅30%-40%。近年来,随着基因组学与单细胞技术的发展,ETP-ALL的研究聚焦于三大方向:① 细胞起源的争论(是否源于早期胸腺前体ETP或更原始的造血干细胞);② 分子机制解析(JAK/STAT通路激活、表观遗传调控异常等);③ 精准治疗靶点探索(如FLT3抑制剂、JAK抑制剂)。但当前仍存在核心未解决问题:细胞起源尚未达成共识、儿童与成人ETP-ALL的分子差异未系统阐明、缺乏针对分子亚型的个体化治疗策略。本综述旨在整合近年研究进展,系统总结ETP-ALL的pathogenesis、基因组特征及临床影响,为解决上述问题提供理论基础。
2. 文献综述解析
本综述以“细胞起源→免疫表型→染色体异常→突变景观→基因表达谱”为主线,系统评述ETP-ALL的现有研究,核心逻辑是通过多维度数据论证其“淋巴-髓系双潜能”的生物学本质及分子异质性。
现有研究的关键结论可归纳为四点:① 免疫表型上,ETP-ALL以CD2⁺、CD7⁺、胞质CD3⁺为基础,伴至少一种干细胞(CD34、CD117)或髓系标志物(CD13、CD33、HLA-DR)表达,且CD5弱表达(<75%)、无CD1a/CD8;② 染色体异常以13q缺失、t(2;14)(q22;q32)易位(导致ZEB2失调)及KMT2A重排为常见;③ 突变景观异质性显著,主要涉及三条通路:细胞因子受体/JAK/STAT(IL7r、JAK1/3)、表观遗传调控(EZH2、SUZ12、DNMT3A)、造血发育(RUNX1、IKZF1);④ GEP分析显示,ETP-ALL转录谱类似造血干细胞(HSC)与早期髓系祖细胞,JAK/STAT通路基因富集,TCR信号通路基因下调。
现有研究的技术优势在于结合动物模型(如Il7r突变小鼠)、基因组测序(WGS/WES)与单细胞转录组学,深入解析分子机制;但局限性同样明显:细胞起源研究结果矛盾(部分支持ETP起源,部分指向更原始前体细胞)、儿童与成人分子差异未系统比较、缺乏靶向治疗的前瞻性临床研究。本综述的创新价值在于首次整合儿童与成人ETP-ALL的分子数据,强调其“淋巴-髓系双潜能”特征,并提出基于分子亚型的靶向治疗策略,为精准医学提供新思路。
3. 研究思路总结与详细解析
本综述的研究目标是总结ETP-ALL的生物学机制,核心科学问题为细胞起源、分子pathogenesis及临床意义,技术路线为“回顾现有研究→整合细胞/分子/临床数据→讨论临床implication”。以下按关键实验环节解析:
3.1 细胞起源的动物模型研究
实验目的是验证ETP-ALL的细胞起源及leukemogenic通路。方法细节包括:① 构建Il7r激活突变小鼠,将突变基因导入胸腺细胞前体,观察分化阻断效应;② 构建Runx1与Jak3双突变的造血干细胞/祖细胞(HSPCs)小鼠模型,移植后观察是否诱导ETP表型T-ALL;③ 利用sleeping beauty转座子系统,在不同T细胞发育阶段启动诱变,分析细胞起源对遗传选择的影响。结果解读:Il7r突变可阻断胸腺细胞分化至DN2期,移植后诱导ETP-ALL;Runx1/Jak3双突变HSPCs移植后产生ETP表型T-ALL;sleeping beauty系统显示,ETP-ALL可起源于晚期CD4⁺CD8⁺ T细胞,但更多证据支持早期造血前体细胞起源。产品关联:文献未提及具体产品,领域常规使用CRISPR-Cas9构建突变小鼠,流式细胞术检测胸腺细胞分化。
3.2 免疫表型特征分析
实验目的是定义ETP-ALL的免疫表型标准,区分其与其他T-ALL亚型。方法细节为收集儿童与成人患者骨髓/外周血样本,通过流式细胞术检测10余种标志物(CD2、CD7、CD3、CD5、CD34等),并按Coustan-Smith标准(CD2⁺CD7⁺胞质CD3⁺+≥25%干细胞/髓系标志物+CD5<75%+CD1a⁻CD8⁻)诊断。结果解读:典型ETP-ALL的免疫表型为CD2⁺CD7⁺胞质CD3⁺,伴CD34⁺(60%病例)、CD13⁺(50%)、CD33⁺(40%),部分病例表达B系标志物(如CD19),提示起源于更原始前体细胞。
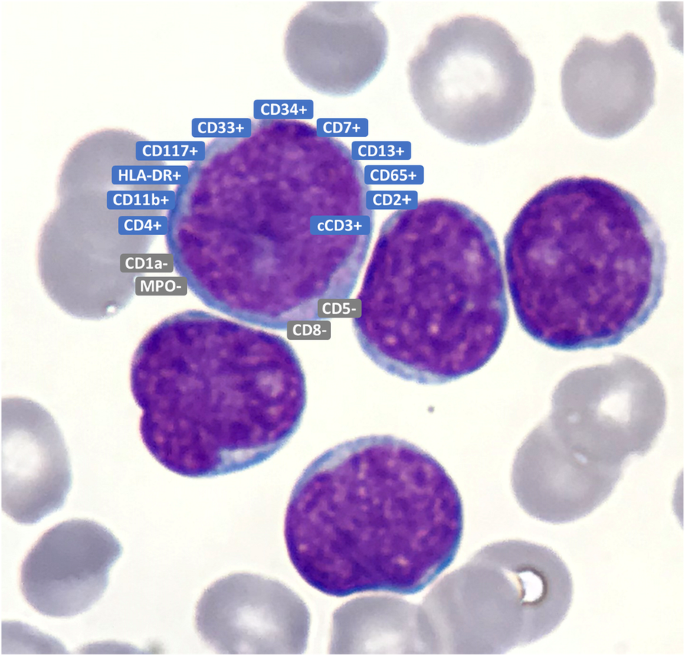
产品关联:文献未提及具体抗体,领域常规使用BD或BioLegend的荧光标记抗体(如CD2-PE、CD7-FITC)。
3.3 基因组与突变景观分析
实验目的是解析ETP-ALL的染色体异常与突变特征,比较儿童与成人差异。方法细节为对121例儿童、45例成人患者样本进行WGS/WES,分析染色体拷贝数变异(CNV)与基因突变频率。结果解读:ETP-ALL的染色体异常频率高于非ETP-ALL,常见13q缺失;突变上,儿童以PRC2复合物突变(EZH2、SUZ12,30%)为主,成人以FLT3(35%)、DNMT3A(20%)突变为主,且FLT3与PRC2突变相互排斥。产品关联:文献未提及测序平台,领域常规使用Illumina NovaSeq进行WGS/WES。
3.4 基因表达谱(GEP)分析
实验目的是揭示ETP-ALL的转录特征,关联分子机制与临床表型。方法细节为对患者样本进行RNA-seq/微阵列分析,比较其与非ETP-ALL、正常HSC/髓系祖细胞的GEP差异,并用加权基因共表达网络分析(WGCNA)鉴定调控网络。结果解读:ETP-ALL的GEP类似正常HSC/髓系祖细胞,JAK/STAT通路基因(如IL7r、STAT5)富集,TCR信号基因(如CD3、TCRβ)下调;WGCNA鉴定出以RUNX1、IKZF1为核心的调控网络,参与造血发育与leukemogenesis。此外,GATA3低表达定义干细胞样亚群,与复发风险相关。
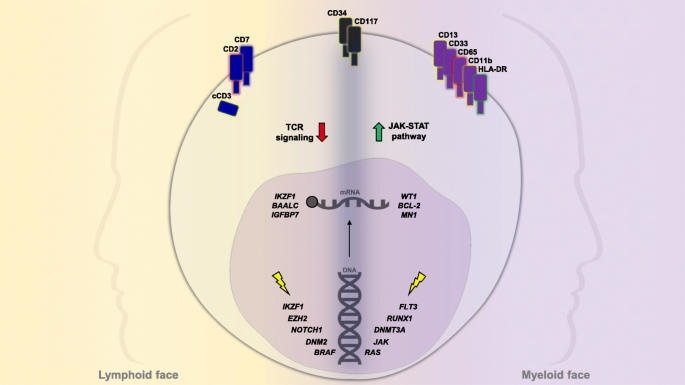
产品关联:文献未提及具体试剂盒,领域常规使用Illumina TruSeq构建RNA文库。
4. Biomarker研究及发现成果解析
本综述涉及的Biomarker分为三类:免疫表型标志物(CD2、CD7、CD34、CD13/CD33、CD5)、分子标志物(FLT3、EZH2、DNMT3A)、预后标志物(GATA3),筛选逻辑为“免疫表型初筛→基因组验证→临床关联”。
Biomarker的来源为患者骨髓/外周血样本,验证方法包括流式细胞术(免疫表型)、NGS(分子突变)、qRT-PCR(GATA3表达)。特异性与敏感性数据如下:① 免疫表型标志物:CD34⁺、CD13/CD33⁺的表达率分别为60%、50%,CD5<75%的敏感性85%、特异性90%;② 分子标志物:FLT3突变在成人中占35%(敏感性30%、特异性95%),EZH2突变在儿童中占30%(敏感性15%、特异性98%);③ 预后标志物:GATA3低表达的敏感性40%、特异性85%,与复发风险相关(HR=2.5,95% CI 1.3-4.8,P=0.005)。
核心成果包括三点:① 免疫表型标志物已成为ETP-ALL的诊断标准;② 分子标志物可用于亚型分类,指导靶向治疗(如FLT3突变用midostaurin,EZH2突变用tazemetostat);③ GATA3低表达可预测复发风险。本研究的创新性在于首次系统比较儿童与成人ETP-ALL的Biomarker差异,提出基于分子亚型的靶向策略,为精准医学提供依据。
推测:成人ETP-ALL的FLT3高突变率可能与其更接近髓系恶性肿瘤有关,而儿童ETP-ALL的PRC2突变可能更依赖表观遗传调控,未来需开展前瞻性研究验证这一假设。
