1. 领域背景与文献引入
文献英文标题:Sintilimab for the treatment of non-small cell lung cancer;发表期刊:Biomarker Research;影响因子:未公开;研究领域:非小细胞肺癌免疫治疗。
肺癌是全球第二大常见恶性肿瘤,也是癌症相关死亡的首要原因,2020年全球新发肺癌病例约220万,死亡病例约180万。非小细胞肺癌(NSCLC)占肺癌总数的85%以上,其中约70%为非鳞癌亚型。传统治疗模式(手术、铂类化疗、放疗)对晚期NSCLC患者的疗效有限,铂类双药化疗的客观缓解率(ORR)仅约20%,中位生存期不足1年。近十年,免疫检查点抑制剂(ICI)尤其是程序性死亡受体-1(PD-1)/程序性死亡配体-1(PD-L1)抑制剂的问世,彻底改变了NSCLC的治疗格局——此类药物通过阻断PD-1/PD-L1通路,恢复T细胞的抗肿瘤活性,已成为无驱动基因突变晚期NSCLC的一线治疗选择。
信迪利单抗(Sintilimab)是中国自主研发的全人源IgG4型抗PD-1单克隆抗体,通过酵母展示技术筛选获得,具有高亲和力(解离常数74 pM)和持续PD-1受体占据率(>95%)。截至研究发表时,信迪利单抗已获中国国家药品监督管理局(NMPA)批准治疗经典霍奇金淋巴瘤、肝细胞癌及鳞状/非鳞状NSCLC,但仍存在未解决的核心问题:①单药治疗肺磨玻璃结节(GGN)的疗效尚不明确;②联合治疗方案的最佳组合及生物标志物筛选仍需系统验证;③病理反应能否作为新辅助免疫治疗的替代终点缺乏统一结论。本研究旨在系统综述信迪利单抗在NSCLC中的临床研究数据,探讨其单药及联合方案的疗效、安全性,以及病理反应和生物标志物的价值,为后续临床试验提供依据。
2. 文献综述解析
作者对NSCLC免疫治疗的现有研究进行了分类梳理:①PD-1/PD-L1抑制剂的应用现状:全球已有6种PD-1/PD-L1抑制剂获批NSCLC治疗,中国获批7种(包括信迪利单抗),但单药治疗的响应率仅约20%-40%;②信迪利单抗的前期研究:在经典霍奇金淋巴瘤中ORR达85.4%,肝细胞癌中联合治疗的ORR达20.5%,但NSCLC中的数据分散;③现有研究的局限:单药治疗对GGN等惰性病变的疗效不明确,联合方案的安全性(如免疫相关不良反应)需更深入分析,生物标志物(PD-L1、肿瘤突变负荷(TMB))的预测价值存在异质性(不同检测方法导致结果不一致)。
通过对比现有研究,本研究的创新点在于:①首次系统整合信迪利单抗在NSCLC中的所有临床试验(涵盖单药、新辅助、联合治疗);②明确病理完全缓解(pCR)/主要病理缓解(MPR)可作为新辅助免疫治疗的替代终点;③发现T细胞受体(TCR)克隆性指数、循环肿瘤DNA(ctDNA)残留等新型生物标志物,弥补了PD-L1/TMB的局限性。
3. 研究思路总结与详细解析
本研究的整体框架为:“系统检索信迪利单抗治疗NSCLC的临床试验→分类分析单药/联合方案的疗效→评估病理反应的替代终点价值→探索生物标志物与疗效的关联→总结安全性特征”。以下分关键环节解析:
3.1 单药治疗临床试验
实验目的:验证信迪利单抗单药在NSCLC中的安全性、剂量及疗效。
方法细节:纳入3项研究:①一线人体研究(NCT02937116):12例晚期实体瘤患者接受递增剂量信迪利单抗(200mg Q3W为推荐剂量);②新辅助治疗研究(ChiCTR-OIC-17013726):40例IA-IIIB期NSCLC患者接受2周期信迪利单抗,37例后续手术;③GGN研究(ChiCTR-1900022159、CCTC-1901):20例高风险GGN患者及36例多发GGN患者接受信迪利单抗治疗。
结果解读:①一线研究显示,信迪利单抗200mg Q3W的ORR为33.3%(2例部分缓解(PR)、2例稳定(SD)),无治疗相关死亡;②新辅助治疗中,37例手术患者的R0切除率为97.3%,MPR率为40.5%(15/37),pCR率为16.2%(6/37),且鳞状癌患者的无病生存期(DFS)更长(HR=2.71,P=0.1479);③GGN研究中,疾病控制率(DCR)达100%,但因GGN的惰性生长特性,无法确认肿瘤退缩是否由药物直接导致。
产品关联:文献未提及具体实验产品,领域常规使用的试剂/仪器包括:信迪利单抗(抗PD-1单克隆抗体)、PD-L1免疫组化检测试剂盒(如Dako 22C3)、多层螺旋CT(用于GGN评估)。
3.2 联合治疗临床试验
实验目的:探索信迪利单抗联合方案的疗效优势及安全性。
方法细节:纳入5类联合方案:①联合铂类化疗(NCT02937116的D/E队列:19例非鳞NSCLC联合培美曲塞+铂类,17例鳞NSCLC联合吉西他滨+铂类;ORIENT-11(非鳞NSCLC)、ORIENT-12(鳞NSCLC)的III期研究);②联合多西他赛(ChiCTR1900027634:25例铂类耐药晚期NSCLC患者接受多西他赛+信迪利单抗);③联合细胞因子诱导的杀伤(CIK)细胞(NCT03987867:34例晚期NSCLC患者接受信迪利单抗+化疗+CIK细胞);④联合放疗(NCT03812549:12例IV期NSCLC患者接受立体定向体部放疗(SBRT)+低剂量放疗(LDRT)+信迪利单抗);⑤联合安罗替尼(NCT03628521:22例晚期NSCLC患者接受信迪利单抗+安罗替尼)。
结果解读:①联合铂类化疗的ORR为64.7%-68.4%(高于单药),ORIENT-11显示联合方案的中位无进展生存期(PFS)为8.9个月(化疗组5.0个月,HR=0.482,P<0.0001),中位总生存期(OS)未达到(化疗组16.8个月,P=0.0003);②联合多西他赛的ORR为24%,中位PFS为5.5个月,无治疗相关死亡;③联合CIK细胞的ORR达81.3%,但1例患者死于肺炎;④联合放疗的ORR为70%,无3级以上不良反应;⑤联合安罗替尼的ORR为72.7%,中位PFS为15个月,但54.5%患者出现3级以上不良反应(1例死于免疫性肺炎)。
产品关联:领域常规使用的联合药物包括铂类(顺铂/卡铂)、多西他赛、安罗替尼(多靶点酪氨酸激酶抑制剂)、CIK细胞制剂,放疗设备为SBRT系统。
3.3 不良反应分析
实验目的:评估信迪利单抗及联合方案的安全性。
方法细节:汇总12项研究的不良反应数据,按单药/联合分类统计:①单药治疗:所有级别治疗相关不良反应(TRAE)发生率16.7%-100%,3级以上TRAE发生率0-25%,致命TRAE发生率0-2.5%(1/40例);②联合铂类化疗:所有级别TRAE发生率99.6%-100%,3级以上TRAE发生率61.7%-86.6%,但致命TRAE发生率(2.3%-4.5%)低于化疗组(6.7%-6.9%);③联合安罗替尼:所有级别TRAE发生率100%,3级以上TRAE发生率54.5%,致命TRAE发生率4.5%(1/22例)。
结果解读:信迪利单抗的安全性特征与其他PD-1抑制剂一致,联合化疗虽增加不良反应发生率,但致命风险未显著升高;联合安罗替尼需警惕免疫性肺炎。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究涉及的Biomarker类型包括:①病理反应(pCR/MPR);②分子标志物(PD-L1表达、TMB、TCR克隆性指数);③液体活检标志物(ctDNA残留)。筛选验证逻辑为:“临床试验数据关联→疗效指标(ORR、PFS、OS)→统计显著性分析”。
研究过程详述
- 病理反应(pCR/MPR):来自新辅助治疗研究(ChiCTR-OIC-17013726)的手术标本,MPR定义为残留活肿瘤≤10%,pCR定义为无活肿瘤。结果显示:MPR患者的2年DFS率(86.7%)显著高于非MPR患者(63.8%),提示MPR可作为新辅助免疫治疗的替代终点。
- PD-L1表达:通过免疫组化检测肿瘤细胞PD-L1表达(肿瘤比例评分,TPS),结果显示:TPS≥50%的患者MPR率更高(P<0.05),但联合治疗中PD-L1表达与疗效无显著关联(可能因检测方法异质性)。
- TMB:通过靶向测序检测肿瘤突变负荷,结果显示:TMB≥10突变/Mb的患者2年DFS率更高(HR=0.125,P<0.05),但联合治疗中TMB与ORR无显著关联。
- TCR克隆性/多样性指数:来自联合铂类化疗研究(NCT02937116)的TCR测序数据,结果显示:TCR克隆性指数升高与疾病控制率(DCR)相关(P<0.05),TCR多样性指数升高与OS延长相关(P<0.05)。
- ctDNA残留:来自联合多西他赛研究(ChiCTR1900027634)的液体活检数据,结果显示:治疗6周后ctDNA阳性患者的OS(HR=100,P<0.05)和PFS显著缩短,提示ctDNA残留是独立预后因子。
核心成果提炼
- 病理反应的替代终点价值:MPR/pCR可作为新辅助信迪利单抗治疗的替代终点,其预测DFS的准确性高于影像学评估(如RECIST标准)。
- 新型Biomarker的创新性:①TCR克隆性指数首次被报道与信迪利单抗联合化疗的DCR相关,TCR多样性指数与OS相关;②ctDNA残留首次被证实为联合多西他赛方案的预后因子(HR=100),其预测价值优于PD-L1/TMB。
- 局限性:PD-L1和TMB的预测价值受检测方法影响(如不同IHC抗体、测序平台),需标准化检测流程;TCR和ctDNA的研究样本量较小,需扩大队列验证。
图片补充
图1:信迪利单抗治疗NSCLC的临床试验时间线
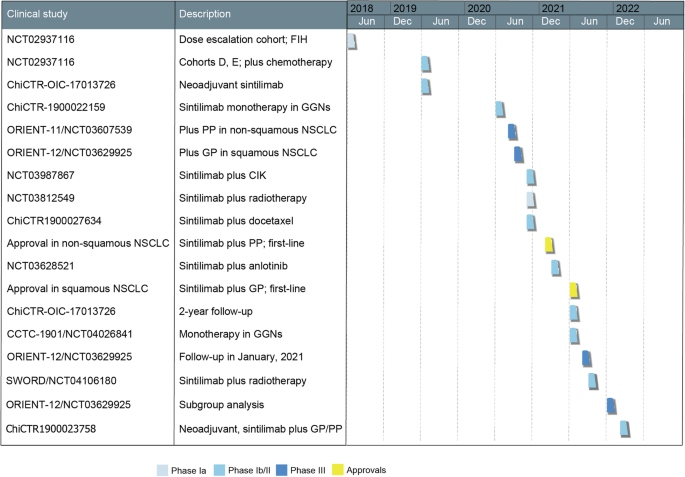
(注:图1展示了信迪利单抗在NSCLC中的临床试验时间线,包括单药、新辅助、联合治疗的关键研究节点。)
图2:信迪利单抗的疗效与不良反应森林图
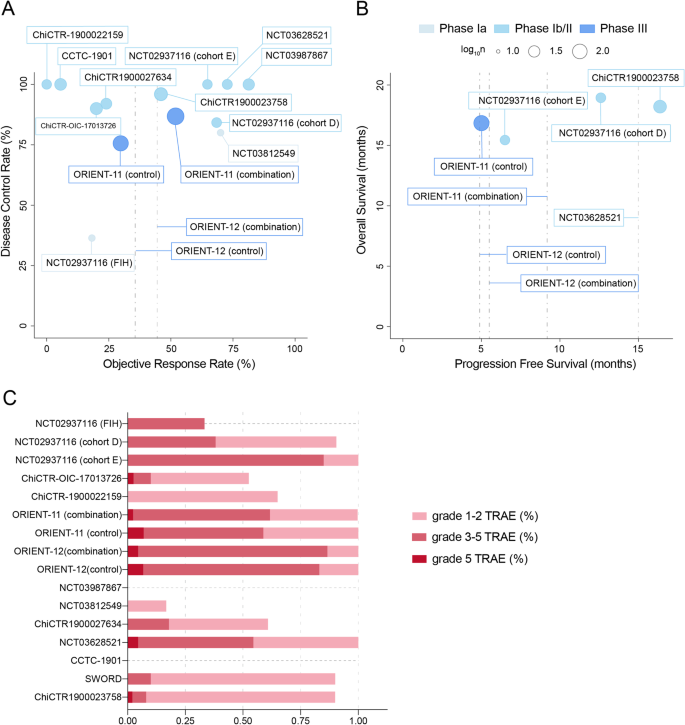
(注:图2A、B展示了信迪利单抗单药及联合方案的ORR和PFS,图2C展示了不同方案的不良反应发生率。)
