1. 领域背景与文献引入
文献英文标题:Lentivirus-based production of human chimeric antigen receptor macrophages from peripheral blood;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫细胞治疗(CAR巨噬细胞方向)
领域共识:嵌合抗原受体T细胞(CAR-T)治疗自2017年FDA批准首个产品上市以来,已成为血液系统恶性肿瘤的突破性治疗手段,其通过基因工程改造T细胞实现对肿瘤细胞的特异性杀伤,在复发难治性B细胞白血病、淋巴瘤中展现出显著疗效。但该疗法仍存在核心局限性:对实体瘤的浸润能力不足,难以克服肿瘤免疫抑制微环境,且易引发细胞因子释放综合征等严重不良反应。在此背景下,嵌合抗原受体巨噬细胞(CAR巨噬细胞)作为新型免疫细胞治疗候选方案受到广泛关注,其天然具备肿瘤组织浸润能力、吞噬杀伤肿瘤细胞的功能,还可通过抗原提呈激活适应性免疫应答,为实体瘤治疗带来新希望。然而,慢病毒介导的人原代巨噬细胞基因转导一直是技术瓶颈,普遍存在转导效率低、细胞毒性高的问题,现有研究多依赖小鼠巨噬细胞、诱导多能干细胞(iPSC)来源巨噬细胞或腺病毒转导原代人巨噬细胞,缺乏可直接用于临床转化的慢病毒转导人外周血来源原代CAR巨噬细胞的有效方案,这一空白严重限制了CAR巨噬细胞的临床应用推进。本文正是针对这一核心问题,开发了一套优化的慢病毒转导方法,成功制备出功能性人原代CAR巨噬细胞。
2. 文献综述解析
本文综述部分围绕CAR细胞治疗的技术演进与CAR巨噬细胞的研究瓶颈展开,以“CAR-T的局限性→CAR巨噬细胞的优势→CAR巨噬细胞的技术障碍”为逻辑主线,对领域内现有研究进行分类评述。
现有研究中,CAR-T细胞治疗的关键结论是其在血液瘤中疗效确切,但实体瘤响应率低;技术优势为特异性强、靶向性高,局限性为实体瘤浸润差、免疫抑制微环境耐受、不良反应风险高。针对CAR巨噬细胞的研究,现有成果证实其具备肿瘤浸润、吞噬杀伤、抗原提呈等多重抗肿瘤功能,技术方法上多采用小鼠巨噬细胞模型进行机制研究,或利用iPSC来源巨噬细胞进行规模化制备,或通过腺病毒转导原代人巨噬细胞,但这些模型均存在临床转化的局限性:小鼠巨噬细胞与人类生理特征差异大,iPSC来源巨噬细胞存在致瘤风险,腺病毒转导则可能引发免疫原性反应。而慢病毒转导作为临床细胞治疗中常用的基因编辑工具,在人原代巨噬细胞中的应用一直受限于低转导效率和高毒性,相关研究报道极少。本文的创新价值在于首次建立了慢病毒转导人外周血单个核细胞(PBMC)来源原代巨噬细胞的优化方案,解决了转导效率与细胞毒性的核心矛盾,为CAR巨噬细胞的临床转化提供了可直接应用的技术路径。
3. 研究思路总结与详细解析
本文的研究目标是开发一套高效、低毒的慢病毒转导人PBMC来源原代巨噬细胞的方法,制备功能性CAR巨噬细胞并验证其抗肿瘤活性;核心科学问题是如何优化慢病毒转导条件以突破人原代巨噬细胞的基因转导障碍;技术路线遵循“条件优化→载体构建→功能验证→信号域优化”的闭环逻辑,逐步推进并验证研究假设。
3.1 人原代巨噬细胞分离与慢病毒转导条件优化
实验目的:筛选慢病毒转导人原代巨噬细胞的最优参数,解决转导效率低、细胞毒性高的核心问题。
方法细节:从健康志愿者捐献的全血中分离PBMC并纯化得到巨噬细胞;测试转导增强剂polybrene对巨噬细胞的毒性,比较添加与不添加polybrene的转导效果;对比1.5小时离心转导(spinoculation)与过夜孵育的转导效率;构建整合密码子优化VSV-G基因(VSVg-CO)的慢病毒颗粒,评估其转导效率;探索单核细胞分离后3天与7天的转导时机差异;测试不同启动子对巨噬细胞中基因表达的影响。
结果解读:通过细胞活力检测发现polybrene对巨噬细胞具有高毒性,去除polybrene后的转导效果显著提升;过夜孵育慢病毒的转导效率显著优于1.5小时离心转导;VSVg-CO修饰的慢病毒颗粒可进一步提高转导效率;单核细胞分离后7天进行转导的效率显著高于3天;EF1α启动子可最大化巨噬细胞中的基因表达水平。
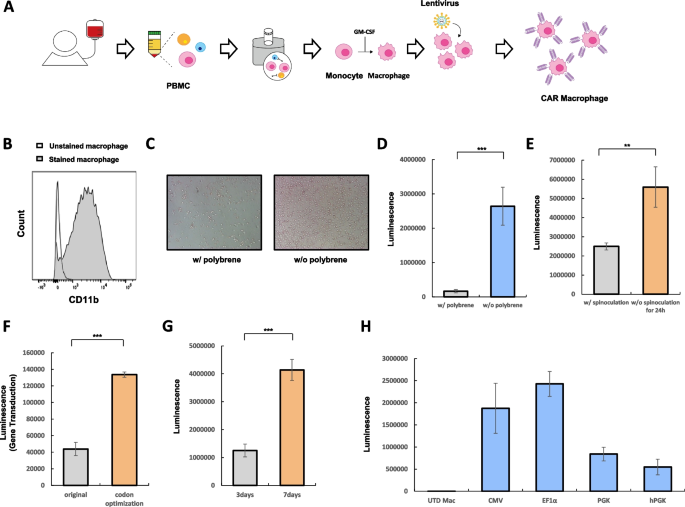
产品关联:文献未提及具体实验产品,领域常规使用PBMC分离试剂盒、慢病毒包装试剂盒、流式细胞仪(FCM)、荧光显微镜等试剂/仪器。
3.2 CAR巨噬细胞构建与表达稳定性验证
实验目的:基于优化的转导条件构建靶向CD19和cMet的CAR巨噬细胞,验证CAR表达水平与稳定性。
方法细节:构建包含CD28跨膜域、CD28胞质域及CD3ζ胞质域的CAR载体;利用优化后的慢病毒转导方案将CAR基因导入人原代巨噬细胞;通过蛋白质免疫印迹(WB)和流式细胞术检测CAR的表达水平;观察转导后巨噬细胞的形态变化;在转导后5、10、15、20天分别检测CAR的表达稳定性。
结果解读:蛋白质免疫印迹和流式细胞术结果证实CAR在巨噬细胞中成功表达;转导后巨噬细胞形态未发生异常改变,说明转导过程无明显细胞损伤;CAR表达在转导后20天内保持稳定。
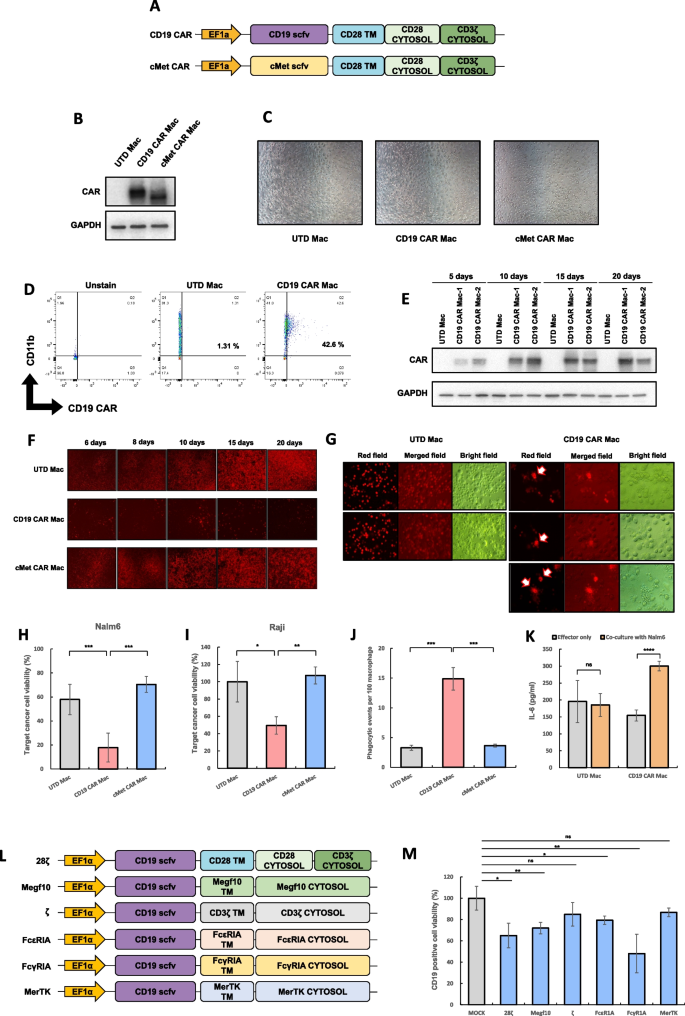
产品关联:文献未提及具体实验产品,领域常规使用CAR基因合成服务、蛋白质免疫印迹试剂盒、流式抗体等试剂/仪器。
3.3 CAR巨噬细胞抗肿瘤功能验证
实验目的:验证CAR巨噬细胞对靶肿瘤细胞的裂解、吞噬及免疫激活功能。
方法细节:将CD19 CAR巨噬细胞与CD19阳性的Nalm6-mCherry细胞、Raji-luciferase细胞共培养;通过荧光显微镜观察肿瘤细胞的裂解情况;利用荧光素酶报告基因检测肿瘤细胞的存活水平;计数每100个巨噬细胞的吞噬事件;通过ELISA检测共培养体系中IL-6的分泌水平。
结果解读:荧光显微镜下可见Nalm6细胞被CD19 CAR巨噬细胞特异性裂解;荧光素酶检测结果显示CD19 CAR巨噬细胞可有效裂解Nalm6和Raji细胞;吞噬实验显示CD19 CAR巨噬细胞的吞噬事件显著高于未转导巨噬细胞;共培养后CAR巨噬细胞分泌IL-6水平升高,表明其具备免疫激活能力。
产品关联:文献未提及具体实验产品,领域常规使用肿瘤细胞系、荧光素酶检测试剂盒、ELISA试剂盒等试剂/仪器。
3.4 CAR信号域优化筛选
实验目的:筛选CAR巨噬细胞的最优胞内信号域,进一步提升其抗肿瘤活性。
方法细节:构建包含不同胞内信号域(28ζ、Megf10、ζ、FcεRIA、FcγRIA、MerTK)的CD19 CAR载体;利用优化后的转导方案制备不同信号域的CAR巨噬细胞;将其与Nalm6-luciferase细胞共培养,通过荧光素酶检测评估肿瘤细胞裂解效率。
结果解读:荧光素酶检测结果显示,FcγRIA信号域的CAR巨噬细胞对肿瘤细胞的裂解活性最强,提示FcγRIA是CAR巨噬细胞的最优胞内信号域。
产品关联:文献未提及具体实验产品,领域常规使用基因合成服务、慢病毒转导试剂等试剂/仪器。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker包括肿瘤靶向抗原CD19、cMet,以及CAR胞内信号域FcγRIA,其中CD19、cMet为已知肿瘤治疗靶点,FcγRIA为本文筛选得到的CAR巨噬细胞最优功能信号域,研究逻辑遵循“已知靶点验证→新型功能域筛选”的完整链条。
Biomarker定位:CD19是B细胞恶性肿瘤的经典治疗Biomarker,cMet是实体瘤的潜在治疗Biomarker,本文中作为CAR的靶向抗原,筛选逻辑基于其在肿瘤细胞上的特异性表达;FcγRIA作为CAR的胞内信号域,是通过比较不同信号域的CAR巨噬细胞抗肿瘤活性筛选得到的功能性Biomarker。研究过程详述:CD19 CAR巨噬细胞的验证采用临床常用的B细胞白血病细胞系Nalm6、Raji作为靶细胞,通过共培养实验验证其裂解、吞噬活性,结果显示CD19 CAR巨噬细胞可特异性识别并杀伤CD19阳性肿瘤细胞;FcγRIA信号域的验证通过构建6种不同信号域的CAR载体,转导巨噬细胞后检测肿瘤细胞裂解效率,数据显示FcγRIA组的肿瘤细胞存活水平最低(荧光素酶活性最低),表明其抗肿瘤活性最强(文献未明确提供具体数值,基于图表趋势推测)。核心成果提炼:CD19 CAR巨噬细胞具备高效的肿瘤细胞裂解、吞噬及免疫激活功能,可作为B细胞恶性肿瘤的潜在治疗方案;FcγRIA是CAR巨噬细胞的最优胞内信号域,为CAR巨噬细胞的载体优化提供了关键依据;本研究首次证实慢病毒转导人PBMC来源原代巨噬细胞可制备功能性CAR巨噬细胞,为CAR巨噬细胞的临床转化奠定了技术基础,相关结果无明确统计学P值及样本量数据(文献未明确提供)。
