1. 领域背景与文献引入
文献英文标题:The effect of n-3 polyunsaturated fatty acids on incidence and severity of oxaliplatin induced peripheral neuropathy: a randomized controlled trial;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤学(结直肠癌化疗不良反应防治)
结直肠癌是全球发病率和死亡率较高的恶性肿瘤之一,近年来发病率呈上升趋势。奥沙利铂是晚期或转移性结直肠癌一线化疗方案的核心药物,同时也用于术后辅助治疗,但其诱导的外周神经病变(OXIPN)是主要的剂量限制性不良反应,分为急性短暂综合征和慢性感觉运动轴索性神经病变,后者通常在累积剂量达750-850mg/m²时出现,且可能在化疗结束后长期存在,严重影响患者的生活质量,甚至导致化疗剂量降低或治疗中断。领域共识:目前针对OXIPN的有效防治手段有限,已报道的干预措施中,钙镁输注对急性OXIPN有一定效果,但存在干扰化疗疗效的担忧;维生素E、谷氨酰胺等药物的预防效果未得到大样本试验证实;抗抑郁药、抗惊厥药仅能缓解症状,无法从根本上降低病变发生率。n-3多不饱和脂肪酸(PUFA)具有神经保护作用,可通过调节电压门控离子通道、减少促炎细胞因子生成发挥作用,此前研究已证实其对紫杉醇诱导的外周神经病变有预防效果,但针对奥沙利铂诱导的神经病变尚未开展相关随机对照试验,因此本研究旨在填补这一空白,评估n-3 PUFA对结直肠癌患者OXIPN发生率及严重程度的影响,为临床提供新的防治策略。
2. 文献综述解析
作者对领域内现有研究的分类维度主要包括化疗诱导外周神经病变的类型(急性vs慢性)、现有干预措施的疗效与局限性、n-3 PUFA的神经保护机制及应用场景。
现有研究显示,奥沙利铂诱导的慢性外周神经病变是影响患者长期生活质量的关键问题,其发病机制可能与离子通道功能异常、炎症反应激活、轴突损伤等有关;现有干预措施中,钙镁输注虽能减轻急性神经病变,但对慢性病变效果不佳,且可能影响化疗疗效;维生素E、谷氨酰胺等营养补充剂的预防作用未得到一致证实;抗抑郁药、抗惊厥药仅能缓解疼痛等症状,无法阻止病变进展。n-3 PUFA的神经保护机制已被证实包括调节钠、钙等离子通道活性、抑制促炎细胞因子生成、促进轴突再生等,且在紫杉醇诱导的外周神经病变中显示出明确的预防效果,但针对奥沙利铂诱导的神经病变,尚无随机对照试验验证其疗效。
通过对比现有研究的未解决问题,本研究的创新价值在于首次开展随机双盲安慰剂对照试验,系统评估n-3 PUFA对结直肠癌患者奥沙利铂诱导慢性外周神经病变的预防作用,同时探讨其潜在的抗炎机制,为OXIPN的防治提供新的循证医学证据,具有重要的临床意义。
3. 研究思路总结与详细解析
本研究为随机双盲安慰剂对照试验,研究目标是评估n-3 PUFA对结直肠癌患者奥沙利铂诱导外周神经病变发生率及严重程度的影响,核心科学问题是n-3 PUFA是否能通过调节炎症反应和神经传导功能发挥神经保护作用,技术路线遵循“患者入组→随机分组→干预实施→多维度评估→结果分析”的闭环逻辑,确保研究结果的客观性和可靠性。
3.1 研究对象筛选与分组
实验目的是确定符合纳入标准的结直肠癌患者,并完成随机分组以保证两组基线特征均衡。方法细节为:纳入2012年2月至2015年1月期间,在Tabriz大学医学院接受奥沙利铂联合卡培他滨化疗的III期结直肠癌患者,年龄20-85岁,WHO体力状况评分0-1分,肝肾功能正常;排除存在预存外周神经病变(如糖尿病、酒精性神经病变等)、使用过其他神经毒性药物或营养补充剂的患者。采用随机分配软件(RAS 1.0.0)进行区组随机化,将患者按1:1比例分为n-3 PUFA组和安慰剂组,仅随机化协调员知晓分组信息。结果解读:最终纳入71例患者,其中n-3 PUFA组36例,安慰剂组35例,两组患者在性别、年龄、BMI等基线特征上无统计学差异(P值分别为0.477、0.816、0.806),确保了两组的可比性。研究流程图如下:
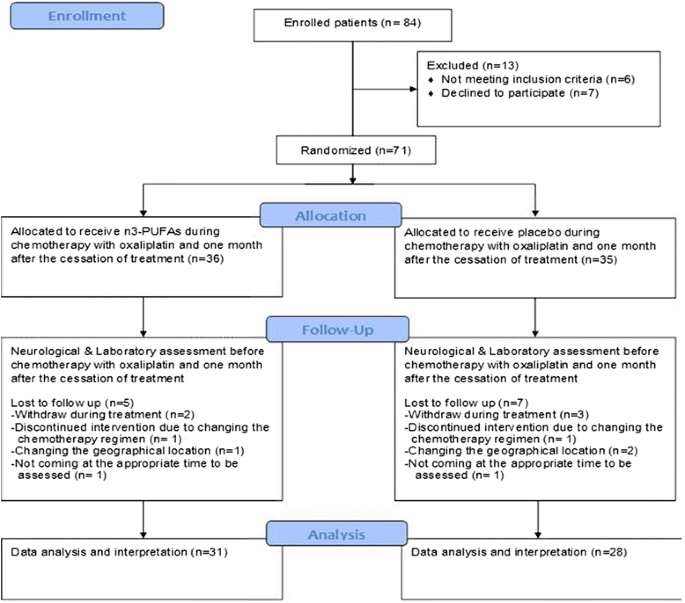
产品关联:文献未提及具体实验产品,领域常规使用随机分组软件、电子病历系统等进行患者筛选与分组。
3.2 干预方案实施
实验目的是为两组患者提供标准化的干预措施,确保干预的一致性和盲法的维持。方法细节为:n-3 PUFA组患者每日三次服用640mg的n-3 PUFA软胶囊(含54% DHA、10% EPA),从化疗开始持续至化疗结束后1个月;安慰剂组服用外观、颜色一致的向日葵油软胶囊,干预时间与n-3 PUFA组相同。所有患者均接受奥沙利铂(130mg/m²,静脉输注2小时,第1天)联合卡培他滨(1000mg/m²,每日两次,第1-4天)的化疗方案,每3周为一个周期,共8个周期。结果解读:两组患者均按方案完成干预,无严重干预相关不良反应,仅少数患者出现轻微胃肠道不适(如恶心),干预耐受性良好。产品关联:实验所用关键产品:n-3 PUFA软胶囊(Mor DHA Mini I.Q. Minami Nutrition NV,比利时)、安慰剂软胶囊(Dana Pharma,伊朗)。
3.3 外周神经病变评估
实验目的是准确评估两组患者OXIPN的发生率及严重程度。方法细节为:在化疗开始前和化疗结束后1个月,由不知情分组情况的神经科医师采用简化总神经病变评分(TNSr)进行评估,该评分包含主观感觉症状、针刺觉、深腱反射、腓肠神经和腓总神经振幅等7项参数,每项评分0-4分,总评分0-28分,对应OXIPN严重程度:0分为无病变,1-10分为轻度,11-19分为中度,20-28分为重度。结果解读:化疗结束后1个月,n-3 PUFA组47%(17/36)的患者未发生OXIPN,42%(15/36)为轻度,3%(1/36)为中度,8%(3/36)为重度;安慰剂组仅11%(4/35)的患者未发生病变,57%(20/35)为轻度,20%(7/35)为中度,12%(4/35)为重度。两组OXIPN发生率存在显著差异(OR=0.14,95%CI 0.04-0.49,P=0.002),n-3 PUFA组发生病变的风险降低86%;严重程度也存在显著差异(B=-1.61,95%CI -2.59至-0.62,P=0.001),n-3 PUFA组病变严重程度显著低于安慰剂组。两组OXIPN分布情况如下:
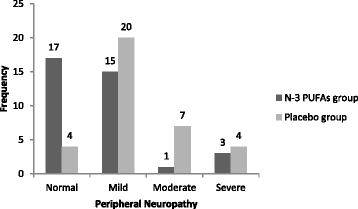
产品关联:文献未提及具体实验产品,领域常规使用标准化神经功能评分量表进行评估。
3.4 神经电生理检测
实验目的是客观评估两组患者的神经传导功能变化。方法细节为:在化疗开始前和化疗结束后1个月,采用Nicolet/VIASYS Viking Quest EMG Machine进行单侧(右侧)神经传导检测,检测参数包括胫神经、腓总神经、尺神经的远端运动潜伏期(DML)、复合肌肉动作电位振幅(a-CMAP)、运动传导速度,以及腓肠神经、尺神经的感觉动作电位振幅(a-SAP)、感觉传导速度(逆向法),检测时远端皮肤温度控制在32-34℃。结果解读:化疗结束后1个月,n-3 PUFA组胫神经、尺神经的a-CMAP较基线升高,而安慰剂组则降低;腓总神经a-CMAP在n-3 PUFA组的升高幅度显著大于安慰剂组。感觉神经方面,两组a-SAP均较基线降低,但安慰剂组的降低幅度显著大于n-3 PUFA组(腓肠神经:-100.00% vs -36.68%;尺神经:-42.06% vs -18.28%),提示n-3 PUFA可减轻奥沙利铂对神经传导功能的损伤。产品关联:实验所用关键产品:Nicolet/VIASYS Viking Quest EMG Machine。
3.5 炎症因子检测
实验目的是探讨n-3 PUFA发挥神经保护作用的潜在机制,检测血清炎症因子的变化。方法细节为:在化疗开始前和化疗结束后1个月,采集患者外周血血清,采用Human IL-6 Platinum ELISA试剂盒、Human TNF alpha Platinum ELISA试剂盒(eBioscience,美国)检测白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)水平,采用Minineph™ Human试剂盒(英国)检测高敏C反应蛋白(hs-CRP)水平。结果解读:化疗结束后1个月,n-3 PUFA组血清IL-6水平降低20.91%,TNF-α水平降低12.50%,而安慰剂组这两种因子的水平均升高;两组hs-CRP水平均降低,但安慰剂组的降低幅度更大(61.02% vs 55.21%),不过上述差异均无统计学意义,推测可能与样本量较小、干预剂量或时间较短有关。产品关联:实验所用关键产品:Human IL-6 Platinum ELISA试剂盒、Human TNF alpha Platinum ELISA试剂盒(eBioscience,美国)、Minineph™ Human试剂盒(英国)。
3.6 统计学分析
实验目的是对研究数据进行科学分析,验证研究假设。方法细节为:采用SPSS软件进行统计分析,定量资料以均数±标准差表示,定性资料以频率(百分比)表示;采用协方差分析比较神经传导检测结果,调整基线值;采用逻辑回归分析比较OXIPN发生率,计算比值比(OR)及95%置信区间(CI);采用有序回归分析比较OXIPN严重程度;所有检验均为双侧检验,显著性水平设为0.05;采用多重插补法处理缺失数据,按意向性治疗(ITT)原则进行分析。结果解读:统计分析结果显示,n-3 PUFA组OXIPN的发生率及严重程度均显著低于安慰剂组,差异具有统计学意义,验证了n-3 PUFA的神经保护作用。产品关联:文献未提及具体实验产品,领域常规使用SPSS等统计软件进行数据分析。
4. Biomarker研究及发现成果
本研究涉及的Biomarker主要包括血清炎症细胞因子(IL-6、TNF-α、hs-CRP)和神经电生理指标(a-CMAP、a-SAP),筛选与验证逻辑为通过化疗前后的动态检测,对比两组指标的变化,探讨其与n-3 PUFA神经保护作用的关联。
研究过程中,血清炎症因子Biomarker来源于患者外周血血清,验证方法包括酶联免疫吸附试验(ELISA)和免疫比浊法;神经电生理指标Biomarker通过神经传导检测获取。具体数据显示,化疗结束后1个月,n-3 PUFA组血清IL-6、TNF-α水平较基线降低,而安慰剂组升高,但差异无统计学意义;神经电生理指标方面,n-3 PUFA组运动神经a-CMAP升高,感觉神经a-SAP降低幅度显著小于安慰剂组,其中腓肠神经a-SAP的变化与神经病变的严重程度相关,可作为客观评估神经损伤的指标。
核心成果方面,本研究未发现具有统计学意义的特异性炎症因子Biomarker,但炎症因子的变化趋势提示n-3 PUFA可能通过抗炎机制发挥神经保护作用;神经电生理指标a-CMAP、a-SAP可作为客观评估OXIPN严重程度及干预效果的生物标志物,其中腓肠神经a-SAP的降低幅度可预测神经病变的预后。本研究的核心临床成果是证实n-3 PUFA可显著降低结直肠癌患者奥沙利铂诱导外周神经病变的发生率(OR=0.14,95%CI 0.04-0.49,P=0.002)和严重程度(B=-1.61,95%CI -2.59至-0.62,P=0.001),且安全性良好,为OXIPN的防治提供了新的有效策略。
