1. 领域背景与文献引入
文献英文标题:THSD4 is a novel mediator of T cell exclusion and anti-PD-1 resistance in hormone receptor-positive breast cancer;发表期刊:Biomarker Research;影响因子:未公开;研究领域:乳腺癌免疫治疗、肿瘤生物标志物研究。
乳腺癌是女性最常见的恶性肿瘤,其中激素受体阳性(HR+)乳腺癌约占所有病例的70%。免疫检查点抑制剂(ICI)中的抗程序性死亡蛋白1(PD-1)抑制剂帕博利珠单抗已在三阴性乳腺癌(TNBC)中显示出明确疗效,但在HR+乳腺癌亚型中的获益十分有限。领域共识:HR+乳腺癌免疫治疗耐药的核心机制之一是“冷”肿瘤免疫微环境,其特征为肿瘤浸润淋巴细胞(TILs)数量少,导致ICI无法有效激活抗肿瘤免疫反应。目前,介导HR+乳腺癌免疫排斥和ICI耐药的特异性遗传决定因素尚未完全明确,缺乏可用于患者分层和治疗靶点的新型生物标志物,这一空白限制了HR+乳腺癌免疫治疗的进一步优化。针对这一临床痛点,本研究通过整合多组学与临床数据,筛选并验证了THSD4作为HR+乳腺癌中T细胞排斥和抗PD-1耐药的新型介导因子,为该领域提供了新的研究方向。
2. 文献综述解析
本文针对HR+乳腺癌抗PD-1治疗耐药的核心问题,系统梳理了现有研究的局限与空白。作者指出,既往研究虽已证实冷肿瘤微环境是ICI耐药的关键因素,但多聚焦于已知免疫调控通路,未充分结合多组学与临床数据挖掘特异性的新型介导因子。现有研究的技术方法优势在于利用公共数据库进行大规模分析,但局限性在于部分研究缺乏临床样本验证或功能实验验证,无法明确标志物的因果关系。
通过对比低T细胞浸润肿瘤与帕博利珠单抗耐药患者的基因表达谱,本文首次锁定THSD4为核心候选基因,其创新价值在于突破了现有研究的局限,从相关性研究推进到功能验证,明确了THSD4在HR+乳腺癌中介导T细胞排斥和抗PD-1耐药的关键作用,填补了HR+乳腺癌免疫排斥机制研究的空白,为该领域提供了新的研究靶点与生物标志物。
3. 研究思路总结与详细解析
本文整体研究思路遵循“数据筛选-临床验证-功能机制”的闭环逻辑,首先通过多组学数据分析筛选介导T细胞排斥和抗PD-1耐药的候选基因,随后利用三个本地临床队列验证THSD4表达与T细胞浸润、患者预后的关联,最后通过小鼠肿瘤模型明确THSD4的功能作用及机制,为HR+乳腺癌免疫治疗耐药提供了完整的证据链。
3.1 多组学数据筛选候选生物标志物
实验目的:筛选介导HR+乳腺癌T细胞排斥和抗PD-1耐药的特异性遗传因子。方法细节:采用CIBERSORTx转录组反卷积工具分析癌症基因组图谱(TCGA)中HR+乳腺癌的RNA测序数据,识别与低T细胞浸润相关的基因;同时整合I-SPY2临床试验中帕博利珠单抗治疗组的基因表达数据,对比病理完全缓解(pCR)与非pCR患者的基因表达差异,交叉筛选核心候选基因。结果解读:分析结果显示,THSD4是排名首位的候选基因,在低T细胞浸润的肿瘤组织中表达显著上调,且在帕博利珠单抗耐药的HR+乳腺癌患者中表达水平显著高于敏感患者(n=40,P<0.01)。产品关联:文献未提及具体实验产品,领域常规使用CIBERSORTx生物信息学分析工具、RNA测序平台及相关数据分析软件。
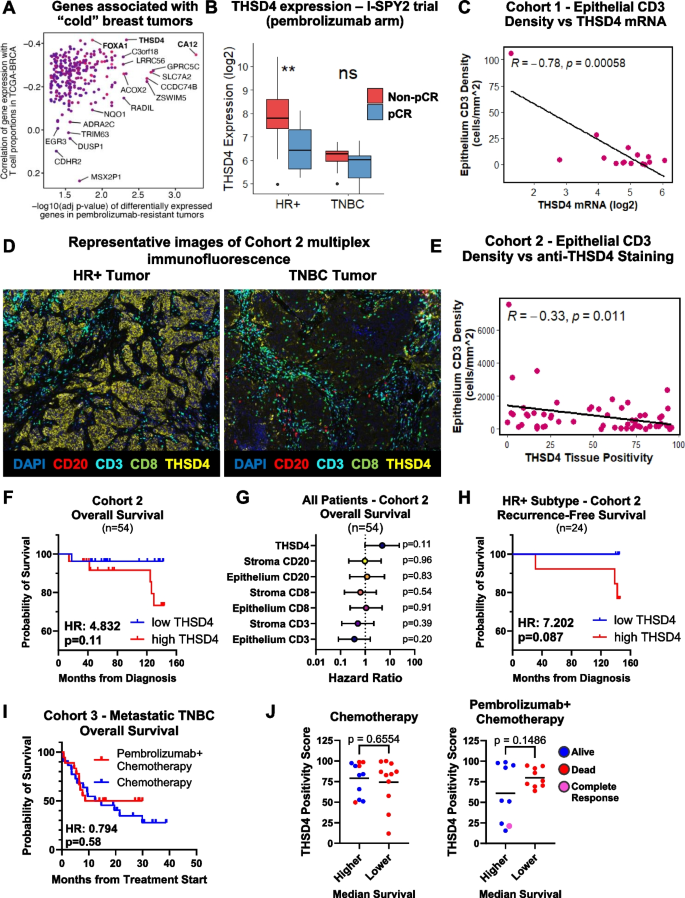
3.2 临床样本验证THSD4与T细胞浸润及预后的关联
实验目的:验证THSD4在临床样本中的表达与肿瘤免疫微环境及患者预后的相关性。方法细节:利用三个本地临床队列的乳腺癌样本,通过RNA测序检测THSD4的mRNA表达水平,采用多重免疫荧光染色检测THSD4蛋白表达及肿瘤上皮内CD3+T细胞密度,同时结合患者临床随访数据进行生存分析。结果解读:在队列1的15例HR+乳腺癌样本中,THSD4的mRNA表达水平与肿瘤上皮内CD3+T细胞密度呈显著负相关(P<0.05);队列2的58例早期乳腺癌样本中,THSD4蛋白高表达的患者总生存期显著缩短(n=54,HR=2.8,P<0.05),其中HR+患者的无复发生存期更差(n=24,HR=3.2,P<0.05);队列3的40例转移性TNBC样本中,帕博利珠单抗治疗后生存期较好的患者THSD4蛋白表达水平更低(接近统计学显著性)。产品关联:文献未提及具体实验产品,领域常规使用多重免疫荧光染色试剂盒、RNA测序试剂、生存分析软件等。
3.3 小鼠模型验证THSD4的功能作用
实验目的:明确THSD4在介导抗PD-1耐药中的功能作用及机制。方法细节:构建HR+TS/A和TNBC 4T1小鼠乳腺癌细胞系,采用shRNA敲低Thsd4基因表达,将细胞原位接种于Balb/c小鼠,待肿瘤可触及后给予抗PD-1抗体治疗,监测肿瘤生长情况,通过流式细胞术检测肿瘤内免疫细胞浸润,采用天狼星红染色检测肿瘤胶原纤维组成。结果解读:HR+TS/A细胞系的Thsd4表达水平显著高于TNBC 4T1细胞系(n=4,P<0.01);Thsd4敲低联合抗PD-1治疗显著抑制TS/A肿瘤生长,肿瘤体积和重量均显著降低(n=5,P<0.001);流式细胞术结果显示,Thsd4敲低联合抗PD-1治疗后,肿瘤内CD3+T细胞、细胞毒性CD8+T细胞及PD-1+CD8+T细胞比例显著增加(n=5,P<0.01);天狼星红染色显示,Thsd4敲低联合抗PD-1治疗改变了肿瘤胶原纤维组成,总胶原含量增加,成熟纤维比例上升(n=5,P<0.05)。产品关联:文献未提及具体实验产品,领域常规使用慢病毒载体构建基因敲低细胞系、抗PD-1抗体、流式细胞术检测试剂、天狼星红染色试剂盒等。
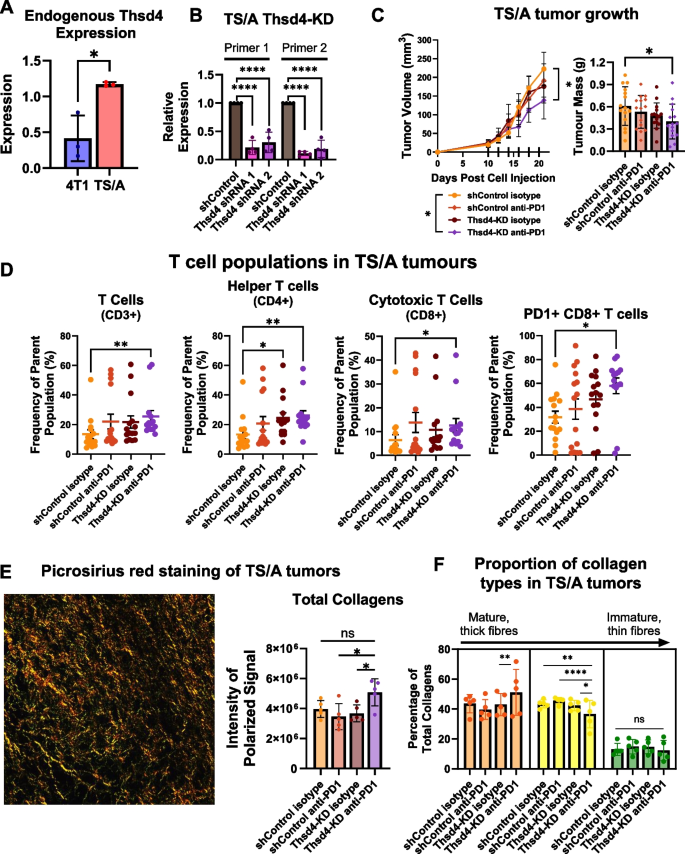
推测:THSD4可能通过调控肿瘤细胞外基质(ECM)重塑影响T细胞的肿瘤浸润能力,具体分子机制需后续实验进一步明确。
4. Biomarker研究及发现成果解析
本文鉴定的生物标志物THSD4是HR+乳腺癌中T细胞排斥和抗PD-1耐药的新型介导因子,具有重要的预后价值和治疗潜力。
Biomarker定位:THSD4属于基因/蛋白类生物标志物,筛选与验证逻辑为“公共数据库筛选→临床样本验证→动物模型功能验证”的完整链条,从相关性研究推进到因果关系验证。研究过程详述:THSD4来源于临床乳腺癌组织样本,验证方法包括RNA测序、多重免疫荧光染色、qRT-PCR、流式细胞术及动物实验;在HR+乳腺癌中,THSD4高表达与肿瘤上皮内T细胞浸润负相关,生存分析显示高THSD4表达患者的总生存期风险比(HR)为2.8(n=54,P<0.05),无复发生存期风险比为3.2(n=24,P<0.05),提示其具有良好的预后特异性。核心成果提炼:THSD4是首次在HR+乳腺癌中被鉴定的介导T细胞排斥和抗PD-1耐药的生物标志物,其功能机制与肿瘤细胞外基质(ECM)重塑相关,创新性在于明确了THSD4的因果作用,而非仅相关性,为HR+乳腺癌的免疫治疗患者分层和靶点开发提供了新方向。目前文献未提供THSD4的ROC曲线敏感性与特异性数据,需进一步大样本研究验证其诊断效能。
