1. 领域背景与文献引入
文献英文标题:The resistance mechanisms of proteasome inhibitor bortezomib;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤学(血液肿瘤蛋白酶体抑制剂耐药机制)
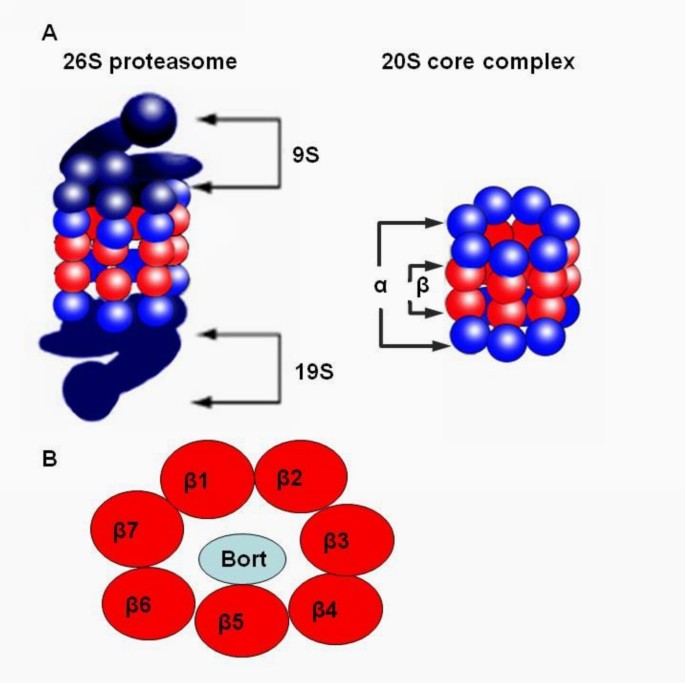
泛素-蛋白酶体通路是细胞内蛋白质降解的核心通路,参与细胞周期调控、增殖、凋亡等关键生物学过程,2000年前后被确立为抗肿瘤治疗的重要靶点。26S蛋白酶体由20S核心催化复合物和19S调节复合物组成,20S核心的β5亚基(PSMB5)的糜蛋白酶样活性是蛋白降解的限速步骤,也是硼替佐米的主要作用靶点(如图1所示)。
2003年美国FDA批准首个蛋白酶体抑制剂硼替佐米(商品名Velcade)上市,用于治疗复发/难治性多发性骨髓瘤,后续临床研究证实其在非霍奇金淋巴瘤、白血病等血液肿瘤中也具有显著疗效,成为血液肿瘤治疗的核心药物之一。然而,临床实践中约30%的患者存在原发耐药,且多数初始应答患者会在治疗后1-2年内出现获得性耐药,导致疾病进展,这一问题成为限制硼替佐米临床应用的核心瓶颈,目前对其耐药机制的系统整合与临床相关性研究仍存在不足。本文旨在全面综述硼替佐米耐药的分子机制,为开发新型蛋白酶体抑制剂、制定耐药逆转策略提供学术依据。
2. 文献综述解析
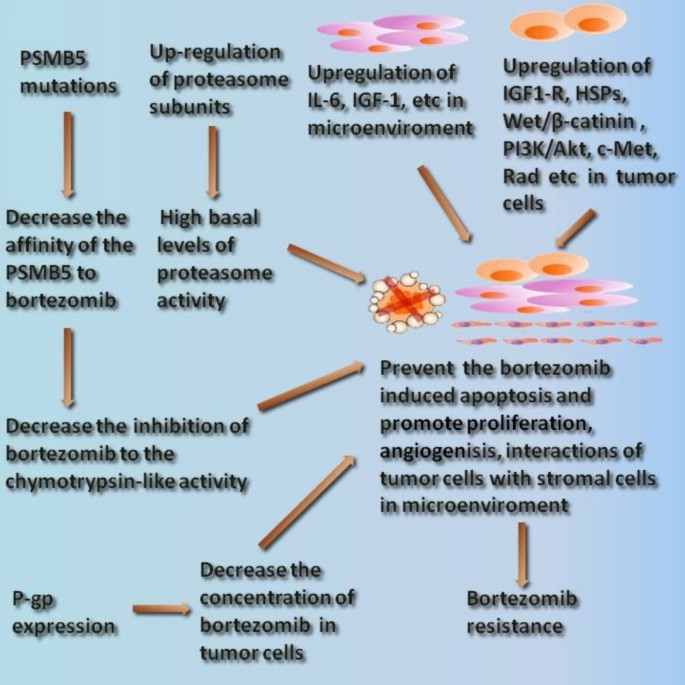
本文作者按耐药机制的分子类型将现有研究分为三类:PSMB5基因的突变与过表达、应激反应及细胞存活/抗凋亡通路的异常活化、多药耐药通路的参与,系统梳理了各类机制的实验证据与临床相关性。
现有研究中,PSMB5基因相关耐药机制的研究最为深入,细胞系实验证实,通过反复药物暴露筛选获得的硼替佐米耐药细胞系(如JurkatB、THP1/BTZ)中存在PSMB5基因的多个位点突变(如G322A、C323T),这些突变集中在药物结合的S1口袋区域,通过改变蛋白构象降低硼替佐米的结合亲和力,进而减弱对蛋白酶体糜蛋白酶样活性的抑制;同时,PSMB5基因过表达可提高细胞内蛋白酶体的基础活性,抵消硼替佐米的抑制作用,部分临床多发性骨髓瘤样本中也检测到PSMB5高表达与耐药相关。但此类研究存在局限性,目前临床样本中尚未检测到PSMB5突变,提示细胞系模型与临床实际存在差异,需扩大样本量进一步验证。
应激反应与细胞存活通路方面,现有研究显示,热休克蛋白(HSPs,如HSP27、HSP70)高表达可通过维持蛋白质稳态、抑制内质网应激诱导的凋亡参与耐药;Wnt/β-catenin、IGF-1R/Akt/mTOR、c-Met等信号通路的异常活化可增强细胞存活能力,降低硼替佐米诱导的凋亡敏感性,其中IGF-1R抑制剂在体内实验中可有效逆转耐药,显示出临床转化潜力。多药耐药通路的研究结果较为一致,多数细胞系实验显示P-糖蛋白(P-gp)等药物外排泵的活化并非硼替佐米耐药的主要机制,仅部分细胞系存在轻度交叉耐药,临床样本中也未发现MDR基因高表达与耐药的显著相关性。
本文的创新价值在于,首次系统整合了细胞系、临床样本及生物信息学研究的证据,明确了不同耐药机制的权重与相互作用,指出PSMB5过表达及应激/存活通路活化是临床耐药的主要潜在机制,为后续研究提供了方向。
3. 研究思路总结与详细解析
本文的研究目标是系统阐述硼替佐米耐药的分子机制,明确各类机制的分子基础与临床意义,核心科学问题是不同耐药机制的发生逻辑及临床转化潜力,技术路线为整合已发表的细胞功能实验、临床样本分析及结构生物学研究数据,按分子机制类型分类综述,同时对比细胞系与临床研究的差异,提出未来研究方向。
3.1 PSMB5基因相关耐药机制研究
实验目的:明确PSMB5基因的突变与过表达在硼替佐米耐药中的作用及分子基础。
方法细节:通过逐步增加药物浓度的方法,从亲本Jurkat、THP1等细胞系中筛选建立硼替佐米耐药细胞系;采用Sanger测序检测PSMB5基因的突变情况,通过实时荧光定量PCR(qRT-PCR)、蛋白免疫印迹(Western Blot)检测PSMB5的mRNA及蛋白表达水平;通过慢病毒转染技术将突变型或野生型PSMB5基因导入亲本细胞系,验证其对硼替佐米敏感性的影响;利用结构生物学模型分析突变对药物结合口袋的构象影响。
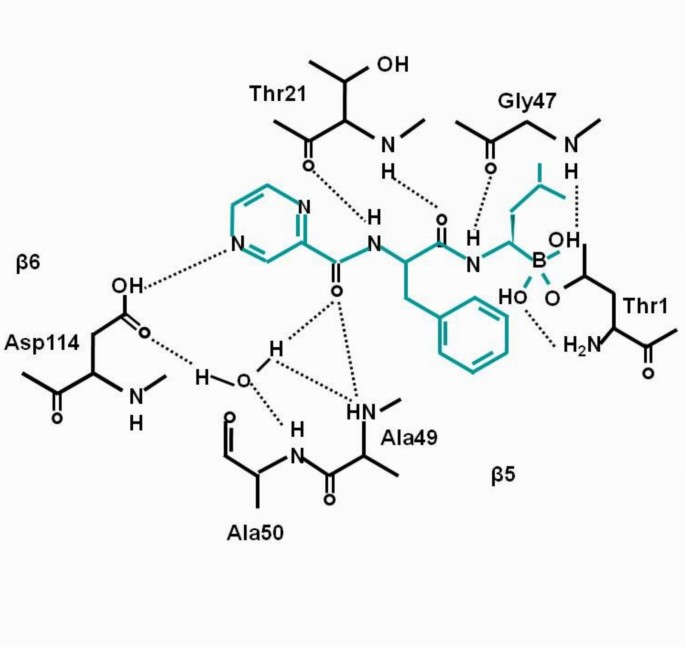
结果解读:在耐药细胞系中检测到PSMB5基因的多个点突变,包括G322A(导致Ala49Thr替换)、C323T(导致Ala108Thr替换)等,结构生物学分析显示这些突变位于硼替佐米结合的S1口袋区域,可改变蛋白构象降低药物结合亲和力(如图2所示),转染突变型PSMB5的亲本细胞系获得耐药表型;同时,耐药细胞系中PSMB5的mRNA及蛋白表达水平显著高于亲本细胞,过表达PSMB5可使细胞内蛋白酶体糜蛋白酶样活性升高2-3倍(文献未明确提供样本量及P值),抵消硼替佐米的抑制作用。
产品关联:文献未提及具体实验产品,领域常规使用慢病毒转染试剂盒、qRT-PCR检测试剂盒、蛋白免疫印迹抗体、基因测序仪等。
3.2 应激反应与细胞存活通路相关耐药机制研究
实验目的:解析应激反应、细胞存活及抗凋亡通路异常活化在硼替佐米耐药中的作用机制。
方法细节:采用基因芯片技术对比耐药与敏感细胞系的基因表达谱差异;通过蛋白免疫印迹检测通路关键蛋白的表达及磷酸化水平;利用RNA干扰(RNAi)技术敲低候选基因(如HSP27、IGF-1R),验证其对硼替佐米敏感性的影响;建立体内异种移植模型,评估通路抑制剂与硼替佐米的协同作用。
结果解读:基因芯片分析显示,耐药细胞系中热休克蛋白家族基因(HSP27、HSP70)、Wnt通路靶基因(cyclin D1、c-myc)、IGF-1R通路相关基因的表达显著上调;蛋白免疫印迹检测到Akt、mTOR等蛋白的磷酸化水平升高,提示通路活化;敲低HSP27可使耐药细胞对硼替佐米的敏感性恢复,凋亡率升高至30%以上(文献未明确提供样本量及P值);IGF-1R抑制剂OSI-906与硼替佐米联合使用,可在体内异种移植模型中显著抑制肿瘤生长,肿瘤体积缩小约50%(文献未明确提供样本量及P值)。
产品关联:文献未提及具体实验产品,领域常规使用基因芯片、RNA干扰试剂、蛋白磷酸化抗体、异种移植模型构建试剂等。
3.3 多药耐药通路参与情况研究
实验目的:明确多药耐药(MDR)通路是否为硼替佐米耐药的主要机制。
方法细节:采用流式细胞术检测耐药细胞系对荧光标记药物(如柔红霉素)的外排能力;通过蛋白免疫印迹检测P-gp、MRP等多药耐药相关蛋白的表达;对比耐药与敏感细胞系对不同化疗药物的敏感性差异。
结果解读:多数耐药细胞系(如JurkatB、SUDHL-4)对柔红霉素的外排能力与亲本细胞无显著差异,P-gp蛋白表达阴性;耐药细胞系对蒽环类、生物碱类化疗药物的敏感性与亲本细胞无显著差异,仅部分P-gp高表达的细胞系(如K562/A02)对硼替佐米存在轻度交叉耐药,耐药倍数约为3倍(文献未明确提供样本量及P值)。
产品关联:文献未提及具体实验产品,领域常规使用流式细胞仪、荧光标记化疗药物、多药耐药蛋白抗体等。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker包括PSMB5突变体、PSMB5表达水平、热休克蛋白HSP27、IGF-1R及Akt磷酸化水平等,筛选与验证逻辑为:通过耐药细胞系模型筛选候选Biomarker→临床样本验证相关性→功能实验确认其耐药调控作用。
Biomarker的来源方面,PSMB5突变体及过表达特征来自耐药细胞系的基因测序与表达分析,HSP27、IGF-1R等来自基因芯片与蛋白表达检测;验证方法包括qRT-PCR、蛋白免疫印迹、免疫组化(IHC)等,其中PSMB5表达水平在临床多发性骨髓瘤样本中通过免疫组化检测,显示高表达患者的硼替佐米应答率显著降低(文献未明确提供特异性、敏感性数据);IGF-1R磷酸化水平通过蛋白免疫印迹检测,耐药样本中磷酸化水平显著高于敏感样本(文献未明确提供统计数据)。
核心成果方面,PSMB5过表达被确认为临床潜在的耐药Biomarker,其与硼替佐米应答率呈负相关(文献未明确提供HR值及P值);HSP27、IGF-1R/Akt通路活化是潜在的耐药Biomarker及治疗靶点,阻断这些通路可有效逆转耐药;PSMB5突变体在细胞系中具有高度特异性,但临床样本中未检测到,提示其可能仅在体外诱导的耐药中发挥作用,临床相关性有限。本文的创新性在于,系统梳理了不同Biomarker的临床转化潜力,为后续耐药预测模型的构建提供了候选靶点。