1. 领域背景与文献引入
文献英文标题:CAR-T cell therapy followed by allogenic hematopoietic stem cell transplantation yielded comparable outcome between Ph like ALL and other high-risk ALL;发表期刊:Biomarker Research;影响因子:未公开;研究领域:急性淋巴细胞白血病免疫治疗与造血干细胞移植。
Ph样急性淋巴细胞白血病(Ph-like ALL)是B细胞急性淋巴细胞白血病(B-ALL)的高危亚型,因对传统化疗耐药且缺乏有效靶向药物,既往被认为预后显著差于其他B-ALL亚型,传统化疗下5年总生存率仅24%。嵌合抗原受体T细胞(CAR-T)治疗已在复发难治B-ALL中取得显著疗效,可诱导深度缓解,但目前关于CAR-T治疗能否改变Ph-like ALL不良预后的临床数据十分有限,成为领域内未解决的核心问题。本研究针对这一空白,通过回顾性分析接受CAR-T治疗后行异基因造血干细胞移植的患者数据,评估该治疗策略对Ph-like ALL的疗效及预后价值,为Ph-like ALL的临床治疗提供新的循证依据。
2. 文献综述解析
作者以Ph-like ALL的临床困境为切入点,先系统梳理该亚型的分子分类、传统治疗的局限性,再结合CAR-T在B-ALL中的应用现状,明确当前领域缺乏CAR-T联合异基因造血干细胞移植对Ph-like ALL疗效的研究数据这一核心空白。
现有研究的关键结论包括,Ph-like ALL可分为JAK-STAT激活型、ABL1类重排型等分子亚型,多数患者对传统化疗耐药,部分患者即使接受酪氨酸激酶抑制剂(TKI)治疗也存在耐药情况;CAR-T治疗在复发难治B-ALL中可实现较高的完全缓解率,但针对Ph-like ALL的研究多为小样本或个案报道,缺乏大样本的预后分析数据。现有研究的技术方法优势在于可通过二代测序、荧光原位杂交(FISH)等技术精准分型Ph-like ALL,但局限性在于未关注CAR-T联合异基因造血干细胞移植这一治疗策略对Ph-like ALL的预后影响,样本量不足导致结论的循证医学证据等级较低。本研究的创新价值在于首次在包含17例Ph-like ALL的较大样本中,系统评估CAR-T联合异基因造血干细胞移植的疗效,通过与Ph+ ALL及其他高危B-ALL患者的对比,证实该治疗策略可使Ph-like ALL患者获得与其他高危亚型相当的预后,填补了领域内关于Ph-like ALL免疫联合移植治疗的研究空白。
3. 研究思路总结与详细解析
本研究的整体研究目标是评估CAR-T细胞治疗联合异基因造血干细胞移植对Ph-like ALL患者的疗效及预后,核心科学问题是该治疗策略能否克服Ph-like ALL的不良预后,技术路线为回顾性筛选符合入组标准的患者,收集临床基线数据、CAR-T治疗反应及预后数据,通过统计学分析比较三组患者的疗效差异,最终得出研究结论。
3.1 患者入组与基线特征分析
实验目的是明确Ph-like ALL、Ph+ ALL及其他B-ALL三组患者的临床基线差异,为后续疗效比较提供基础。方法细节为回顾性筛选2016年3月至2021年1月在苏州大学第一附属医院接受CAR-T细胞治疗后行异基因造血干细胞移植的患者,最终纳入17例Ph-like ALL、23例Ph+ ALL和51例其他B-ALL患者,收集患者年龄、诊断时白细胞计数、CAR-T输注前疾病状态等基线数据,采用卡方检验或方差分析进行统计学比较。结果解读显示,Ph-like组和其他B-ALL组患者年龄显著小于Ph+组(P=0.001);Ph-like组和Ph+组诊断时白细胞计数显著高于其他B-ALL组(P=0.025);Ph-like组CAR-T输注前处于活动性疾病的患者比例为64.7%,Ph+组为39.1%,其他B-ALL组为62.7%,三组间该比例无显著统计学差异(P=0.085)。产品关联:文献未提及具体实验产品,领域常规使用流式细胞仪、荧光原位杂交试剂盒、二代测序平台等试剂/仪器。
3.2 CAR-T治疗疗效评估
实验目的是评估三组患者对CAR-T细胞治疗的反应率,明确CAR-T对Ph-like ALL的诱导缓解效果。方法细节为采用流式细胞术检测微小残留病(MRD),定义MRD阴性为骨髓中白血病细胞比例<0.01%,评估患者的完全缓解(CR)率及MRD阴性完全缓解率。结果解读显示,Ph-like组CAR-T治疗总反应率为94.1%(16/17,n=17),其中MRD阴性完全缓解率为64.7%(11/17,n=17);Ph+组总反应率为95.6%(22/23,n=23),MRD阴性完全缓解率为60.9%(14/23,n=23);其他B-ALL组总反应率为98.0%(50/51,n=51),MRD阴性完全缓解率为54.9%(28/51,n=51),三组间总反应率及MRD阴性完全缓解率均无显著统计学差异。产品关联:实验所用关键产品:上海优卡迪生物医药科技有限公司的抗CD19 CAR-T细胞、抗CD19/CD22双靶点CAR-T细胞。
3.3 长期生存预后分析
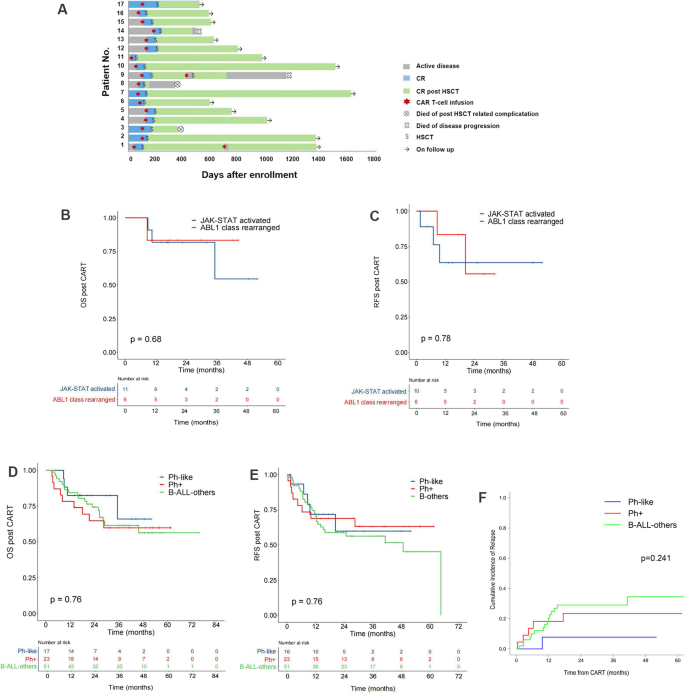
实验目的是比较三组患者接受CAR-T联合异基因造血干细胞移植后的长期生存预后,明确Ph-like ALL患者的预后是否与其他高危亚型相当。方法细节为采用Kaplan-Meier法绘制生存曲线,分析3年总生存率(OS)、无复发生存率(RFS)及累积复发率(CIR),通过Log-rank检验比较三组间的统计学差异。结果解读显示,Ph-like组3年总生存率为65.9%±16.5%(n=17,P=0.758),Ph+组为59.7%±10.5%(n=23,P=0.758),其他B-ALL组为61.6%±7.3%(n=51,P=0.758);三组3年无复发生存率分别为59.8%±14.8%(n=17,P=0.764)、63.1%±10.5%(n=23,P=0.764)和56.3%±7.1%(n=51,P=0.764);3年累积复发率分别为7.8%±0.6%(n=17,P=0.241)、23.4%±0.9%(n=23,P=0.241)和29.0%±0.4%(n=51,P=0.241),三组间上述预后指标均无显著统计学差异。此外,Ph-like ALL亚组中,JAK-STAT激活型与ABL1类重排型患者的3年总生存率及无复发生存率也无显著差异。
4. Biomarker研究及发现成果解析
本研究涉及的生物标志物主要包括Ph-like ALL的分子亚型、微小残留病(MRD),旨在明确这些标志物与CAR-T联合异基因造血干细胞移植预后的关联。
Biomarker定位:Ph-like ALL的分子亚型包括JAK-STAT激活型、ABL1类重排型等,筛选逻辑为通过靶向DNA二代测序、RNA测序及荧光原位杂交(FISH)技术从患者骨髓样本中检测分子重排及突变;微小残留病(MRD)通过流式细胞术检测,作为疗效及预后评估的核心标志物,验证逻辑为比较MRD阴性与阳性患者的预后差异。研究过程详述:分子亚型的样本来源为患者诊断时的骨髓样本,检测方法包括靶向DNA二代测序、RNA测序及FISH;MRD的样本来源为CAR-T治疗后的骨髓样本,检测方法为流式细胞术,阈值设定为<0.01%。本研究未直接报告MRD作为预后Biomarker的ROC曲线数据,因此特异性与敏感性数据未明确提供。核心成果:首次证实Ph-like ALL患者接受CAR-T联合异基因造血干细胞移植后的预后与Ph+ ALL及其他高危B-ALL相当,打破了Ph-like ALL预后更差的传统认知;Ph-like ALL亚组中,不同分子亚型的预后无显著差异,提示CAR-T联合异基因造血干细胞移植可克服不同分子亚型Ph-like ALL的不良预后;微小残留病阴性完全缓解率与其他组无差异,推测微小残留病可作为该治疗策略下的预后预测指标,但本研究未报告具体的风险比(HR)数据。
