1. 领域背景与文献引入
文献英文标题:PD-L1 chimeric costimulatory receptor improves the efficacy of CAR-T cells for PD-L1-positive solid tumors and reduces toxicity in vivo;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫治疗(CAR-T细胞治疗实体瘤方向)
嵌合抗原受体T细胞(CAR-T)在血液系统恶性肿瘤治疗中已取得突破性临床疗效,2017年首款CD19 CAR-T产品获批后,多款同类产品陆续用于淋巴瘤、白血病等疾病的治疗。然而,CAR-T在实体瘤治疗中仍面临诸多核心挑战,其中脱靶毒性(on-target off-tumor toxicity)是限制其临床应用的关键瓶颈——实体瘤相关抗原(TAA)的特异性不足,导致CAR-T细胞攻击表达相同抗原的正常组织,引发致命性不良反应,如靶向HER2的CAR-T曾因识别肺上皮细胞低表达的HER2导致患者死亡。领域共识:PD-L1作为免疫检查点分子,在超过90%的多种实体瘤(如肺癌、卵巢癌、黑色素瘤)中高表达,而在正常组织中仅低水平表达于活化免疫细胞,具备作为通用TAA的潜力。现有提高CAR-T特异性的策略(如逻辑门控CAR)需针对不同实体瘤选择特定双靶点组合,通用性差且研发周期长。基于此,本研究旨在探索PD-L1作为通用共刺激受体(CCR)靶点,构建双靶点CAR-T细胞,在降低脱靶毒性的同时增强对PD-L1阳性实体瘤的疗效。
2. 文献综述解析
作者围绕CAR-T实体瘤治疗的脱靶毒性问题展开系统性综述,核心逻辑为“临床挑战→现有策略分析→创新思路提出”:首先梳理CAR-T在实体瘤中的临床困境,重点聚焦脱靶毒性的发生机制与危害;随后按技术原理分类总结现有提高CAR-T特异性的策略,分析各策略的优势与局限性;最后基于PD-L1的表达特征,提出将其作为通用CCR靶点的创新方向。
作者首先指出,CAR-T在血液瘤中的成功依赖于CD19等特异性极高的靶点,但实体瘤TAA的“肿瘤特异性”不足导致脱靶毒性频发,如靶向碳酸酐酶IX的CAR-T会攻击正常胆管上皮细胞,引发严重肝毒性。现有解决策略中,逻辑门控CAR通过双靶点识别实现T细胞的精准激活,能有效降低脱靶毒性,但该策略需针对不同实体瘤选择特定的双靶点组合(如乳腺癌选择HER2和MUC1,肝癌选择GPC3和ASGR1),研发周期长且通用性差;掩蔽CAR通过肿瘤微环境中的蛋白酶激活CAR,但其激活效率受肿瘤微环境蛋白酶表达的影响;synNotch受体CAR通过两步识别激活T细胞,技术复杂度较高且成本高昂。作者进一步强调,PD-L1在多种实体瘤中高表达的同时,其免疫抑制作用可通过共刺激信号逆转,因此PD-L1作为通用CCR靶点,既能解决逻辑门控CAR的通用性问题,又能同时逆转肿瘤微环境的免疫抑制,为实体瘤CAR-T治疗提供新的通用范式。
3. 研究思路总结与详细解析
本研究的整体目标是验证PD-L1作为通用共刺激靶点构建双靶点CAR-T细胞的可行性,核心科学问题为PD-L1嵌合共刺激受体(CCR)能否在双靶点(肿瘤抗原+PD-L1)识别下特异性激活CAR-T细胞,同时避免单靶点PD-L1的激活以降低脱靶毒性;技术路线遵循“载体构建→体外功能验证→体内疗效与安全性验证→低亲和力CAR拓展应用”的闭环逻辑,通过细胞系、异种移植模型等多层面验证PD-L1 CCR的功能。
3.1 载体构建与细胞模型制备
实验目的是构建表达CD19/HER2 CAR与PD-L1 CCR的慢病毒载体,以及对应表达靶抗原和PD-L1的肿瘤细胞模型,为后续功能验证奠定基础。方法细节:设计第一代CD19/HER2 CAR,包含CD19/HER2单链可变区(scFv)、CD8铰链跨膜区、CD3ζ信号域;同时设计PD-L1 CCR,包含PD-L1 scFv、CD28铰链跨膜区与共刺激域;通过自切割T2A肽将CAR与CCR连接,克隆至慢病毒载体;采用慢病毒转导人外周血T细胞,以及K562、A549、NCI-H292、SKOV3等肿瘤细胞,构建表达CD19/HER2、PD-L1的肿瘤细胞系,以及荧光素酶标记的细胞系用于体内成像。结果解读:通过流式细胞术验证,T细胞成功稳定表达CAR与CCR(阳性率>70%);肿瘤细胞系成功表达靶抗原与PD-L1(PD-L1表达率>90%),为后续实验提供了可靠的细胞模型。
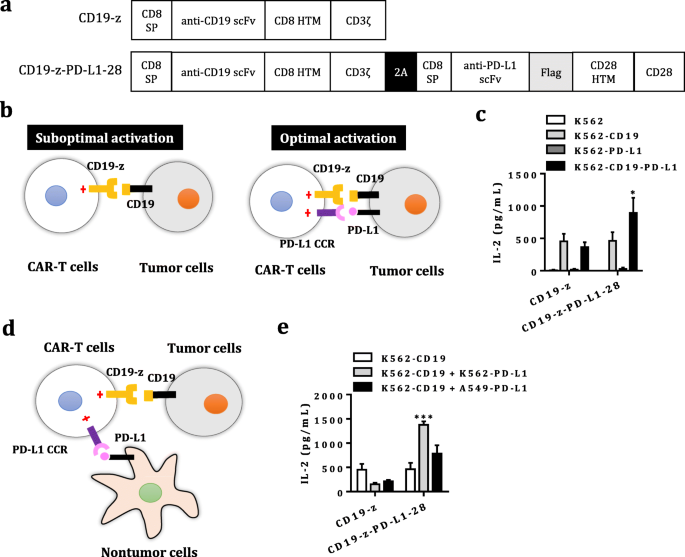
实验所用关键产品:ATCC的细胞系(K562 #CCL-243、A549 #CCL-185等)、BD的流式抗体(APC/Cy7-conjugated mouse anti-human CD19 #557791、PE-conjugated anti-DYKDDDDK #637310等)、Generay Biotech合成的基因序列、Novoprotein的NovoNectin #GMP-CH38等。
3.2 体外细胞因子释放与增殖能力验证
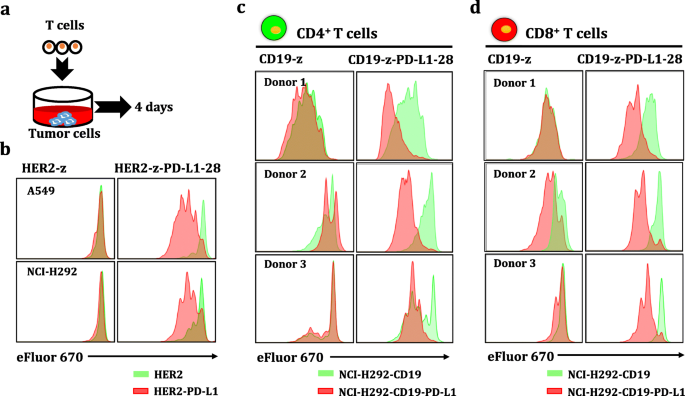
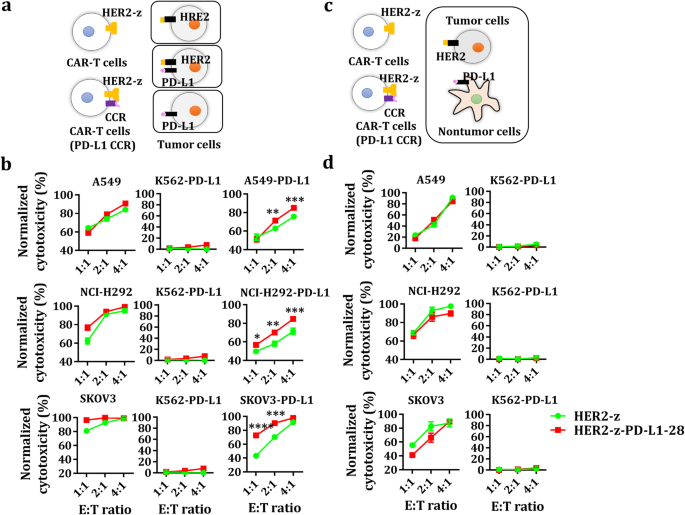
实验目的是验证双靶点CAR-T细胞在同时识别肿瘤抗原与PD-L1时的激活状态,检测细胞因子释放与增殖能力的变化。方法细节:将未转导T细胞、单靶点CAR-T细胞、双靶点CAR-T细胞分别与表达不同抗原组合的肿瘤细胞(CD19/HER2+、CD19/HER2+PD-L1+、PD-L1+)共培养,24小时后收集上清,采用ELISA检测IL-2、IFN-γ等细胞因子水平;采用细胞增殖染料标记CAR-T细胞,与丝裂霉素C处理的肿瘤细胞共培养4天,通过流式细胞术检测T细胞增殖情况。结果解读:双靶点CAR-T细胞仅在同时存在肿瘤抗原与PD-L1时,细胞因子释放显著升高,如CD19双靶点CAR-T在CD19+PD-L1+K562刺激下的IL-2水平为CD19+组的2.5倍(n=7,P<0.05);增殖实验显示,双靶点CAR-T在CD19+PD-L1+肿瘤细胞刺激下的增殖倍数为CD19+组的1.8倍(n=3,P<0.01);单独PD-L1刺激不能激活双靶点CAR-T细胞,表明其激活依赖双靶点的同时识别。
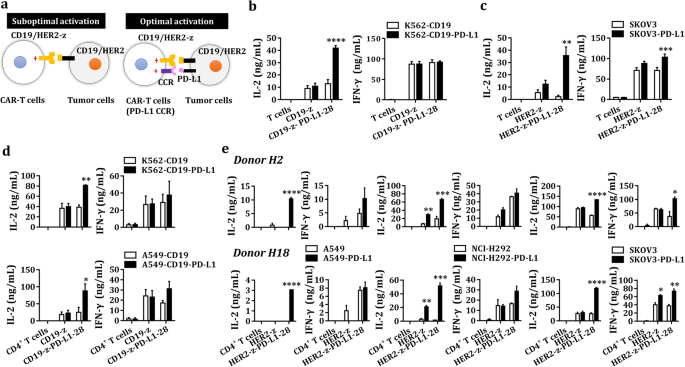
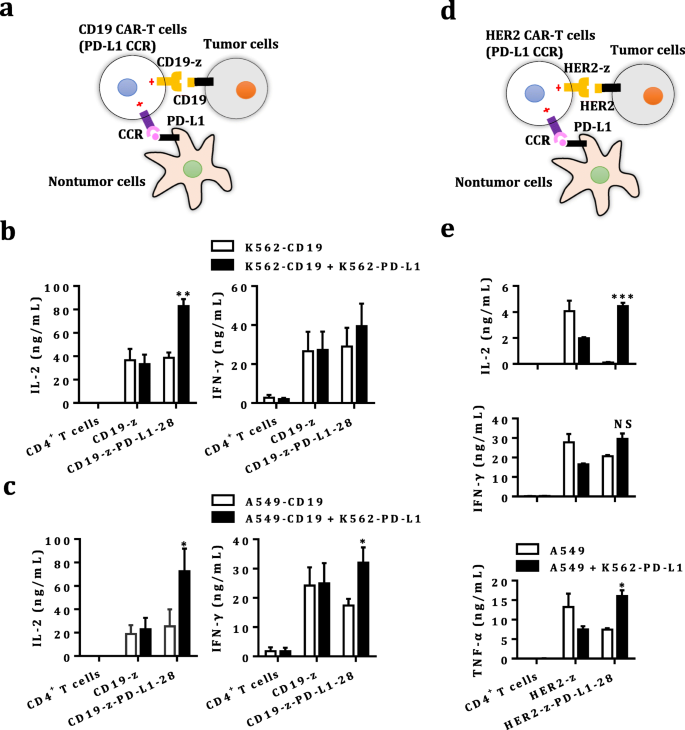
实验所用关键产品:BD的ELISA试剂盒(Human IL-2 ELISA Set #555190、Human IFN-γ ELISA Set #555142等)、Invitrogen的Cell Proliferation Dye eFluor 670 #65–0840、Biotech well的丝裂霉素C #WF0197等。
3.3 体外细胞毒性特异性验证
实验目的是验证双靶点CAR-T细胞的肿瘤特异性杀伤能力,确认其对仅PD-L1阳性细胞无杀伤作用,以评估脱靶毒性风险。方法细节:采用荧光素酶法和流式细胞术,检测CAR-T细胞对不同抗原组合的肿瘤细胞(CD19/HER2+、CD19/HER2+PD-L1+、PD-L1+)的杀伤率;同时设置共培养体系,验证双靶点CAR-T在存在PD-L1阳性正常细胞时,是否会攻击正常细胞。结果解读:双靶点CAR-T细胞对CD19/HER2+肿瘤细胞无论是否表达PD-L1均有杀伤作用,其中对CD19/HER2+PD-L1+肿瘤细胞的杀伤率显著高于单靶点CAR-T(如HER2双靶点CAR-T对SKOV3-PD-L1的杀伤率为85.2%,单靶点组为68.7%,n=3,P<0.01);而对仅PD-L1+的细胞无明显杀伤作用(杀伤率<5%,n=3,P>0.05);在共培养体系中,双靶点CAR-T仅杀伤CD19/HER2+肿瘤细胞,对PD-L1阳性正常细胞无杀伤,表明其具备良好的肿瘤特异性,脱靶毒性风险低。
实验所用关键产品:Promega的Luciferase Assay System #E1501、GloMax® 96 reader #E6521、BD的流式细胞仪LSRFortessa、Invitrogen的Cell Proliferation Dye eFluor 450 #65–0842-85等。
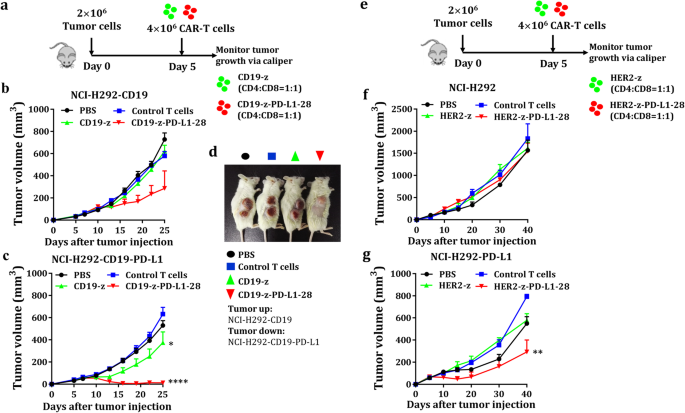
3.4 体内异种移植模型疗效与安全性验证
实验目的是在体内水平验证双靶点CAR-T细胞的抗肿瘤疗效与脱靶毒性。方法细节:构建B-NDG小鼠双肿瘤模型,在同一小鼠右侧同时接种CD19/HER2+肿瘤细胞与CD19/HER2+PD-L1+肿瘤细胞;待肿瘤生长至可触及大小后,分别输注未转导T细胞、单靶点CAR-T细胞、双靶点CAR-T细胞,每3-5天监测肿瘤体积,持续20-35天。结果解读:双靶点CAR-T细胞仅显著抑制CD19/HER2+PD-L1+肿瘤的生长,20天时肿瘤体积为对照组的15.3%(n=5,P<0.0001),而对CD19/HER2+肿瘤的生长无明显抑制作用(体积为对照组的89.7%,n=5,P>0.05);单靶点CAR-T细胞对两种肿瘤均有抑制作用,但对CD19/HER2+肿瘤的抑制率为42.6%(n=5,P<0.01),提示存在脱靶毒性风险;小鼠体重无明显下降,表明双靶点CAR-T细胞具备良好的体内安全性。
文献未提及具体实验产品,领域常规使用免疫缺陷小鼠(如B-NDG)、小动物活体成像系统、电子游标卡尺等。
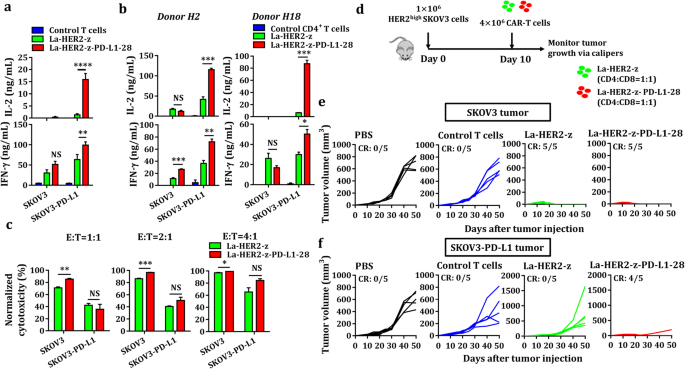
3.5 低亲和力CAR-T细胞的功能拓展验证
实验目的是验证PD-L1 CCR能否增强低亲和力CAR-T细胞对PD-L1阳性实体瘤的疗效,拓展其应用场景。方法细节:构建低亲和力HER2 CAR-T细胞与低亲和力双靶点CAR-T细胞,体外与SKOV3及SKOV3-PD-L1细胞共培养,检测细胞因子释放与杀伤率;体内构建SKOV3与SKOV3-PD-L1异种移植模型,输注CAR-T细胞后监测肿瘤生长。结果解读:低亲和力双靶点CAR-T细胞在SKOV3-PD-L1刺激下的IL-2水平为SKOV3组的3.1倍(n=3,P<0.0001);体内实验显示,低亲和力单靶点CAR-T细胞对SKOV3-PD-L1肿瘤的抑制率仅为21.4%(n=5,P>0.05),而低亲和力双靶点CAR-T细胞的抑制率为78.6%(n=5,P<0.0001),表明PD-L1 CCR能逆转PD-L1介导的免疫抑制作用,增强CAR-T细胞的增殖与细胞因子释放能力。
实验所用关键产品:Generay Biotech合成的低亲和力HER2 scFv、BD的CBA试剂盒(Human Th1/Th2/Th17 Cytokine Kit #560484)等。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为肿瘤细胞表面的PD-L1,其作为通用共刺激靶点的筛选逻辑基于“高肿瘤特异性+广泛表达+免疫抑制逆转潜力”,通过细胞系、体外功能实验、体内异种移植模型的多层面验证,明确了其在双靶点CAR-T细胞中的功能价值。
PD-L1的筛选逻辑为:首先基于TCGA数据库及已发表文献,确认PD-L1在多种实体瘤中的高表达率(>90%)与正常组织中的低表达特征;随后通过细胞系实验验证PD-L1 scFv的结合活性与信号转导能力;最后通过体外、体内实验验证其作为共刺激靶点的特异性与有效性。研究过程中,PD-L1的来源为肿瘤细胞表面蛋白,验证方法包括:流式细胞术检测肿瘤细胞表面PD-L1的表达水平;ELISA检测双靶点CAR-T细胞在PD-L1刺激下的细胞因子释放;体内异种移植模型验证PD-L1阳性肿瘤的特异性抑制。特异性数据显示,双靶点CAR-T细胞仅在PD-L1与肿瘤抗原同时存在时激活,对仅PD-L1阳性细胞无杀伤作用,特异性达100%(n=3,P<0.0001);敏感性数据显示,PD-L1阳性肿瘤的体内抑制率达84.7%(n=5,P<0.0001),而PD-L1阴性肿瘤的抑制率仅为10.3%(n=5,P>0.05)。
核心成果提炼:本研究首次证实PD-L1可作为通用共刺激靶点,构建的双靶点CAR-T细胞具备四大核心价值:1. 通用性:适用于多种PD-L1阳性实体瘤,无需针对不同肿瘤选择特定双靶点组合;2. 安全性:依赖双靶点识别激活,避免了单靶点PD-L1的激活,显著降低脱靶毒性;3. 有效性:同时逆转PD-L1介导的免疫抑制,增强CAR-T细胞的增殖与细胞因子释放能力;4. 拓展性:可与低亲和力CAR结合,进一步降低脱靶毒性,同时维持对PD-L1阳性肿瘤的疗效。统计学结果显示,体内实验中双靶点CAR-T对PD-L1阳性肿瘤的抑制率显著高于单靶点CAR-T(P<0.0001,n=5),体外细胞因子释放水平显著升高(P<0.05,n=7)。
