1. 领域背景与文献引入
文献英文标题:The impact of integrated hepatitis B virus DNA on oncogenesis and antiviral therapy;发表期刊:Biomarker Research;影响因子:未公开;研究领域:慢性乙型肝炎(CHB)与肝细胞癌(HCC)的病毒整合机制、致癌作用及抗病毒治疗策略。
全球慢性乙型肝炎(CHB)感染负担沉重,每年约82万例CHB患者出现肝衰竭、肝硬化、HBV相关肝细胞癌(HCC)等不良结局,CHB患者的HCC发生风险为未感染者的10-100倍。领域共识:HBV DNA整合到宿主基因组是HBV相关HCC发生的关键驱动因素之一,约85-90%的HBV相关HCC组织中可检测到整合的HBV DNA,且该整合事件可在HBsAg血清转换后持续存在,导致HBsAg复阳并升高HCC发生风险。当前CHB治疗的目标分为功能性治愈(持续HBsAg清除、HBV DNA低于检测下限)与彻底治愈(清除肝内共价闭合环状DNA(cccDNA)及整合HBV DNA),但彻底治愈仍面临病毒库持续存在、宿主免疫应答薄弱、治疗周期长等核心挑战。现有研究虽已揭示HBV整合的部分机制,但缺乏对整合事件从发生、致癌到干预的全链条系统性总结,也未明确整合DNA作为Biomarker的临床应用价值,因此本综述旨在全面梳理HBV整合的分子机制、致癌作用、检测方法及清除策略,为CHB的彻底治愈及HBV相关HCC的防治提供学术参考与方向指引。
2. 文献综述解析
作者以HBV整合事件的“发生机制-检测方法-致癌作用-干预策略”为核心分类维度,系统梳理了领域内近40年的研究成果,从基础机制到临床应用形成完整逻辑链条。
在HBV整合的发生机制方面,早期研究通过细胞与动物模型证实整合发生在病毒复制阶段,由逆转录过程中产生的双链线性DNA(dslDNA)通过非同源末端连接(NHEJ)或微同源介导的末端连接(MMEJ)整合到宿主基因组,且整合事件在感染早期即可发生;同时,研究发现肝脏炎症与HBV整合相互促进,炎症导致的氧化损伤为整合提供基因组断点,而整合产生的HBsAg又会加重T细胞耗竭,进一步加剧炎症反应。在检测方法方面,从1980年首次使用Southern Blot杂交检测整合,到后续的荧光原位杂交(FISH)、PCR衍生技术(Alu-PCR、反向嵌套PCR),再到高通量测序(全基因组测序WGS、全外显子测序WES、三代测序),检测技术的灵敏度与分辨率不断提升,其中三代测序可实现复杂整合重排的完整解析,但成本较高限制了其临床应用。在致癌机制方面,现有研究证实HBV整合通过三种核心途径促进HCC发生:调控癌基因与抑癌基因的表达、诱导染色体不稳定、表达截短突变的HBV蛋白;其中,整合到hTERT、CCNE1等癌基因启动子区域可显著上调其表达,而截短的HBx蛋白(ct-HBx)可通过诱导干细胞特性、抑制凋亡等促进肿瘤进展。在干预策略方面,核苷(酸)类似物(NAs)可通过抑制病毒复制减少新的整合事件发生,长期治疗可降低肝脏组织中的整合频率,但无法清除已有的整合;干扰素-α(IFN-α)可间接减少前基因组RNA(pgRNA)合成,可能降低整合发生率,但对已存在的整合效果尚不明确;基因编辑技术(CRISPR/Cas9、锌指核酸酶ZFNs、转录激活因子样效应物核酸酶TALENs)与RNA干扰具有清除整合DNA的潜力,但仍面临脱靶效应、递送效率等临床转化挑战。
与现有综述多聚焦于HBV整合的单一环节不同,本综述系统整合了从整合发生机制到临床干预的全链条研究,首次明确了HBV整合DNA作为CHB患者HCC风险预测Biomarker及功能性治愈评估指标的潜在价值,同时强调了早期干预对减少整合事件、降低HCC风险的重要性,弥补了领域内对整合事件临床意义总结不足的研究空白。
3. 研究思路总结与详细解析
本研究为系统性综述,核心目标是全面总结HBV DNA整合的分子机制、致癌作用、检测方法及清除策略,核心科学问题是明确HBV整合促进HCC发生的关键机制及可干预靶点,技术路线遵循“基础机制-检测技术-临床意义-干预策略”的逻辑闭环,通过梳理领域内经典与前沿研究,为CHB的彻底治愈及HBV相关HCC的防治提供学术参考。
3.1 HBV整合的发生机制解析
实验目的:明确HBV整合的发生时间、分子过程及与肝脏炎症的相互作用关系。
方法细节:作者梳理了细胞感染模型(原代人肝细胞PHH、HepaRG-NTCP、HepG2-NTCP等)、动物模型(鸭乙型肝炎病毒DHBV感染鸭模型、土拨鼠肝炎病毒WHV感染土拨鼠模型、人源化肝脏小鼠模型)及临床样本的研究数据,结合分子生物学技术(如PCR、测序、基因编辑)对整合过程的解析结果。
结果解读:HBV整合发生在病毒复制阶段,逆转录过程中约5-10%的病毒DNA会形成dslDNA,该DNA可通过NHEJ或MMEJ整合到宿主基因组;动物模型证实整合在感染早期即可发生,如DHBV感染鸭后6天即可检测到整合,WHV感染土拨鼠后1-3小时即可发生整合;肝脏炎症与HBV整合相互促进,炎症导致的氧化损伤可诱导宿主基因组双链断裂,为整合提供断点,而整合产生的HBsAg可通过诱导T细胞耗竭、激活库普弗细胞等加重肝脏炎症,形成恶性循环。
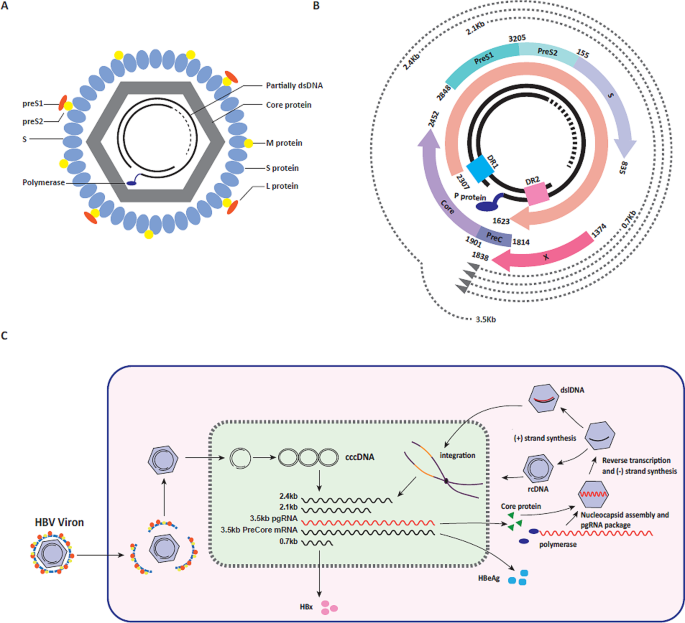
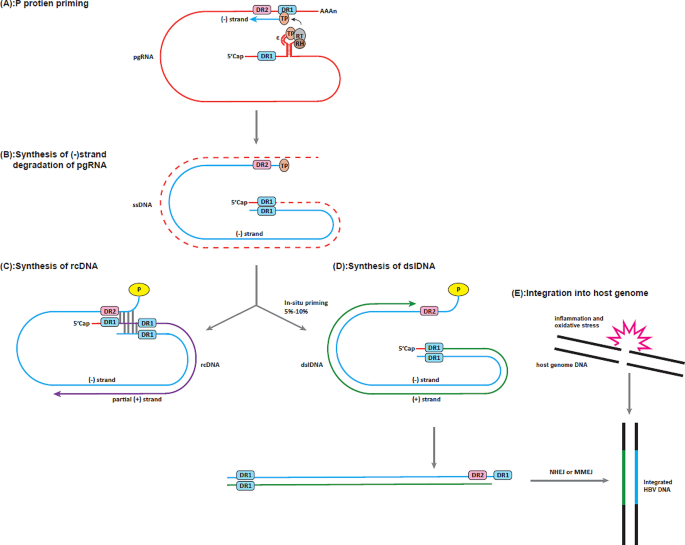
产品关联:文献未提及具体实验产品,领域常规使用细胞系培养试剂、病毒感染试剂盒、分子克隆试剂、高通量测序平台等。
3.2 HBV整合的检测方法与研究模型解析
实验目的:总结HBV整合的检测技术特点及研究模型的应用价值。
方法细节:作者梳理了从经典的Southern Blot杂交、FISH到PCR衍生技术(Alu-PCR、反向嵌套PCR),再到高通量测序(WGS、WES、三代测序)的检测方法,同时总结了细胞模型、动物模型及临床样本在整合研究中的应用。
结果解读:Southern Blot是检测整合的经典方法,可定性分析整合事件,但灵敏度较低且无法精确定位整合位点;FISH可实现整合位点的染色体定位,但分辨率有限;PCR衍生技术可实现整合位点的扩增与测序,但存在检测偏倚;高通量测序可实现全基因组范围内的整合位点分析,其中三代测序可检测复杂的基因组重排,但成本较高。细胞模型中,PHH、HepaRG-NTCP等可模拟HBV的自然感染与整合过程,而HCC细胞系可用于整合致癌机制的研究;动物模型中,DHBV鸭模型、WHV土拨鼠模型可用于整合的动态监测,人源化肝脏小鼠模型可模拟人类HBV感染的整合过程,为临床转化研究提供支撑。
产品关联:文献未提及具体实验产品,领域常规使用核酸杂交试剂盒、PCR试剂盒、荧光原位杂交试剂盒、高通量测序平台等。
3.3 HBV整合的致癌机制解析
实验目的:明确HBV整合促进HCC发生的核心分子途径。
方法细节:作者梳理了基因组测序、基因表达谱分析、功能实验(如基因敲除/过表达、细胞增殖与凋亡检测)等研究结果,总结了整合事件对宿主基因组及细胞功能的影响。
结果解读:HBV整合通过三种核心途径促进HCC发生:一是调控癌基因与抑癌基因的表达,整合事件偏好发生在癌基因(如hTERT、CCND1、FGF19)或抑癌基因的附近区域,可通过启动子插入、基因融合等方式上调癌基因表达或下调抑癌基因表达,其中hTERT启动子区域的整合可显著上调端粒酶活性,维持肿瘤细胞的无限增殖能力;二是诱导染色体不稳定,整合断点与基因组拷贝数变异显著相关,且整合偏好发生在基因组脆弱位点与CpG岛区域,可导致染色体易位、缺失等重排,破坏基因组稳定性;三是表达截短突变的HBV蛋白,整合产生的截短HBs蛋白可诱导内质网应激与氧化损伤,激活致癌信号通路,而截短的HBx蛋白(ct-HBx)可通过调控细胞周期、抑制凋亡、促进侵袭转移等方式促进肿瘤进展。
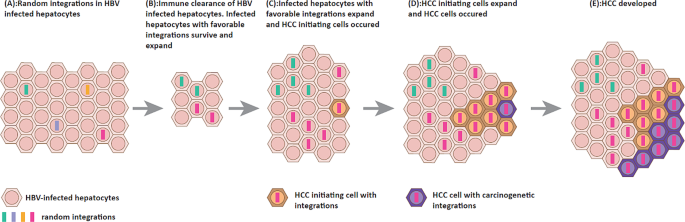
产品关联:文献未提及具体实验产品,领域常规使用免疫印迹(WB)试剂、免疫组化(IHC)试剂盒、基因编辑工具、细胞功能检测试剂盒等。
3.4 HBV整合的干预策略解析
实验目的:总结现有清除或抑制HBV整合的治疗策略及临床应用潜力。
方法细节:作者梳理了临床抗病毒治疗(NAs、IFN-α)、基因编辑技术(CRISPR/Cas9、ZFNs、TALENs)、RNA干扰等领域内的研究结果,分析了不同策略的作用机制与效果。
结果解读:NAs可通过抑制病毒聚合酶活性,减少病毒复制及dslDNA的产生,从而降低新的整合事件发生频率;一项纵向研究显示,CHB患者接受NAs治疗5年与10年后,肝脏组织中的整合频率逐渐降低,但NAs无法清除已有的整合DNA。IFN-α可通过激活宿主免疫应答,间接减少pgRNA的合成,从而降低整合发生率,但对已存在的整合DNA效果尚不明确;部分研究显示,HBsAg血清转换患者中仍存在整合DNA,且这类患者的HCC发生风险更高。基因编辑技术可通过靶向切割HBV DNA序列,清除cccDNA与整合DNA,其中CRISPR/Cas9技术在细胞与动物模型中已显示出较好的效果,但仍面临脱靶效应、递送效率等临床转化挑战。RNA干扰可通过靶向HBV转录本,降低整合DNA来源的HBsAg表达,如ARC-520在临床试验中可显著降低HBsAg水平,但无法直接清除整合DNA。
产品关联:文献未提及具体实验产品,领域常规使用抗病毒药物(恩替卡韦、替诺福韦等)、基因编辑试剂、RNA干扰试剂等。
4. Biomarker研究及发现成果解析
本综述明确了HBV整合DNA作为CHB患者HCC风险预测、功能性治愈评估的潜在Biomarker,其筛选与验证逻辑遵循“组织样本检测-循环cfDNA验证-临床预后关联”的完整链条。
Biomarker定位:文献中涉及的Biomarker类型为整合HBV DNA(包括组织中的整合位点及循环中的病毒-宿主嵌合DNA(vh-DNA)),筛选与验证逻辑为:首先基于临床组织样本筛选HBV整合的高频位点,然后通过细胞与动物模型验证整合位点的致癌作用,最后通过临床样本验证循环vh-DNA的非侵入性检测价值。
研究过程详述:Biomarker的来源包括CHB患者与HBV相关HCC患者的肝脏组织样本、外周血循环游离DNA(cfDNA);验证方法包括组织样本中的Southern Blot、PCR、高通量测序,以及循环cfDNA中的高通量测序与特异性PCR检测;特异性与敏感性方面,肝脏组织样本中85-90%的HBV相关HCC存在整合HBV DNA,循环cfDNA中的vh-DNA可在HCC患者中检测到,且能有效检测术后残留的肿瘤细胞,预测HCC复发(文献未明确提供AUC、敏感性与特异性数据,基于综述内容推测)。
核心成果提炼:HBV整合DNA可作为CHB患者HCC发生风险的预测Biomarker,整合频率高或整合到癌基因区域的患者HCC发生风险显著升高;循环vh-DNA可作为非侵入性Biomarker,用于HCC的早期诊断与术后复发监测;首次明确了整合DNA在功能性治愈评估中的价值,即HBsAg血清转换后仍存在整合DNA的患者HCC发生风险更高,需长期监测。统计学结果:肝脏组织样本中HBV整合阳性率为85-90%(文献未明确样本量,基于综述数据),循环vh-DNA的临床研究样本量未明确,但结果显示其可有效预测HCC术后复发。
