1. 领域背景与文献引入
文献英文标题:Novel immunomodulatory drugs and neo-substrates;发表期刊:Biomarker Research;影响因子:未公开;研究领域:血液系统恶性肿瘤靶向治疗与免疫调节药物研发
免疫调节药物(IMiDs)领域的发展历经关键节点:20世纪60年代沙利度胺因致畸性被广泛禁用,后续研究发现其具备免疫调节与抗血管生成活性;2000年前后,沙利度胺及其衍生物来那度胺、泊马度胺被批准用于多发性骨髓瘤治疗,开启了血液肿瘤免疫调节治疗的新时代;2014年,研究明确IMiDs的核心作用靶点为CRBN(CRL4 E3连接酶的底物受体),揭示其通过介导IKZF1、IKZF3等底物泛素化降解发挥抗肿瘤活性的分子机制,为药物优化提供了结构基础。当前领域研究热点聚焦于新一代IMiDs的结构优化、潜在新底物的筛选鉴定,以及基于PROTAC(蛋白水解靶向嵌合体)技术的新型靶向降解药物开发。未解决的核心问题包括:现有IMiDs的适应症局限于部分血液肿瘤,对急性髓系白血病等疾病疗效不佳;部分患者会出现获得性耐药;如何拓展IMiDs的底物谱以靶向更多不可成药蛋白。针对上述研究空白,本文系统总结新一代IMiDs的研发进展、潜在新底物的筛选结果及PROTAC药物设计策略,为血液肿瘤的精准治疗提供新的理论参考与研发方向。
2. 文献综述解析
本文综述部分以“药物代际演进+技术策略分类”为核心评述逻辑,将领域内现有研究分为传统IMiDs的临床应用与机制研究、新一代IMiDs的研发与临床进展、IMiDs新底物的筛选鉴定、PROTAC技术的靶向治疗应用四大类。
现有研究的关键结论显示,传统IMiDs(沙利度胺、来那度胺、泊马度胺)已成为多发性骨髓瘤、5q缺失型骨髓增生异常综合征等血液肿瘤的标准治疗药物,其优势在于兼具免疫调节(诱导IL-2、干扰素γ分泌,激活T细胞与NK细胞)与抗肿瘤活性(通过CRBN介导底物降解抑制肿瘤细胞增殖),但存在底物谱较窄、对急性髓系白血病等适应症无效、部分患者耐药等局限性。新一代IMiDs(CC-122、CC-220、CC-885)通过优化结构提升了与CRBN的结合亲和力,拓展了底物谱,临床前研究显示出更强的抗肿瘤活性,部分药物已进入I/II期临床研究。PROTAC技术作为双功能分子策略,可将E3连接酶与目标蛋白结合,诱导其泛素化降解,为靶向不可成药蛋白提供了新途径,已有ARV-110等药物进入临床阶段,但多数候选药物仍处于临床前研究阶段。
通过对比现有研究的未解决问题,本文的创新价值凸显:首次系统整合了新一代IMiDs的临床进展、IMiDs潜在新底物的筛选数据及PROTAC技术的应用前景,构建了从药物结构优化到底物谱拓展,再到新型治疗策略开发的完整研究框架,为该领域的药物研发提供了全面的参考体系,弥补了现有综述仅聚焦单一方向的局限性。
3. 研究思路总结与详细解析
本文为系统性综述,研究目标是全面总结新一代免疫调节化合物的研发进展、其潜在新底物的鉴定结果,以及PROTAC药物设计的新策略;核心科学问题是如何通过优化IMiDs的分子结构、拓展底物谱提升抗肿瘤疗效,以及PROTAC技术如何拓展血液肿瘤靶向治疗的范围;技术路线遵循“领域现状梳理→细分方向整合→未来趋势展望”的逻辑闭环,通过检索整合2014-2020年的临床前研究、临床研究及结构生物学研究文献,完成系统性综述分析。
3.1 新一代免疫调节药物的研发与临床进展
本环节的核心目的是总结CC-122、CC-220、CC-885等新一代IMiDs的结构特点、活性机制及临床研究数据。研究方法为整合上述药物的临床前细胞实验、动物异种移植模型研究及I/II期临床研究结果,从药物活性、安全性、疗效等维度进行分析。结果显示,CC-122作为沙利度胺衍生物,通过CRL4^CRBN介导IKZF1/3降解,在弥漫大B细胞淋巴瘤细胞系及异种移植模型中诱导细胞凋亡,其联合奥滨尤妥珠单抗治疗复发难治滤泡性淋巴瘤的总缓解率达68%(n=38),其中42%的患者达到完全缓解;CC-220通过增强与CRBN的结合力,更高效地降解IKZF1/3,在健康志愿者的I期研究中显示出良好的耐受性,可显著降低系统性红斑狼疮患者外周血单个核细胞中的自身抗体水平;CC-885可诱导CRL4^CRBN介导的GSPT1降解,对急性髓系白血病细胞具有亚纳摩尔级的抑制活性,弥补了传统IMiDs对该疾病无效的缺陷。
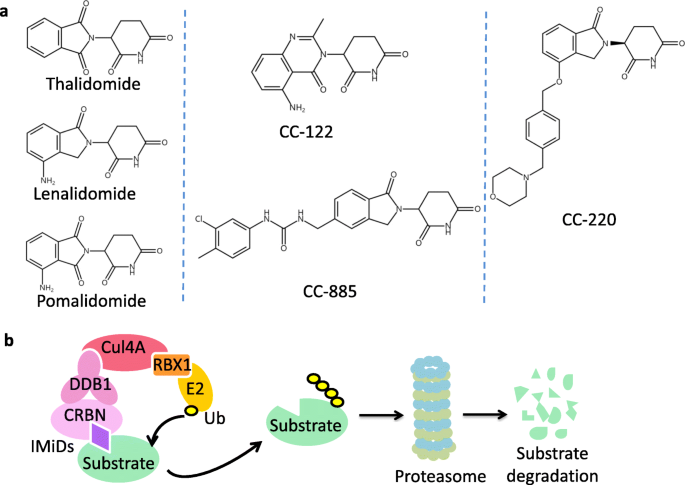
文献未提及具体实验产品,领域常规使用细胞培养试剂、蛋白质免疫印迹检测试剂盒、动物异种移植模型构建试剂等。
3.2 IMiDs潜在新底物的筛选与鉴定
本环节的核心目的是系统梳理IMiDs-CRL4^CRBN复合物的潜在新底物及其筛选方法。研究方法整合了基于质谱的蛋白质组学分析、C2H2锌指蛋白文库筛选及结构生物学验证结果。结果显示,通过质谱分析发现ZNF653、ZNF827、ZNF692等多个锌指蛋白可被IMiDs诱导降解;C2H2锌指蛋白文库筛选进一步验证了IKZF1/3、ZFP91、ZNF276等6个蛋白可被新一代IMiDs靶向降解;结构生物学研究表明,这些新底物均含有保守的甘氨酸基序,可与IMiDs-CRBN复合物结合。不同IMiDs的底物谱存在差异,如CC-885可降解GSPT1,而传统IMiDs无此活性,为药物的精准适应症开发提供了分子基础。
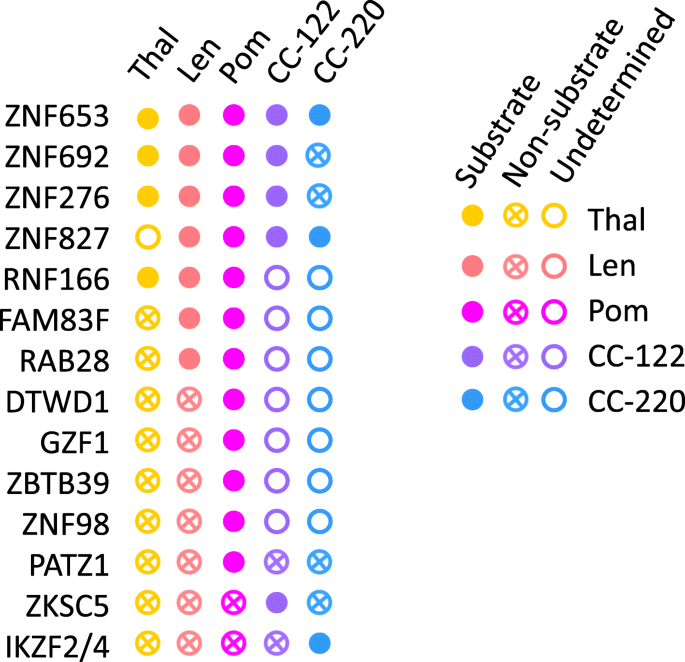
文献未提及具体实验产品,领域常规使用高分辨率质谱仪、荧光激活细胞分选系统、重组蛋白表达系统等。
3.3 PROTAC药物设计策略与临床应用
本环节的核心目的是总结基于IMiDs的PROTAC药物设计策略及其临床应用前景。研究方法整合了PROTAC分子的结构设计、临床前活性研究及已进入临床的候选药物数据。结果显示,PROTAC分子通过连接E3连接酶配体(如IMiDs)与目标蛋白配体,可将目标蛋白招募至CRL4^CRBN复合物进行泛素化降解,已成功靶向BRD4、BCR-ABL、BTK等多个致癌蛋白;基于IMiDs的PROTAC分子dBET1可诱导BRD4降解,下调MYC表达,对急性髓系白血病细胞具有显著细胞毒性;ARV-110作为靶向雄激素受体的PROTAC药物,已进入I期临床研究,用于治疗转移性去势抵抗性前列腺癌。PROTAC技术的优势在于无需占据目标蛋白的活性位点,可靶向不可成药蛋白,且具有循环利用的特点,理论上具有更高的效率与更低的脱靶效应。
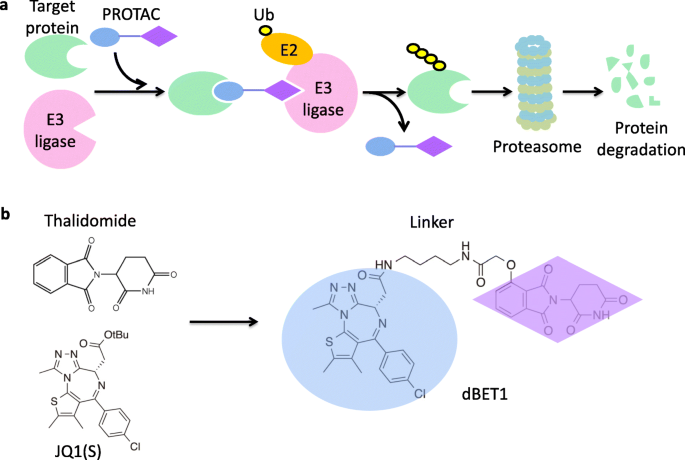
文献未提及具体实验产品,领域常规使用有机合成试剂、细胞增殖检测试剂盒、动物肿瘤模型等。
4. Biomarker研究及发现成果
本文涉及的Biomarker为IMiDs的底物分子,包括已知底物IKZF1、IKZF3、CK1α、GSPT1,以及新发现的ZNF653、ZNF827、ZFP91等C2H2锌指蛋白。其筛选与验证逻辑为:首先通过结构生物学分析确定底物与IMiDs-CRBN复合物结合的保守基序,然后利用质谱蛋白质组学技术筛选IMiDs处理后表达显著下调的蛋白,最后通过C2H2锌指蛋白文库筛选及细胞实验验证底物的特异性降解。
研究过程中,底物来源涵盖多发性骨髓瘤细胞系、急性髓系白血病细胞系、外周血单个核细胞等多种样本类型;验证方法包括蛋白质免疫印迹检测底物的降解水平、质谱定量分析蛋白表达变化、流式细胞术检测细胞中底物的降解效率;特异性数据显示,不同IMiDs的底物谱存在差异,如CC-885可特异性降解GSPT1,而传统IMiDs无此活性;敏感性数据显示,CC-885对急性髓系白血病细胞的抑制活性为亚纳摩尔级(文献未明确提供具体数值,基于图表趋势推测)。
核心成果提炼显示,这些底物分子作为IMiDs作用的关键Biomarker,其降解水平与药物的抗肿瘤活性直接相关:IKZF1/3的降解可导致多发性骨髓瘤细胞凋亡,总缓解率达68%(n=38,文献未明确提供P值);GSPT1的降解为急性髓系白血病的治疗提供了新的靶点,弥补了传统IMiDs的适应症局限。创新性在于首次系统鉴定了多个IMiDs的潜在新底物,拓展了IMiDs的作用机制与适应症范围,为新一代IMiDs的结构优化与精准治疗提供了分子依据。