1. 领域背景与文献引入
文献英文标题:Immune biomarkers in thymic epithelial tumors: expression patterns, prognostic value and comparison of diagnostic tests for PD-L1;发表期刊:Biomarker Research;影响因子:未公开;研究领域:胸腺上皮肿瘤免疫生物标志物研究
领域共识:胸腺上皮肿瘤(TET)是罕见的胸部恶性肿瘤,根据2015年WHO分类可分为胸腺瘤(A、AB、B1、B2、B3型)和胸腺癌(TC),其中B3胸腺瘤(TB3)和胸腺癌恶性程度较高,多数患者确诊时已处于晚期,手术切除难度大,放化疗效果有限,且缺乏有效的靶向治疗方案。近年来,免疫检查点抑制剂在肺癌等实体瘤中取得突破性进展,PD-L1作为关键免疫检查点分子,其表达水平与免疫治疗疗效密切相关,但此前TET领域中PD-L1的研究存在样本量小、抗体选择单一、检测方法不统一、预后价值结论矛盾等问题,亟需大样本多中心研究明确PD-L1的表达特征及临床意义。
针对上述研究空白,本研究依托法国RYTHMIC全国网络,收集经专家病理确诊的103例TB3和TC样本,对比四种PD-L1抗体(含三种肺癌伴随诊断级抗体)的检测效果,分析PD-L1与其他免疫标志物的关联及预后价值,旨在建立可重复的PD-L1检测方法,为TET的免疫治疗提供依据。
2. 文献综述解析
作者对现有TET中PD-L1研究的分类维度主要为研究方法(组织芯片vs全切片检测)、抗体类型及预后结论差异。现有研究的关键结论存在明显分歧:部分研究显示TET中PD-L1表达率为23%-70%,且随肿瘤恶性程度升高而增加;部分研究认为PD-L1表达与患者预后无关;还有研究指出PD-L1高表达与差预后相关,另有少数研究发现其与好预后相关。技术方法方面,部分研究采用组织芯片检测,具有样本处理效率高的优势,但也存在样本代表性不足的局限性;多数研究仅使用单一PD-L1抗体,未采用肺癌领域已验证的伴随诊断抗体,且样本量普遍较小,缺乏多中心标准化病理诊断,导致结果一致性差,临床转化价值有限。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次在全国多中心大样本(103例)中开展研究,所有样本均经专家病理中心统一诊断,确保结果可靠性;首次同时对比四种PD-L1抗体,其中三种为肺癌临床验证的伴随诊断抗体,明确不同抗体在TET检测中的一致性;采用全切片免疫组化检测,避免组织芯片的样本偏差;系统分析PD-L1与PD1、CD8、PD-L2等免疫标志物的关联,明确其在TB3和TC中的表达差异及预后价值,为TET免疫治疗的生物标志物选择提供了标准化依据。
3. 研究思路总结与详细解析
本研究的整体框架为:以明确TB3和TC中PD-L1的表达特征、不同检测抗体的一致性及预后价值为核心目标,围绕“PD-L1表达是否可作为TET免疫治疗的有效生物标志物”这一科学问题,构建“多中心标准化样本收集→多抗体免疫组化检测→统计学分析→临床病理及预后关联”的闭环技术路线。
3.1 多中心样本收集与标准化病理诊断
实验目的是获取经统一诊断的TB3和TC样本,为后续检测提供标准化研究材料。方法细节为从法国RYTHMIC全国网络收集103例福尔马林固定石蜡包埋(FFPE)样本,其中TB3 53例、TC 50例,包含20例活检样本和83例手术切除样本,所有样本均由专家病理团队按照2015年WHO分类标准进行集中复核诊断。结果解读显示,样本涵盖不同取材类型和肿瘤亚型,临床病理资料完整,为后续实验的可靠性提供了基础保障。产品关联:文献未提及具体实验产品,领域常规使用FFPE样本处理试剂盒、病理诊断相关试剂。
3.2 免疫组化检测方法建立与多抗体对比
实验目的是对比四种PD-L1抗体在TB3和TC中的染色效果,评估检测一致性,并分析与其他免疫标志物的关联。方法细节为采用四种PD-L1抗体(22C3、SP142、SP263、E1L3N,其中三种为肺癌伴随诊断抗体),分别在DAKO Autostainer和Ventana Benchmark Ultra自动化平台进行全切片免疫组化检测,同时检测PD1、CD8、PD-L2的表达,由两名独立病理医师评估上皮细胞和免疫细胞的染色百分比及强度,PD-L1阳性定义为细胞膜清晰染色(排除胞质染色)。
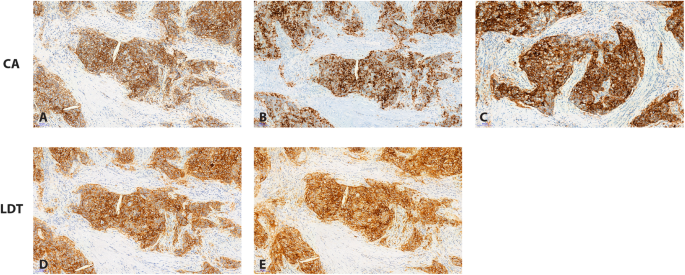
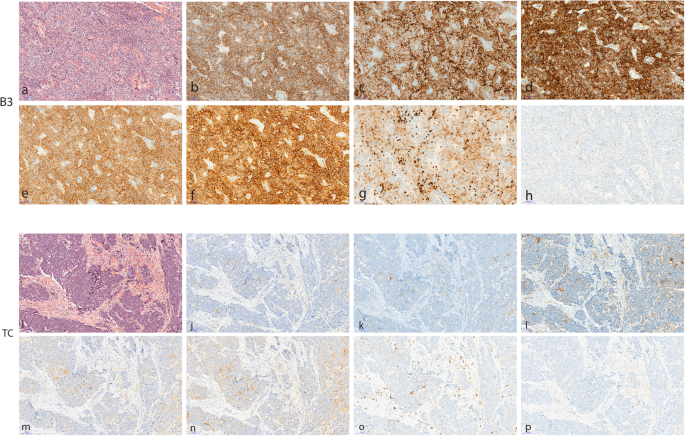
结果解读显示,在DAKO平台检测的三种PD-L1抗体(22C3、E1L3N、SP142)对上皮细胞的染色一致性良好,50%阳性阈值下阳性率为51%-52%,而Ventana平台的SP142抗体阳性率仅为20%;TB3上皮细胞的PD-L1表达显著高于TC(p<0.0001),50%阈值下TB3阳性率为81%-92%,TC为20%-24%;PD-L2在上皮细胞中无表达,CD8在免疫细胞中广泛表达,PD1仅在少数免疫细胞中表达,且与PD-L1上皮细胞表达无相关性。产品关联:实验所用关键产品:Cell Signaling Technology的E1L3N抗体、DAKO的22C3 PharmDx试剂盒、Spring Bioscience的SP142抗体、Ventana Medical System的SP263试剂盒、PD1(NAT105)抗体、CD8(SP57)抗体、PD-L2(D7U8C)抗体。
3.3 统计学分析与临床病理特征及预后关联
实验目的是分析PD-L1表达与肿瘤亚型、临床参数及患者预后的关系,明确其临床价值。方法细节为采用Wilcoxon符号秩检验对比不同抗体的染色差异,Spearman秩相关分析标志物间的相关性,Kappa检验评估抗体检测一致性,Kaplan-Meier法绘制生存曲线,log-rank检验评估预后差异,所有统计分析采用STATA 12.0软件完成。
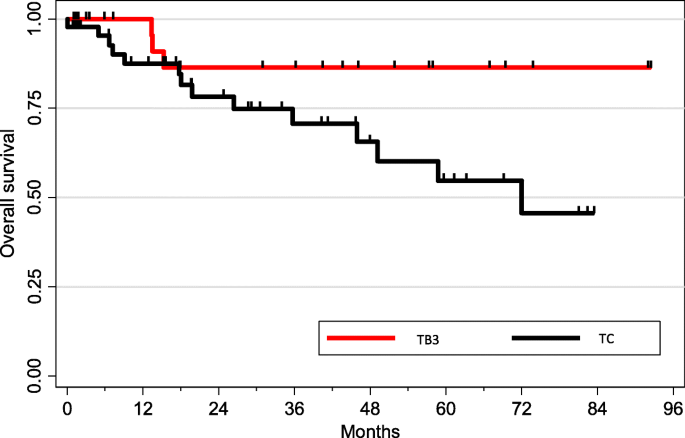
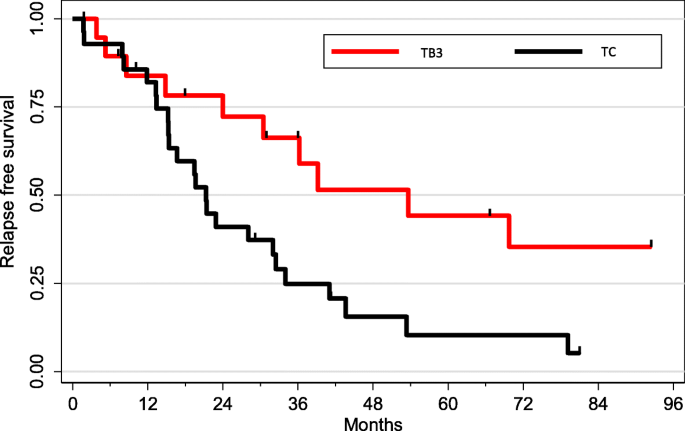
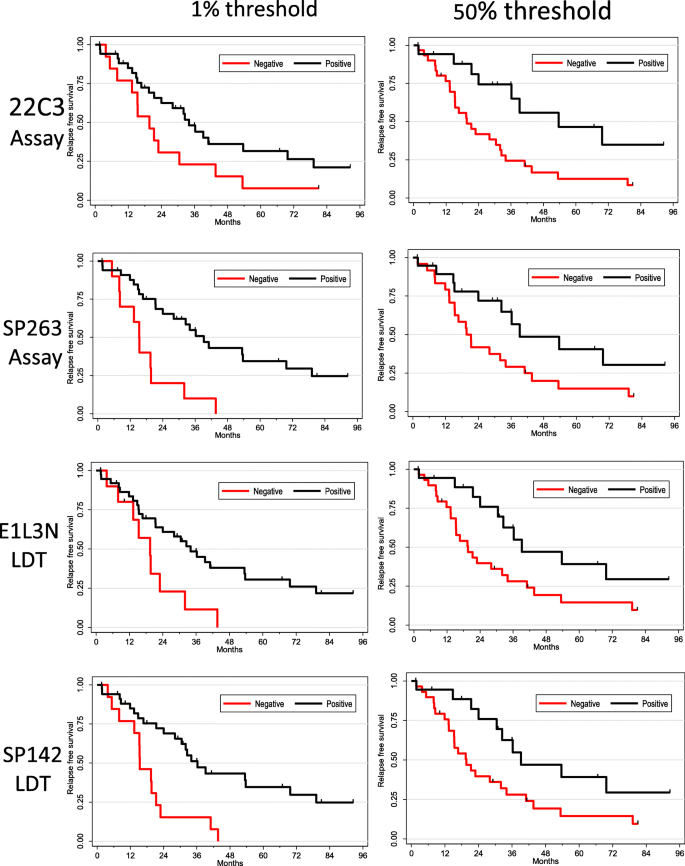
结果解读显示,PD-L1表达与肿瘤分期无关,但与副肿瘤综合征的发生显著相关;TB3患者的总生存期和无复发生存期显著优于TC(p=0.04,p=0.01);在TB3亚组中,高PD-L1表达与更好的无复发生存期相关,无论使用哪种抗体或阳性阈值(1%或50%),无复发生存期几乎翻倍。产品关联:文献未提及具体实验产品,领域常规使用STATA等统计分析软件。
4. Biomarker研究及发现成果
本研究的核心Biomarker为PD-L1,其类型为免疫检查点分子,筛选与验证逻辑为:基于多中心标准化大样本,对比四种经临床验证的PD-L1抗体,通过全切片免疫组化检测评估表达特征,结合统计学分析关联临床病理参数及预后,明确其作为TET免疫治疗生物标志物的价值。
研究过程中,Biomarker来源为103例TB3和TC的FFPE临床样本,验证方法为不同自动化平台的免疫组化检测,特异性方面,TB3上皮细胞的PD-L1表达显著高于TC(p<0.0001),50%阳性阈值下TB3阳性率为81%-92%,TC为20%-24%;敏感性方面,1%阳性阈值下TB3阳性率为92%-98%,TC为66%-73%。
核心成果方面,首次明确四种PD-L1抗体在TET检测中的一致性,建立了可重复的实验室检测方法;明确PD-L1在TB3中呈高弥漫性表达,在TC中呈局灶异质性表达,1%和50%阳性阈值可有效区分TB3与TC;首次发现TB3中高PD-L1表达与更好的无复发生存期相关(文献未明确提供HR值),为TET免疫治疗的患者筛选提供了关键依据;同时证实PD-L2不适用于TET的免疫生物标志物,PD1和CD8的表达与PD-L1无显著关联。本研究的创新性在于首次在大样本中系统评估肺癌伴随诊断级PD-L1抗体在TET中的应用,明确其表达特征及预后价值,为TET免疫治疗的临床转化奠定了基础。
