1. 领域背景与文献引入
文献英文标题:Global target mRNA specification and regulation by the RNA-binding protein ZFP36;发表期刊:Genome Biology;影响因子:10.43(2014年);研究领域:RNA结合蛋白介导的转录后基因调控,AU-rich元件(ARE)的功能与组合调控机制
转录后调控是基因表达调控网络的核心环节之一,RNA结合蛋白(RBP)与非编码RNA通过识别RNA调控元件(RRE),精准调控mRNA的剪接、多聚腺苷酸化、核输出、稳定性及翻译效率等过程。AU-rich元件(ARE)是一类位于mRNA 3"非翻译区(UTR)的保守顺式调控元件,最初发现于细胞因子、免疫应答相关基因的不稳定转录本中,通过结合不同功能的RBP实现对mRNA稳定性的动态调控。其中,ELAVL1(又称HuR)与ZFP36(又称TTP)是两类研究最为深入的ARE结合RBP,但功能完全拮抗:ELAVL1通过结合ARE序列稳定靶标mRNA,而ZFP36则促进靶标mRNA的降解。
此前的研究已通过光激活核糖核苷交联免疫沉淀(PAR-CLIP)等技术系统解析了ELAVL1的全基因组结合特异性与调控模式,但ZFP36的体内结合偏好尚未在全基因组水平得到精准验证,且两者在转录组范围内的组合调控机制仍不明确。针对这一研究空白,本研究利用PAR-CLIP技术解析ZFP36的体内RNA结合特异性,结合转录组分析与偏相关量化模型,揭示ZFP36与ELAVL1对ARE的组合调控规律,为转录后调控网络的解析提供了新的技术方法与理论依据。
2. 文献综述解析
作者对领域内现有研究的分类维度主要围绕RBP的功能属性(稳定/降解mRNA)、研究技术体系(体外生化实验/体内组学实验)及调控模式(单独调控/组合调控)展开。现有研究中,ELAVL1的相关研究较为系统,已通过PAR-CLIP技术明确其结合序列偏好为U-rich和CU-rich序列,并证实其通过核质穿梭实现对mRNA稳定性的调控;而ZFP36的研究多集中于体外结合实验,已明确其通过串联CCCH锌指结构(TZF)结合经典ARE序列(如非amer UUAUUUAUU)并招募降解复合物促进mRNA降解,但体内全基因组水平的结合特异性及功能验证仍存在不足。此外,已有少量研究提示ELAVL1与ZFP36可能通过竞争结合ARE序列实现功能拮抗,但缺乏全基因组水平的直接证据,且两者组合调控的序列基础与功能效应尚未被量化解析。
本研究的核心创新价值在于填补了ZFP36体内结合特异性研究的空白,首次在全基因组水平建立了ZFP36体外结合亲和力与体内结合偏好的定量关联,并通过偏相关分析技术排除混杂因素干扰,精准量化了ZFP36与ELAVL1的组合调控效应,为ARE介导的转录后组合调控机制研究提供了范式。
3. 研究思路总结与详细解析
本研究的整体目标是解析ZFP36的体内RNA结合特异性及与ELAVL1的组合调控机制,核心科学问题包括ZFP36在体内的结合序列偏好、结合位点的功能效应,以及两者组合调控的序列基础与模式。技术路线遵循“体内结合位点鉴定→调控效应验证→组合调控解析→跨物种验证”的闭环逻辑:首先通过PAR-CLIP技术在人类HEK293细胞中鉴定ZFP36的全基因组结合位点;然后通过转录组分析与偏相关解析ZFP36结合对mRNA丰度的直接调控效应;接着对比ZFP36与ELAVL1的结合位点与序列偏好,解析组合调控模式;最后利用ZFP36敲除小鼠细胞的mRNA稳定性数据验证人类细胞中的发现。
3.1 ZFP36体内结合位点的全基因组鉴定
实验目的:鉴定ZFP36在人类细胞中的全基因组RNA结合位点及结合区域偏好,明确其靶标转录本的功能特征。
方法细节:构建四环素诱导的FLAG/HA标签ZFP36表达HEK293细胞系,通过PAR-CLIP技术交联ZFP36与RNA复合物,经免疫沉淀、SDS-PAGE分离后,对结合的RNA进行高通量测序;利用PARalyzer软件分析测序数据中的T-to-C转换位点(PAR-CLIP技术特异性标记),确定ZFP36的结合位点,并结合基因本体(GO)分析靶标基因的功能富集。
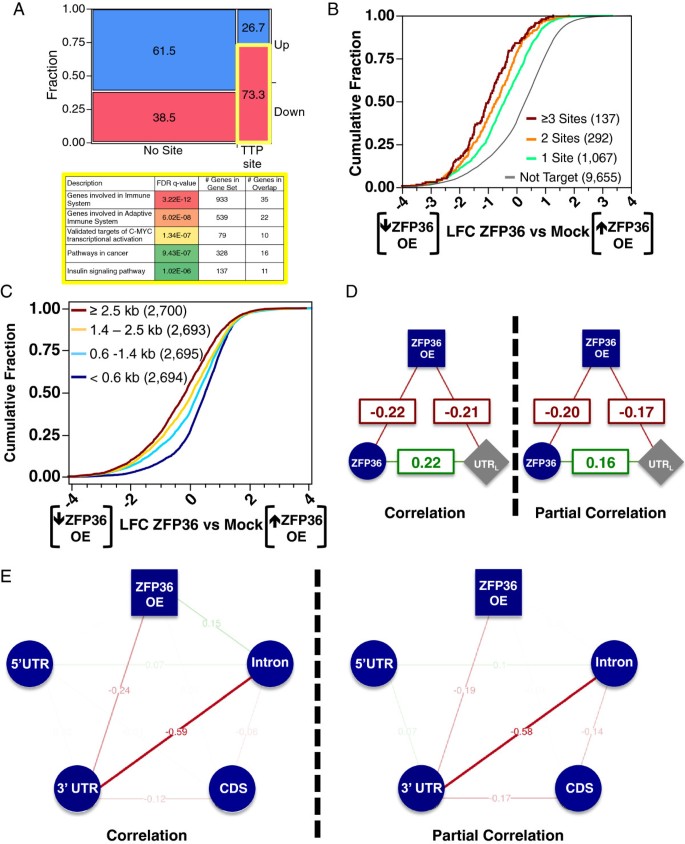
结果解读:共鉴定到4626个ZFP36结合位点,其中70%位于mRNA的3"UTR区域,且在3"UTR的最后100个核苷酸区域显著富集(图1E),这一空间分布与ZFP36促进mRNA去腺苷酸化的功能一致;结合位点中富含经典ARE序列,包括非amer UUAUUUAUU(8%)、八聚体UAUUUAUU(14%)等;GO分析显示,ZFP36结合的转录本主要编码转录与转录后调控蛋白,包括其他RBP(如ZFP36家族成员、ELAVL1等)(图2A-F),提示ZFP36可能通过调控其他RBP的表达参与转录后调控网络的层级调控。
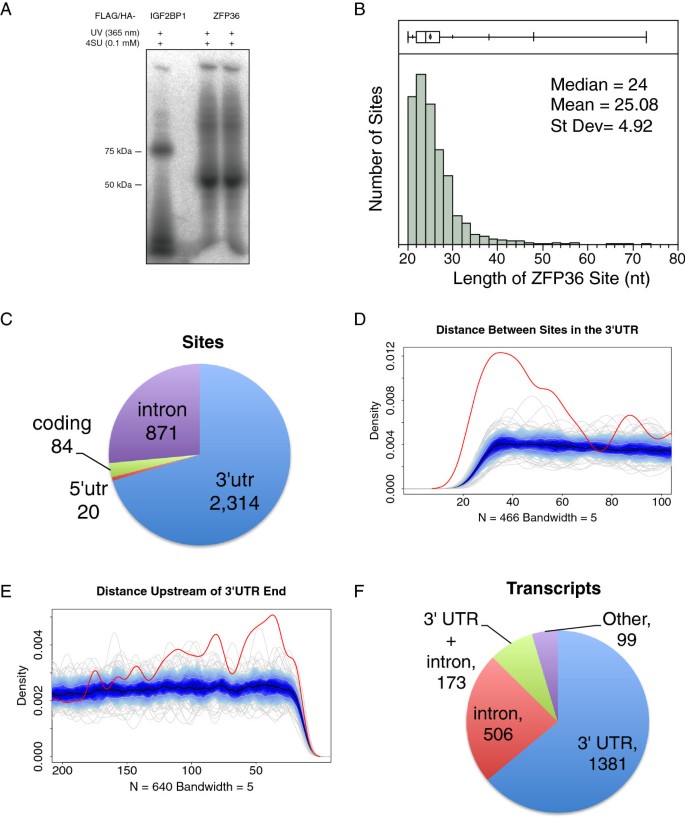
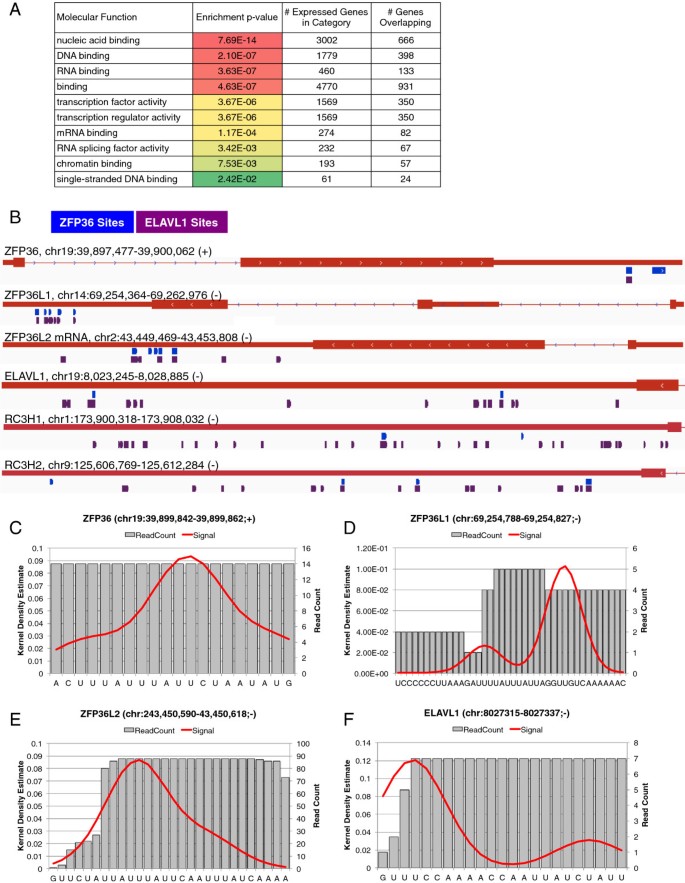
产品关联:实验所用关键产品:Flp-In™ T-REx™ 293细胞系(Life Technologies)、doxycycline(Sigma)、Illumina高通量测序平台、Affymetrix Human Genome U133 Plus 2.0基因芯片等。
3.2 ZFP36结合特异性的体内外关联分析
实验目的:验证ZFP36体内结合偏好与体外结合亲和力的一致性,解析序列特征对结合特异性的影响。
方法细节:计算ZFP36 3"UTR结合位点中各ARE序列基序的信号噪声比(SNR),反映基序在结合位点中的富集程度;将SNR值与此前报道的体外荧光各向异性实验测得的结合解离常数(Kd)进行相关性分析;通过在ARE半位点间插入不同类型的间隔核苷酸,预测其对ZFP36结合亲和力的影响。
结果解读:体内SNR值与体外Kd值呈显著负相关(相关系数R²=0.79),表明ZFP36的体内结合特异性与体外结合亲和力高度一致(图3C);在八聚体UAUUUAUU的半位点间插入非尿苷酸会显著升高预测Kd值(降低结合亲和力),而插入尿苷酸则对结合亲和力影响较小(图3D);五聚体AUUUA在ZFP36结合位点中的富集程度是背景的40-250倍,显著高于同长度的poly-U序列(图3A)。
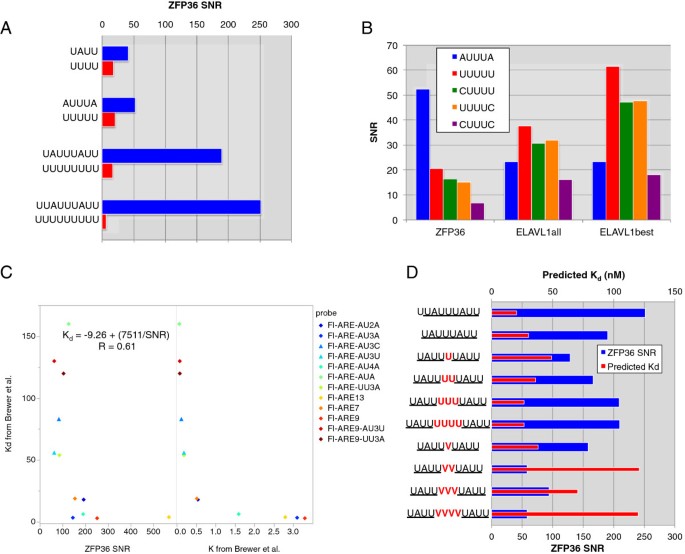
产品关联:文献未提及具体实验产品,领域常规使用荧光分光光度计、生物信息学分析软件(R、Python)等。
3.3 ZFP36对mRNA丰度的调控效应解析
实验目的:明确ZFP36结合对靶标mRNA丰度的调控效应,排除3"UTR长度等混杂因素的干扰,验证调控效应的直接性。
方法细节:在HEK293细胞中诱导EGFP-ZFP36过表达,通过荧光激活细胞分选(FACS)富集阳性细胞,提取RNA后进行微阵列转录组分析;采用偏相关分析方法,排除3"UTR长度的影响,量化ZFP36结合位点数量与mRNA丰度变化的直接关联;对比ZFP36敲除小鼠成纤维细胞与野生型细胞的mRNA半衰期数据,验证人类细胞中ZFP36的调控效应。
结果解读:ZFP36过表达导致1254个基因的mRNA显著下调,平均下调倍数为3.5倍(n=5,P<0.01,Bonferroni校正),这些下调基因显著富集ARE序列;偏相关分析显示,ZFP36 3"UTR结合位点数量与mRNA下调程度呈显著负相关,且该关联独立于3"UTR长度的影响(图4D);ZFP36敲除小鼠细胞中mRNA半衰期延长的基因,显著富集于人类细胞中ZFP36的结合靶标(P=0.003),证实ZFP36的调控效应在物种间保守。
产品关联:实验所用关键产品:EGFP-ZFP36表达载体、Becton Dickinson FACSAria II流式分选系统、Affymetrix Human Genome U133 Plus 2.0基因芯片等。
3.4 ZFP36与ELAVL1的组合调控机制解析
实验目的:解析ZFP36与ELAVL1在全基因组水平的组合调控模式,明确两者组合调控的序列基础与功能效应。
方法细节:对比ZFP36与ELAVL1的PAR-CLIP结合位点,分析两者的重叠程度及空间分布;采用偏相关分析,量化ZFP36与ELAVL1结合位点对ZFP36过表达后mRNA丰度变化的独立贡献;分析不同序列基序在重叠结合位点与ELAVL1特异性位点中的富集差异。
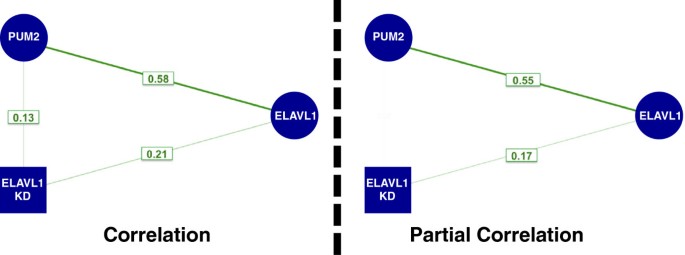
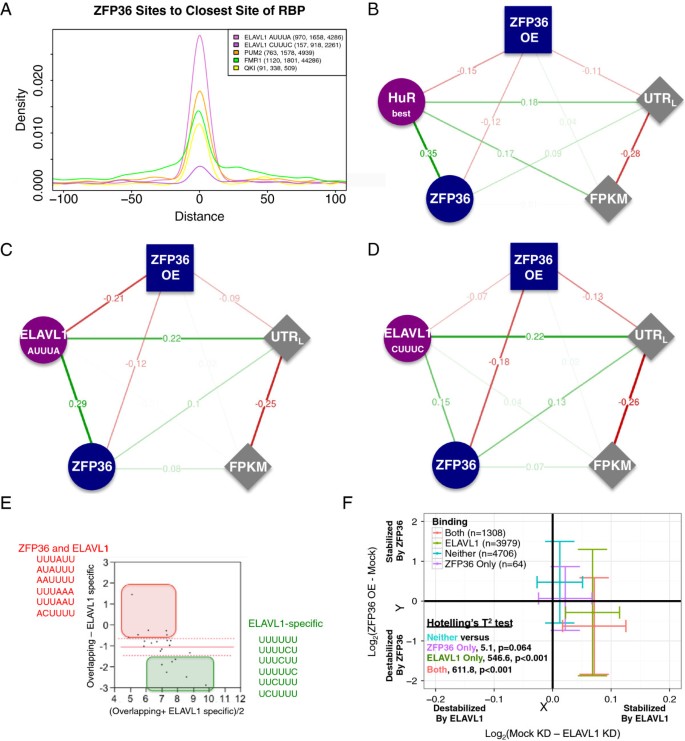
结果解读:1313个基因的3"UTR中存在ZFP36与ELAVL1的重叠结合位点,其中84%的ZFP36 3"UTR结合位点与ELAVL1位点重叠;序列分析显示,ZFP36偏好结合AU-rich序列,而ELAVL1偏好结合U-rich和CU-rich序列,重叠位点更富集AU-rich基序(图5E);偏相关分析显示,含AUUUA基序的ELAVL1位点对ZFP36过表达后mRNA丰度变化的解释度显著高于含CUUUC基序的位点(图5C-D);同时含两者结合位点的转录本,在ZFP36过表达时下调更显著,在ELAVL1敲低时上调更显著,证实两者的功能拮抗效应(图5F)。
产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析软件(R、Python)、公共数据库(doRiNA)等。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究中涉及的Biomarker为ZFP36结合的ARE序列基序,包括经典非amer UUAUUUAUU、八聚体UAUUUAUU、半位点UAUU及五聚体AUUUA等,属于转录后调控层面的功能元件Biomarker。其筛选与验证逻辑为:通过PAR-CLIP技术鉴定ZFP36体内结合位点→分析位点中的序列基序富集特征→结合体外结合实验验证基序的结合亲和力→通过转录组分析与小鼠敲除模型验证基序的调控功能,形成完整的“筛选-验证-功能”链条。
研究过程详述
这些ARE基序来源于人类HEK293细胞的mRNA 3"UTR区域,通过PAR-CLIP技术捕获ZFP36与RNA的交联复合物,经高通量测序与生物信息学分析鉴定结合位点;利用信号噪声比(SNR)计算各基序在结合位点中的富集程度,结果显示AUUUA五聚体在ZFP36位点中的富集程度是背景的40-250倍,显著高于同长度的poly-U序列;通过与体外荧光各向异性实验测得的Kd值关联,证实体内SNR值与体外结合亲和力呈显著负相关;功能验证方面,含这些ARE基序的转录本在ZFP36过表达时显著下调,且在ZFP36敲除小鼠细胞中mRNA半衰期显著延长(P=0.003)。
核心成果提炼
本研究鉴定的ARE基序是ZFP36介导mRNA降解的特异性功能Biomarker,其中AUUUA五聚体及相关的非amer、八聚体基序具有最高的结合特异性与调控效应;首次揭示ZFP36与ELAVL1通过偏好不同的ARE亚基序实现组合调控:ZFP36优先结合AU-rich序列促进降解,ELAVL1优先结合U-rich/CU-rich序列促进稳定,两者在重叠的AU-rich位点形成竞争,实现对mRNA稳定性的动态调控;同时建立了体内结合偏好与体外结合亲和力的定量关联模型,为预测RBP的靶标转录本提供了新方法。统计学结果显示,ZFP36靶标基因在ZFP36敲除小鼠细胞中mRNA半衰期延长的富集显著性为P=0.003,ZFP36过表达下调基因的平均倍数为3.5倍(n=5,P<0.01,Bonferroni校正)。