1. 领域背景与文献引入
文献英文标题:Natural cutaneous anthrax infection, but not vaccination, induces a CD4+ T cell response involving diverse cytokines;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:炭疽病免疫机制与新型疫苗研发
炭疽病是由炭疽芽孢杆菌引起的烈性人兽共患病,传统保护性免疫研究长期聚焦于中和抗体的作用,尤其是针对炭疽保护性抗原(PA)的抗体被认为是现有疫苗的核心保护机制。随着免疫研究的深入,T细胞免疫在细菌感染中的保护作用逐渐受到关注,尤其是Th17细胞分泌的IL-17A在多种小鼠感染模型中被证实为清除病原体的必需因子。然而,动物模型的研究结果如何转化到人类自然感染和疫苗接种的免疫反应中,尚未完全明确。现有炭疽疫苗如英国许可的炭疽沉淀疫苗(AVP)基于炭疽芽孢杆菌培养上清制备,主要诱导针对PA的中和抗体反应,但这种免疫反应的持久性和广谱性存在局限性,无法完全模拟自然感染后产生的长期保护性免疫。当前研究空白在于,自然皮肤炭疽感染与疫苗接种诱导的CD4+T细胞细胞因子反应谱差异尚未被系统解析,这一差异的明确对新型炭疽疫苗的理性设计具有关键指导意义。本研究正是针对这一空白,对比了自然感染康复者与疫苗接种者针对炭疽致死因子(LF)IV结构域的CD4+T细胞细胞因子反应,为新型疫苗研发提供实验依据。
2. 文献综述解析
作者在综述部分以炭疽病保护性免疫的研究进展为核心逻辑,从传统的抗体免疫机制过渡到T细胞免疫的新兴研究,系统梳理了动物模型与人类研究的差异,最终聚焦于现有疫苗与自然感染诱导免疫反应的未知差异,为本次研究的开展奠定理论基础。
现有研究表明,针对炭疽芽孢杆菌的保护性免疫长期以来被认为依赖于中和抗体,尤其是针对PA的抗体能够阻断炭疽毒素的细胞结合过程,从而发挥保护作用。近年来,T细胞免疫在细菌感染中的作用逐渐凸显,IL-17A作为Th17细胞的标志性细胞因子,在多种细菌感染小鼠模型中被证实是清除病原体的必需因子。在炭疽病研究中,小鼠模型显示灭活芽孢疫苗诱导的保护依赖于Th1细胞分泌的IFNγ,但人类自然感染后的T细胞免疫特征仍不明确。现有商业化炭疽疫苗如AVP和美国的AVA疫苗,均基于炭疽芽孢杆菌培养上清制备,含有PA、LF和水肿因子(EF)等毒素成分,但疫苗诱导的免疫反应主要集中于PA特异性中和抗体,对LF等其他毒素成分的免疫反应较弱,且这种免疫反应的记忆持久性不足。此外,炭疽毒素在体外实验中被证实能够抑制T细胞的活化和细胞因子分泌,如LF通过丝裂原活化蛋白激酶(MAPK)通路抑制T细胞增殖和IFNγ、TNFα等细胞因子的产生,EF则可通过升高细胞内cAMP水平诱导Th2细胞分化,但这些体外结果与人类自然感染后的体内免疫反应是否一致仍不清楚。
本研究的创新价值在于,首次系统对比了人类自然皮肤炭疽感染与AVP疫苗接种后,针对LF IV结构域的CD4+T细胞细胞因子反应谱,明确了两者之间的显著差异,填补了人类炭疽T细胞免疫研究的空白,为新型疫苗设计提供了关键方向。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确自然皮肤炭疽感染与AVP疫苗接种者针对炭疽LF IV结构域的CD4+T细胞细胞因子反应差异,核心科学问题是自然感染与疫苗诱导的免疫反应是否存在极化差异,以及这种差异对新型炭疽疫苗设计的指导意义,技术路线遵循“样本招募→体外刺激→细胞因子检测→统计分析→结论推导”的闭环逻辑。
3.1 研究对象招募与外周血单个核细胞样本制备
实验目的是获取具有不同炭疽暴露史的人类外周血单个核细胞(PBMC)样本,为后续体外免疫反应检测提供实验材料。方法细节:研究共招募三组人群,第一组为9名土耳其炭疽流行区的皮肤炭疽康复者,均在8年内发生过自然感染;第二组为10名英国常规接种AVP疫苗的志愿者,接种时间至少4.5年且每年接种一次;第三组为10名无炭疽暴露史的健康对照。采用Sigma-Aldrich的Accuspin管结合Histopaque-1077分离外周血中的外周血单个核细胞,离心条件为800g离心30分钟,收集界面层细胞后用AIM-V无血清培养基洗涤两次,调整细胞浓度至2×10^6细胞/ml。结果解读:成功从三组研究对象中分离得到合格的外周血单个核细胞样本,细胞活力符合实验要求,为后续的抗原刺激实验奠定了基础。实验所用关键产品:Sigma-Aldrich的Accuspin管;文献未提及Histopaque-1077分离液、AIM-V无血清培养基的具体品牌,领域常规使用同类外周血单个核细胞分离试剂、无血清细胞培养基。
3.2 抗原刺激与细胞因子多维度检测
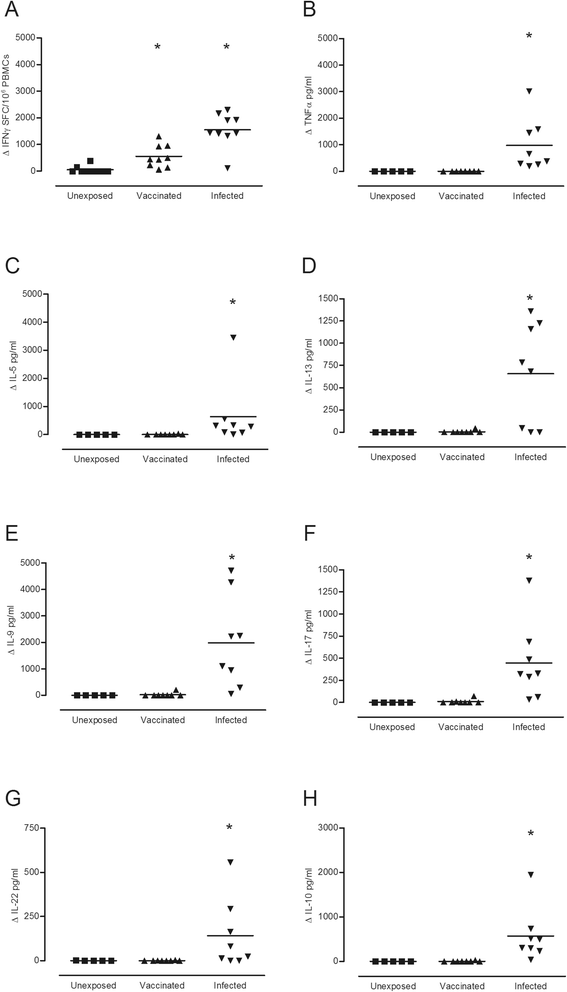
实验目的是对比三组研究对象的外周血单个核细胞在LF IV结构域刺激后的细胞因子分泌谱差异,明确不同暴露史诱导的免疫反应特征。方法细节:将调整好浓度的外周血单个核细胞接种于96孔ELISpot板,分别加入25μg/ml的LF IV结构域蛋白作为刺激原,或仅加入AIM-V培养基作为阴性对照,体外培养72小时。培养结束后,收集细胞培养上清,采用ELISpot法检测CD4+T细胞分泌的IFNγ水平;采用Bio-Rad的Bioplex多因子检测试剂盒,结合Luminex 200系统检测上清中IL-5、IL-9、IL-10、IL-13、IL-17和TNFα的浓度;采用eBioscience的IL-22 ELISA试剂盒,结合BIO-Tek的μQuant ELISA酶标仪检测IL-22的浓度。所有细胞因子浓度均以Δpg/ml表示,即刺激组浓度减去阴性对照组浓度,采用Kruskal Wallis非参数检验结合Dunns多重比较进行统计学分析。结果解读:自然皮肤炭疽感染康复者的外周血单个核细胞在LF IV刺激后,分泌的IFNγ(n=8-9,P<0.001)、TNFα(n=8-9,P<0.001)、IL-5(n=8-9,P<0.001)、IL-9(n=8-9,P<0.001)、IL-10(n=8-9,P<0.001)、IL-13(n=8-9,P=0.045)、IL-17(n=8-9,P=0.002)和IL-22(n=8-9,P=0.03)水平均显著高于健康对照组;而AVP疫苗接种者仅IFNγ水平显著高于对照组(n=8-10,P=0.002),其他细胞因子水平与对照组无显著差异。这一结果表明,自然感染诱导了广泛的CD4+T细胞细胞因子反应,涵盖Th1、Th2、Th9、Th17和Th22等多种Th亚型,而疫苗接种仅诱导了极化的Th1型IFNγ反应。
3.3 统计学分析与差异验证
实验目的是通过统计学方法明确三组研究对象细胞因子反应的显著性差异,确保实验结果的可靠性。方法细节:采用GraphPad Prism软件进行统计学分析,对三组间的细胞因子Δ值采用Kruskal Wallis非参数检验,组间多重比较采用Dunns检验,以P≤0.05为差异有统计学意义。结果解读:统计学分析进一步验证了自然感染组与疫苗组、对照组之间的显著差异,自然感染组的多种细胞因子反应均显著强于疫苗组和对照组,而疫苗组仅IFNγ反应显著,其他细胞因子反应与对照组无差异。这一结果明确了自然感染与疫苗接种诱导的CD4+T细胞免疫反应的本质差异,为后续结论的推导提供了统计学依据。
4. Biomarker研究及发现成果解析
本研究中,自然感染诱导的广谱CD4+T细胞细胞因子反应谱可作为潜在的炭疽保护性免疫Biomarker,而疫苗诱导的单一IFNγ反应可作为现有疫苗免疫效果的Biomarker,两者的差异为新型疫苗的评估提供了参考标准。
Biomarker定位:本研究涉及的Biomarker为CD4+T细胞分泌的多种细胞因子(IFNγ、IL-5、IL-9、IL-10、IL-13、IL-17、IL-22),筛选逻辑为通过对比自然感染康复者、疫苗接种者与健康对照的细胞因子反应,鉴定出仅在自然感染组显著升高的细胞因子谱,作为自然感染诱导的保护性免疫特征;而单一IFNγ反应为疫苗诱导的免疫特征。
研究过程详述:Biomarker的来源为人类外周血单个核细胞经LF IV结构域体外刺激72小时后的细胞培养上清,验证方法包括ELISpot(IFNγ)、Luminex多因子检测(IL-5、IL-9、IL-10、IL-13、IL-17、TNFα)和ELISA(IL-22),所有检测均采用标准化的实验流程,确保结果的准确性。特异性与敏感性数据显示,自然感染组中各细胞因子的Δ值均显著高于健康对照组,其中IFNγ的敏感性在疫苗组也有体现,但其他细胞因子仅在自然感染组表现出显著反应,提示广谱细胞因子反应具有更高的特异性,可作为自然感染后保护性免疫的标志。
核心成果提炼:本研究首次发现自然皮肤炭疽感染诱导的CD4+T细胞反应涵盖多种Th亚型的细胞因子,包括Th1型的IFNγ、TNFα,Th2型的IL-5、IL-13,Th9型的IL-9,Th17型的IL-17,以及Th22型的IL-22,而AVP疫苗仅诱导极化的Th1型IFNγ反应。该Biomarker的创新性在于,首次明确了自然感染与疫苗诱导的炭疽免疫反应的细胞因子谱差异,其中IL-22在炭疽免疫中的作用为首次报道,提示IL-22在皮肤黏膜屏障的抗菌免疫中可能发挥关键作用。统计学结果显示,自然感染组的多种细胞因子水平与疫苗组、对照组存在显著差异(P值范围为0.03至<0.001,样本量n=8-9),为该Biomarker的临床应用提供了实验依据。此外,该研究结论提示,新型炭疽疫苗需要诱导类似自然感染的广谱细胞因子反应,才能获得更持久、更有效的保护性免疫。
