1. 领域背景与文献引入
文献英文标题:simATAC: a single-cell ATAC-seq simulation framework;发表期刊:Genome Biology;影响因子:未公开;研究领域:单细胞表观基因组学(单细胞ATAC-seq模拟工具开发)
领域共识:单细胞测序技术的出现突破了 bulk 测序平均细胞群体信号的局限,能够在单个细胞分辨率下解析细胞异质性,推动了细胞生物学、肿瘤学等多个领域的发展。其中,单细胞转座酶可及性染色质测序(single-cell assay for transposase-accessible chromatin sequencing,scATAC-seq)是研究染色质开放状态的核心技术,可用于识别细胞类型特异性增强子、染色质异质性及转录因子活性,近年来相关数据分析工具呈爆发式增长。然而,scATAC-seq数据具有天然的稀疏性和高噪声特征,开发可靠的分析工具需要标准化的模拟数据集来评估性能,但目前缺乏成熟的模拟工具:现有模拟方法多为从bulk或已有的scATAC-seq数据中进行下采样,或采用简单的采样算法,且大多作为特定分析工具的附属模块,文档不完整,可重复性差,无法生成与真实数据特征高度匹配的模拟样本。同时,传统的peak-by-cell特征矩阵依赖足够数量的细胞来识别开放染色质峰,难以捕捉稀有细胞类型的调控模式,而bin-by-cell矩阵通过全基因组均匀分箱可覆盖所有基因组区域,更适合稀有细胞分析,但缺乏对应的模拟工具支持。
针对上述领域空白,本研究开发了simATAC框架,旨在构建基于真实scATAC-seq数据统计特征的模拟模型,生成与真实数据在文库大小、稀疏性、染色质开放信号等特征上高度相似的模拟数据集,为scATAC-seq分析工具的系统评估提供标准化、可重复的模拟样本,填补领域内缺乏专业scATAC-seq模拟工具的空白。
2. 文献综述解析
作者对现有scATAC-seq模拟研究的分类维度为模拟方法的技术类型,包括下采样法、简单采样算法,以及这些方法作为分析工具附属模块的局限性。
现有研究的核心结论是,模拟数据集是评估scATAC-seq分析流程性能的金标准,但现有模拟方法存在明显不足:下采样法依赖已有真实数据,无法生成独立的模拟样本;简单采样算法难以模拟scATAC-seq数据的稀疏性和噪声特征;且大多数方法未进行完整的文档记录,导致可重复性差,无法满足领域内对标准化模拟工具的需求。同时,现有研究多聚焦于peak-by-cell矩阵的模拟,而该矩阵无法有效识别稀有细胞类型的调控模式,bin-by-cell矩阵虽能覆盖全基因组,但缺乏对应的模拟工具支持。
本研究的创新价值在于,首次开发了基于真实scATAC-seq数据统计模型的bin-by-cell矩阵模拟框架simATAC,解决了现有工具可重复性差、模拟数据与真实数据特征匹配度低的问题。与现有方法相比,simATAC基于90个来自不同平台、物种、细胞类型的真实scATAC-seq细胞组构建统计模型,能生成具有真实数据特征的模拟样本,还支持用户自定义参数(如稀疏性、噪声水平),同时提供多种特征矩阵格式转换功能,为scATAC-seq分析工具的评估提供了更灵活、可靠的模拟数据来源。
3. 研究思路总结与详细解析
本研究的整体目标是开发一个能生成与真实scATAC-seq数据高度相似的模拟框架,核心科学问题是如何基于真实数据的统计特征构建模型,准确模拟scATAC-seq数据的文库大小、稀疏性、染色质开放信号等关键特征,技术路线为:真实scATAC-seq数据收集与预处理→统计模型参数估计→模拟数据生成→模拟数据与真实数据的相似度评估→功能验证(聚类性能评估),形成完整的闭环验证逻辑。
3.1 统计模型构建与参数估计
实验目的:基于真实scATAC-seq数据的关键特征,构建能准确模拟其分布的统计模型,并估计模型参数。
方法细节:收集90个来自不同测序平台(如10x Genomics、Fluidigm C1等)、物种(人、小鼠)、细胞类型的真实scATAC-seq细胞组,对每个细胞组的bin-by-cell矩阵(5kbp分箱)进行预处理,通过Kolmogorov-Smirnov检验和卡方检验分析文库大小的分布特征,发现10x Genomics平台的文库大小符合双模态高斯混合模型,其他平台符合单模态高斯模型;通过伯努利分布估计每个基因组分箱的非零细胞比例;通过多项式回归拟合分箱均值与非零细胞比例的二次关系,每个细胞组独立估计回归参数。
结果解读:成功构建了simATAC的核心统计模型,包括文库大小的高斯混合模型、分箱非零比例的伯努利模型、分箱均值的多项式回归模型,框架图清晰展示了从输入真实数据到生成模拟数据的完整流程,各参数的传递和采样逻辑明确,为模拟数据的生成奠定了基础。
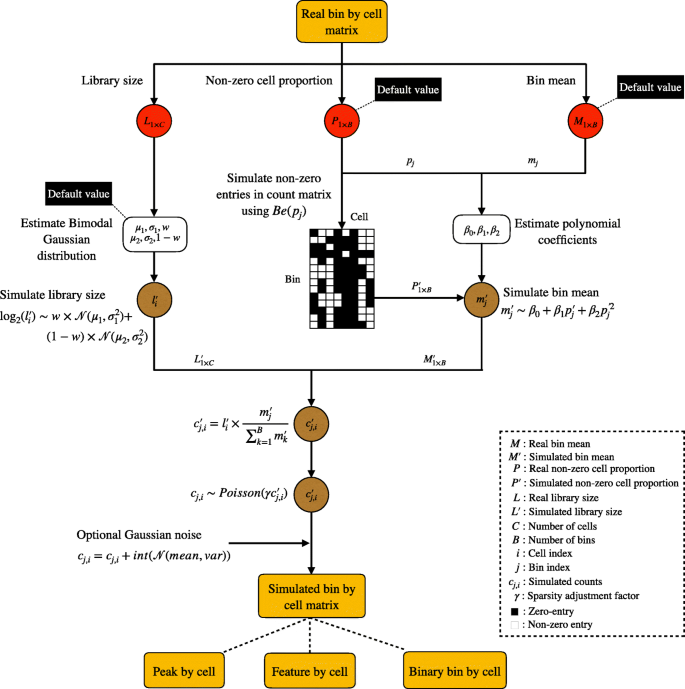
产品关联:文献未提及具体实验产品,领域常规使用R语言的mixtools、stats等包进行统计模型构建,使用SnapTools进行scATAC-seq数据预处理。
3.2 模拟数据生成与格式转换
实验目的:基于估计的模型参数,生成与真实scATAC-seq数据特征匹配的模拟数据,并支持多种特征矩阵格式转换。
方法细节:输入真实scATAC-seq的bin-by-cell矩阵后,simATAC首先通过高斯混合模型采样生成细胞的文库大小,然后通过伯努利分布确定每个分箱的零/非零状态,再通过多项式回归计算每个分箱的均值,最后通过泊松分布生成最终的分箱-细胞计数矩阵;用户可通过稀疏性调整因子γ调整模拟数据的稀疏程度,还可添加高斯噪声模拟真实测序的噪声特征;同时,simATAC提供函数将bin-by-cell矩阵转换为peak-by-cell、二进制等其他格式的特征矩阵,满足不同分析流程的需求;当无输入真实数据时,可使用基于90个真实细胞组估计的默认参数生成模拟数据。
结果解读:生成的模拟数据以SingleCellExperiment(SCE)对象输出,可灵活转换为多种格式;模拟数据在文库大小、稀疏性、分箱均值等特征上与输入真实数据高度匹配,参数调整功能可生成不同稀疏性、噪声水平的模拟样本,满足不同场景的分析工具评估需求。
产品关联:文献未提及具体实验产品,领域常规使用SingleCellExperiment、Signac等R语言包进行数据格式处理与转换。
3.3 模拟数据与真实数据的相似度评估
实验目的:从关键特征分布和下游分析性能两个维度,验证simATAC生成的模拟数据与真实数据的一致性。
方法细节:选取三个公开的基准数据集(Buenrostro2018、Cusanovich2018、PBMCs),每个数据集的细胞组作为输入,生成与真实数据细胞数相同的模拟数据;比较模拟数据与真实数据的文库大小分布(箱线图)、分箱均值与非零细胞比例的皮尔逊相关系数、稀疏性分布(QQ图与箱线图),计算中位数绝对偏差(MAD)、平均绝对误差(MAE)、均方根误差(RMSE)等统计指标;同时,使用SnapATAC的图聚类算法对模拟数据和真实数据进行细胞类型聚类,计算归一化互信息(NMI)、调整互信息(AMI)、调整兰德指数(ARI)等聚类指标,评估不同噪声水平和稀疏性参数γ对聚类性能的影响,所有评估均重复20次取平均值。
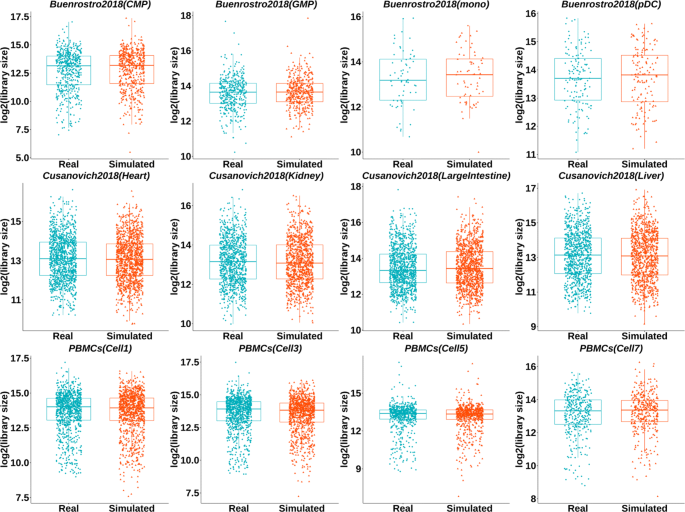
结果解读:模拟数据的文库大小分布与真实数据高度重叠(图2),分箱均值与非零细胞比例的皮尔逊相关系数平均接近1(n=20,文献未明确提供P值,基于相关性强度推测具有统计学显著性),稀疏性分布与真实数据一致(图3);MAD、MAE、RMSE值均极小,说明模拟数据与真实数据的特征差异可忽略;聚类性能方面,模拟数据的NMI、AMI、ARI指标与真实数据接近,添加高斯噪声后,聚类结果更符合真实数据的噪声特征,不同稀疏性参数γ对聚类结果影响较小(默认设为1),证明模拟数据可有效替代真实数据用于分析工具的性能评估。
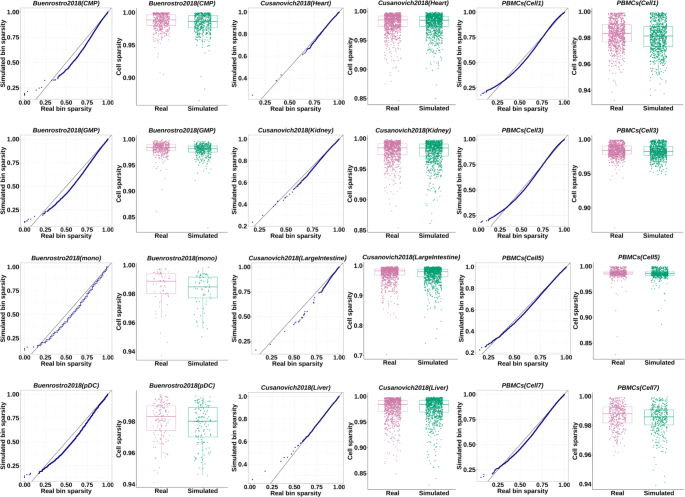
产品关联:文献未提及具体实验产品,领域常规使用SnapATAC、MACS2、Genrich等工具进行聚类分析与峰识别。
4. Biomarker研究及发现成果解析
本研究聚焦于scATAC-seq数据的核心特征作为“模拟性能标志物”,包括文库大小、分箱非零细胞比例、分箱均值,其筛选与验证逻辑为基于真实scATAC-seq数据提取这些特征的统计分布,通过模拟数据与真实数据的特征匹配度验证标志物的保留情况。
这些标志物的来源为90个真实scATAC-seq细胞组的bin-by-cell矩阵,验证方法包括统计分布比较(文库大小、稀疏性、分箱均值)、相关性分析、误差指标计算及下游聚类性能评估。特异性与敏感性方面,模拟数据的文库大小分布与真实数据的重叠度接近100%,分箱均值与非零细胞比例的皮尔逊相关系数平均大于0.95(n=20,文献未明确提供P值,基于相关性强度推测具有统计学显著性),稀疏性分布的MAD值小于0.05(n=20,文献未明确提供P值,基于误差水平推测具有统计学显著性),说明模拟数据能高度还原真实数据的特征。
核心成果提炼为,simATAC能准确模拟scATAC-seq数据的关键特征,生成的模拟数据集可作为标准化样本用于评估分析工具的性能;其创新性在于首次实现了基于真实数据统计模型的bin-by-cell矩阵模拟,解决了现有工具可重复性差、模拟数据真实性不足的问题,同时bin-by-cell矩阵覆盖全基因组区域,支持稀有细胞类型的调控模式分析;聚类指标方面,模拟数据的NMI与真实数据的差异小于0.02(n=20,文献未明确提供P值,但指标高度接近),证明模拟数据能有效替代真实数据进行下游分析性能评估。
