1. 领域背景与文献引入
文献英文标题:LncRNA SNHG16 as a potential biomarker and therapeutic target in human cancers;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤学(长非编码RNA与肿瘤生物标志物)

癌症是全球范围内导致死亡的重要原因,2018年全球新增癌症病例约1810万,癌症相关死亡病例达960万,尽管近年来对肿瘤分子机制的理解不断深入,治疗手段也取得了显著进展,但癌症患者的复发率和死亡率仍处于较高水平,因此亟需发掘新型、有效的生物标志物和治疗靶点。非编码RNA(ncRNA)在肿瘤发生发展中的作用逐渐受到关注,其中长非编码RNA(lncRNA)长度超过200个核苷酸,虽无蛋白编码功能,但可通过表观遗传修饰、转录调控、转录后调控等多种方式介导内源基因表达,其异常表达与肿瘤的恶性表型密切相关。目前已有多个肿瘤相关lncRNA被报道,但仍有大量lncRNA的功能、调控机制及临床价值尚未明确,长非编码RNA小核RNA宿主基因16(SNHG16)作为新型肿瘤相关lncRNA,其在不同肿瘤中的表达模式、功能作用及临床应用潜力缺乏系统梳理,本文献旨在整合已发表的研究成果,全面总结SNHG16在人类肿瘤中的研究进展,为其作为生物标志物和治疗靶点提供理论依据。
2. 文献综述解析
本文献综述部分以SNHG16的表达模式、功能作用、调控机制及临床价值为核心分类维度,系统梳理了领域内的现有研究。现有研究的关键结论显示,SNHG16在急性淋巴细胞白血病、膀胱癌、乳腺癌等多数人类肿瘤中呈现高表达趋势,仅在结直肠癌、肝细胞癌中存在表达争议,部分研究显示高表达,部分研究显示低表达;功能上,SNHG16参与调控肿瘤细胞的增殖、凋亡、侵袭转移及化疗耐药等恶性生物学行为;机制上,SNHG16主要通过作为竞争性内源RNA(ceRNA)吸附微小RNA(miRNA),或直接结合蛋白质调控靶基因表达;临床价值方面,SNHG16的异常表达与肿瘤患者的临床病理特征及预后密切相关,具备作为诊断和预后生物标志物的潜力。现有研究的优势在于覆盖了多种肿瘤类型,初步揭示了SNHG16的部分调控机制,为后续研究奠定了基础,但也存在局限性,如部分肿瘤中SNHG16的表达和功能结论存在矛盾,机制研究不够深入,缺乏大规模多中心临床验证数据。本研究的创新价值在于首次系统整合了SNHG16在各肿瘤中的研究成果,明确了其研究现状与争议点,为后续的机制研究和临床应用提供了全面的参考框架,解决了现有研究分散、结论不统一的问题。
3. 研究思路总结与详细解析
本文献为综述类研究,整体研究目标是系统总结SNHG16在人类肿瘤中的表达、功能、调控机制及临床价值,核心科学问题是明确SNHG16在不同肿瘤中的作用模式、调控网络及作为生物标志物的临床潜力,技术路线为通过检索已发表的相关研究文献,按表达模式、功能作用、调控机制、临床价值四个维度进行分类整理,分析研究中的共识与争议,最终总结SNHG16的研究现状并提出未来研究方向。
3.1 SNHG16在肿瘤中的表达模式梳理
本环节的核心目标是明确SNHG16在不同人类肿瘤中的表达水平及存在的争议点。研究方法为全面检索已发表的关于SNHG16在各肿瘤中表达的研究文献,整合肿瘤组织样本、细胞系中的表达数据,并分析表达差异的潜在原因。结果解读显示,SNHG16在急性淋巴细胞白血病、膀胱癌、乳腺癌、宫颈癌、神经母细胞瘤等多数肿瘤的组织样本及对应细胞系中均呈现高表达,但在结直肠癌和肝细胞癌中存在表达争议,部分研究显示SNHG16高表达,部分研究显示低表达,分析认为差异可能与RNA质量、肿瘤组织中肿瘤细胞比例、所使用细胞系的特性等因素有关。文献未提及具体实验产品,领域常规使用实时荧光定量PCR(qRT-PCR)检测lncRNA表达,使用临床组织样本库和已建立的肿瘤细胞系开展研究。
3.2 SNHG16的肿瘤功能及调控机制解析
本环节的核心目标是总结SNHG16在肿瘤中的功能作用及调控网络。研究方法为梳理已发表的功能实验和机制研究文献,涵盖细胞增殖、凋亡、侵袭转移、化疗耐药等功能实验,以及ceRNA机制、蛋白质结合机制等分子机制研究。结果解读显示,功能上,SNHG16可促进肿瘤细胞增殖、抑制细胞凋亡、通过调控上皮间质转化(EMT)过程促进肿瘤侵袭转移,还参与肿瘤细胞的化疗耐药;机制上,SNHG16主要通过两种方式发挥作用,一是作为ceRNA吸附miR-124-3p、miR-98、miR-200a-3p等多种miRNA,解除miRNA对下游靶基因的抑制作用,二是直接结合增强子zeste同源物2(EZH2)、转录因子SPI1/PU.1等蛋白质,调控靶基因的表达。
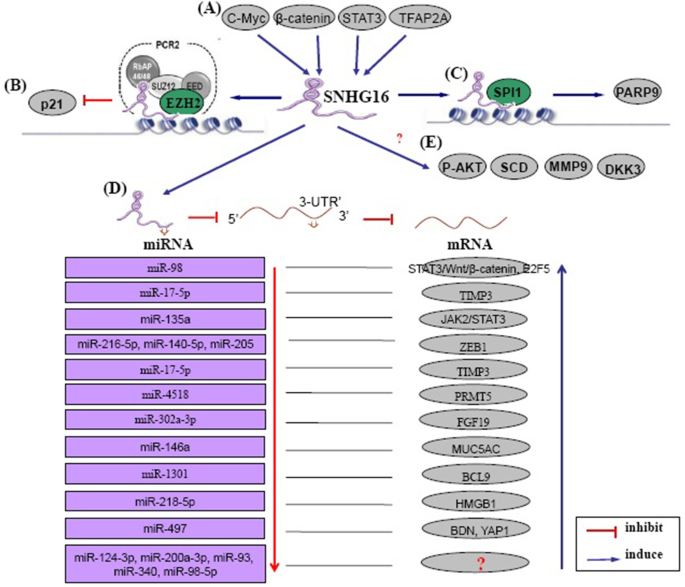
文献未提及具体实验产品,领域常规使用小干扰RNA(siRNA)、慢病毒载体进行基因沉默或过表达实验,使用双荧光素酶报告实验、RNA免疫沉淀(RIP)、RNA pull-down实验验证RNA之间的相互作用,使用流式细胞术检测细胞凋亡,使用Transwell实验检测细胞侵袭转移能力。
3.3 SNHG16的临床生物标志物价值分析
本环节的核心目标是评估SNHG16作为肿瘤诊断和预后生物标志物的潜力。研究方法为整合已发表的临床研究数据,分析SNHG16表达与肿瘤患者临床病理特征、生存预后的关系,以及其在体液样本中的诊断价值。结果解读显示,SNHG16的高表达与膀胱癌、宫颈癌、食管癌、胶质瘤等多种肿瘤的不良总生存期(OS)、无进展生存期(PFS)密切相关,可作为独立预后因子;单独将SNHG16作为诊断标志物时准确性较低,如乳腺癌患者血清中SNHG16的受试者工作特征(ROC)曲线下面积(AUC)为0.681,但与其他lncRNA联合组成的标志物panel可显著提高诊断准确性,如膀胱癌中由SNHG16、MEG3、MALAT1组成的三lncRNA panel,在训练集的AUC为0.857,敏感性为0.85,特异性为0.78,在验证集的AUC为0.826,敏感性为0.80,特异性为0.75,诊断效能显著优于尿液细胞学检查。文献未提及具体实验产品,领域常规使用qRT-PCR检测血清、血浆、外泌体等体液样本中的lncRNA表达,使用ROC曲线分析诊断价值,使用Kaplan-Meier生存曲线和Cox回归分析评估预后价值。
4. Biomarker研究及发现成果解析
Biomarker定位
SNHG16是一种肿瘤相关长非编码RNA生物标志物,其筛选逻辑为通过分析已发表的临床研究数据,明确其在肿瘤组织及体液样本中的表达差异,以及与患者临床病理特征和预后的相关性;验证逻辑为在多种肿瘤类型中开展组织样本表达检测、细胞功能实验及临床预后分析,多维度验证其生物标志物潜力。
研究过程详述
SNHG16的样本来源包括肿瘤组织样本、血清、血浆、血清外泌体等体液样本;验证方法主要包括实时荧光定量PCR检测SNHG16的表达水平,免疫组化(IHC)检测相关靶蛋白的表达,生存分析评估其与患者预后的关系,ROC曲线分析其诊断价值;特异性与敏感性方面,单独使用SNHG16作为诊断标志物时效能有限,如乳腺癌血清SNHG16的AUC为0.681(文献未明确样本量及P值),而与其他lncRNA联合使用时,膀胱癌三lncRNA panel在训练集的AUC为0.857(n=100,P<0.05),敏感性为0.85,特异性为0.78,验证集的AUC为0.826(n=320,P<0.05),敏感性为0.80,特异性为0.75。
核心成果提炼
核心成果显示,SNHG16可作为多种人类肿瘤的独立预后生物标志物,其高表达与膀胱癌、宫颈癌、食管癌等肿瘤患者的不良OS、PFS密切相关(部分研究显示风险比HR>1.5,P<0.05);创新性在于首次系统总结了SNHG16在各肿瘤中的生物标志物潜力,提出与其他lncRNA联合使用可显著提高诊断效能,为临床应用提供了新的方向;此外,SNHG16还具备作为肿瘤治疗靶点的潜力,其表达沉默可抑制肿瘤细胞的恶性生物学行为,为肿瘤的靶向治疗提供了新的候选分子。
