1. 领域背景与文献引入
文献英文标题:Roles of IFN-γ in tumor progression and regression: a review;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫与免疫治疗
肿瘤免疫治疗是当前肿瘤治疗领域的核心前沿方向,自2011年首个免疫检查点抑制剂伊匹木单抗获批以来,以PD-1/PD-L1抑制剂为代表的免疫治疗已在黑色素瘤、非小细胞肺癌等多种肿瘤中展现出显著的长期疗效,成为晚期肿瘤患者的重要治疗选择。领域共识:免疫检查点抑制剂的疗效高度依赖肿瘤微环境中有效的抗肿瘤免疫应答,而细胞因子作为免疫调控的核心分子,在其中发挥着关键的调控作用。干扰素-γ(IFN-γ)作为II型干扰素家族的唯一成员,被认为具有潜在的抗肿瘤活性,曾被尝试用于肿瘤的辅助免疫治疗,但临床研究结果存在明显矛盾——部分研究显示其能抑制肿瘤生长,部分研究则发现其可促进肿瘤进展与转移。当前领域未解决的核心问题是干扰素-γ在肿瘤微环境中的双向作用机制尚未完全阐明,其功能的调控规律不明确,导致临床应用缺乏精准指导。因此,这篇综述系统梳理了干扰素-γ在肿瘤微环境中的作用机制,为解决上述问题提供了全面的研究框架,对推动精准肿瘤免疫治疗具有重要学术价值。
2. 文献综述解析
该综述以干扰素-γ在肿瘤微环境中的双向作用为核心,按“基础生物学-免疫细胞相互作用-抗肿瘤机制-促肿瘤机制-临床意义”的逻辑框架,整合了近60年的相关研究成果,重点解析了干扰素-γ功能的浓度依赖性调控及临床转化价值。
作者对领域内现有研究的分类维度为基础生物学研究、免疫细胞相互作用研究、抗肿瘤作用研究、促肿瘤作用研究及临床转化研究五大类,系统梳理了不同研究方向的关键结论、技术优势与局限性。现有研究的关键结论显示,在抗肿瘤方面,高剂量干扰素-γ可通过激活JAK-STAT1通路诱导肿瘤细胞凋亡,抑制肿瘤血管生成,促进M1型肿瘤相关巨噬细胞极化,增强细胞毒性T淋巴细胞的杀伤活性,还能提升免疫检查点抑制剂的疗效;在促肿瘤方面,低剂量干扰素-γ可诱导肿瘤细胞获得干细胞特性,促进上皮间质转化与转移,通过上调PD-L1、吲哚胺2,3-双加氧酶(IDO)等分子介导免疫逃逸。现有研究的技术优势是涵盖了分子生物学、细胞实验、动物模型及临床样本等多个层面,技术手段包括基因编辑、流式细胞术、免疫组化等,能从多维度解析干扰素-γ的作用机制;局限性在于不同研究中干扰素-γ的给药剂量、肿瘤类型、实验模型存在差异,导致研究结果难以直接对比,且对干扰素-γ浓度依赖的信号通路切换机制解析不够深入,缺乏大规模临床研究验证精准调控干扰素-γ的治疗策略。
这篇综述的创新价值在于首次系统整合了干扰素-γ在肿瘤微环境中的双向作用,明确了浓度、细胞类型及信号通路状态是调控其功能的关键因素,提出了以干扰素-γ响应性为基础的精准免疫治疗思路,弥补了现有研究中缺乏系统性整合的不足,为后续研究提供了清晰的方向。
3. 研究思路总结与详细解析
该综述的研究目标是全面阐明干扰素-γ在肿瘤微环境中的双向作用机制,核心科学问题是解析干扰素-γ功能的调控规律及临床转化潜力,技术路线遵循“基础特征解析-免疫相互作用分析-功能机制阐述-临床意义讨论”的逻辑闭环,通过整合已发表研究成果,系统呈现了干扰素-γ在肿瘤中的复杂作用网络。
3.1 干扰素-γ的基础生物学特征与合成调控
实验目的是明确干扰素-γ的分子结构、合成来源及信号传导通路,为后续功能解析奠定基础。方法细节为作者梳理了已有的分子生物学、细胞实验及动物模型研究,涵盖干扰素-γ的基因结构、蛋白修饰、细胞来源及信号通路激活机制。结果解读显示,干扰素-γ由Th1细胞、自然杀伤(NK)细胞、细胞毒性T淋巴细胞等产生,其蛋白由两条反平行多肽链组成,糖基化修饰可延长其在血液中的半衰期但不影响生物活性;经典信号通路为JAK-STAT通路,干扰素-γ结合受体后激活JAK1/JAK2,进而磷酸化STAT1形成同源二聚体,进入细胞核结合干扰素激活位点(GAS)启动靶基因转录,同时还存在非经典PI3K-Akt-mTOR通路参与信号传导;合成过程受IL-12、IL-18等细胞因子及T-bet等转录因子调控,形成正反馈循环维持其表达。
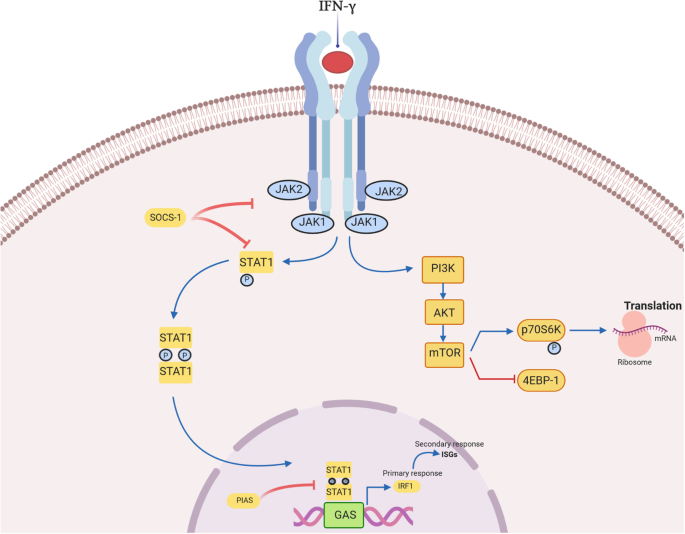
文献未提及具体实验产品,领域常规使用重组干扰素-γ蛋白、流式细胞术检测试剂盒、Western blot抗体、实时荧光定量PCR试剂等。
3.2 干扰素-γ与肿瘤微环境中免疫细胞的相互作用
实验目的是解析干扰素-γ对肿瘤微环境中各类免疫细胞功能的调控作用,明确其免疫调控网络。方法细节为作者总结了巨噬细胞、树突状细胞、T细胞等免疫细胞与干扰素-γ相互作用的已发表研究,涵盖细胞极化、成熟、分化及功能调控等层面。结果解读显示,干扰素-γ可促进巨噬细胞向M1型极化,增强其吞噬及抗肿瘤活性;诱导树突状细胞成熟,上调MHC分子及共刺激分子表达,提升抗原提呈能力;调控CD4+T细胞向Th1方向分化,抑制Th2、Th17及调节性T细胞(Treg)的功能,同时也能诱导部分T细胞凋亡,维持免疫稳态。
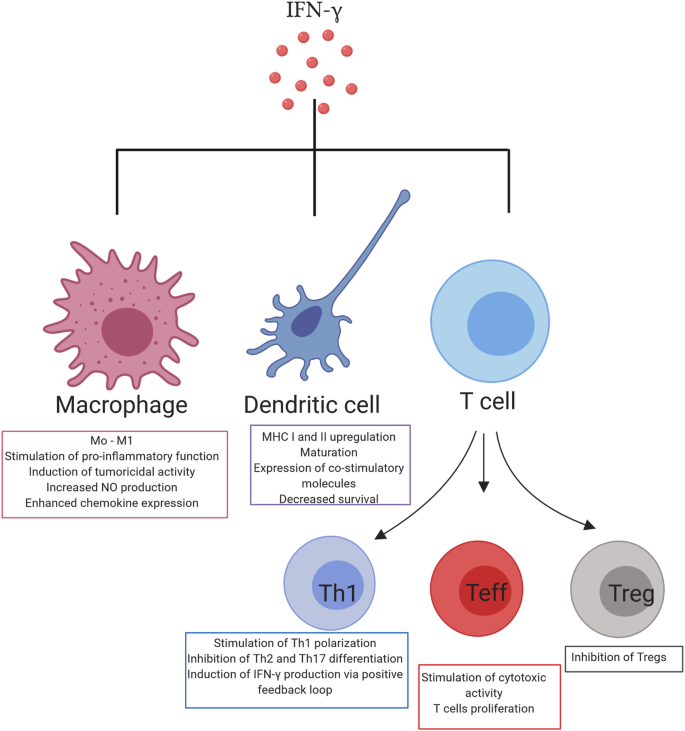
文献未提及具体实验产品,领域常规使用免疫细胞分离试剂盒、细胞因子检测试剂、免疫组化染色试剂盒等。
3.3 干扰素-γ的抗肿瘤作用机制解析
实验目的是系统阐明干扰素-γ抑制肿瘤生长与进展的具体途径,明确其抗肿瘤活性的核心机制。方法细节为作者整合了细胞凋亡、血管生成抑制、免疫激活及免疫治疗增效等多个方向的研究成果,涵盖细胞实验、动物模型及临床样本分析。结果解读显示,高剂量干扰素-γ可通过激活JAK-STAT1-caspase通路诱导肿瘤细胞凋亡,还能通过下调溶质载体家族7成员11(SLC7A11)等分子介导铁死亡;直接破坏肿瘤血管内皮细胞,下调血管内皮生长因子A(VEGF-A)表达,抑制肿瘤血管生成;促进M1型巨噬细胞及细胞毒性T淋巴细胞的抗肿瘤活性,增强肿瘤微环境中的免疫应答;此外,干扰素-γ相关基因signature可预测免疫检查点抑制剂的治疗响应,其浓度升高能提升免疫治疗的疗效。
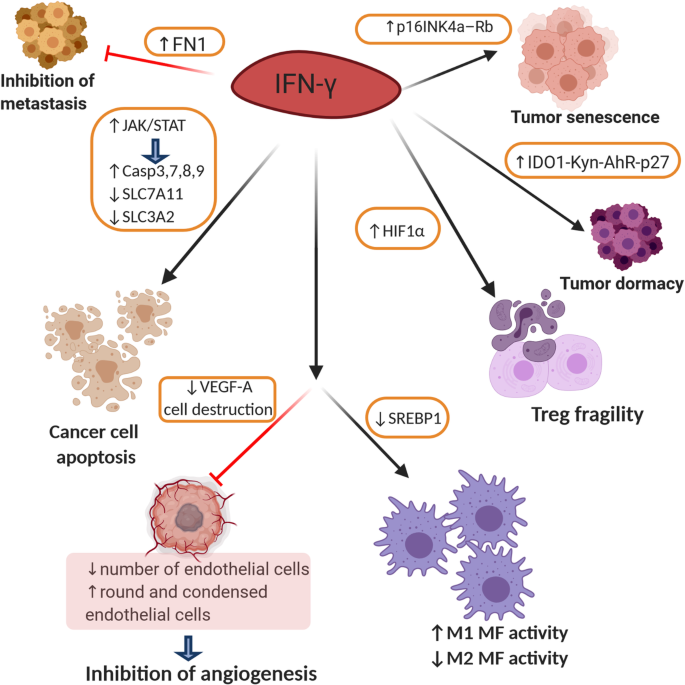
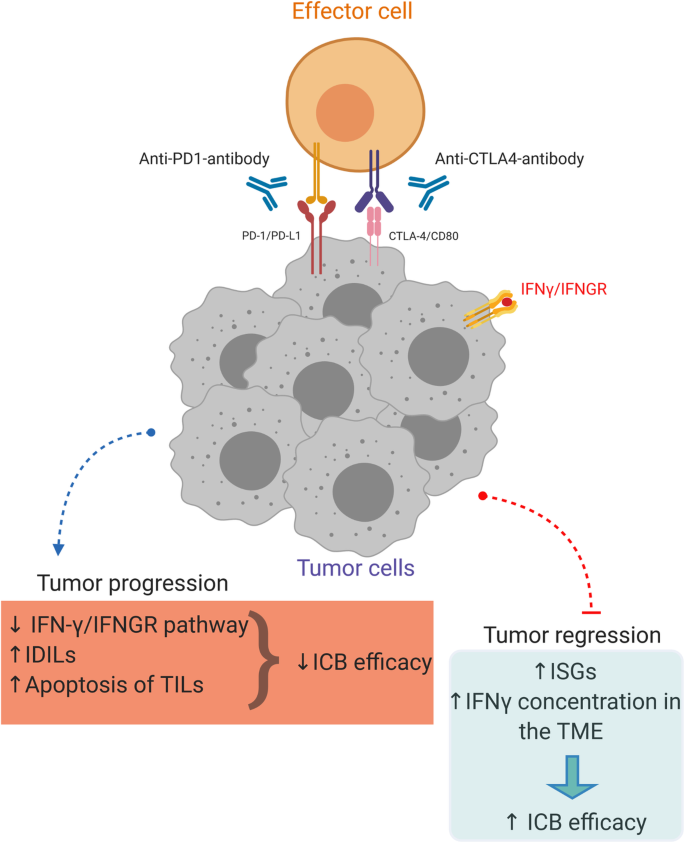
文献未提及具体实验产品,领域常规使用肿瘤细胞系、异种移植动物模型、免疫检查点抑制剂试剂等。
3.4 干扰素-γ的促肿瘤作用机制解析
实验目的是揭示干扰素-γ促进肿瘤进展与转移的潜在机制,明确其促肿瘤活性的调控因素。方法细节为作者梳理了低剂量干扰素-γ的作用、免疫逃逸、肿瘤转移等方向的研究,涵盖细胞实验、动物模型及临床样本分析。结果解读显示,低剂量干扰素-γ可通过激活ICAM1-PI3K-Akt-Notch1通路诱导肿瘤细胞获得干细胞特性,上调CD133等干细胞标志物表达;促进上皮间质转化,上调CXCR4等分子增强肿瘤细胞的迁移与侵袭能力;通过JAK-STAT通路诱导PD-L1、IDO等免疫抑制分子表达,介导免疫细胞凋亡及免疫逃逸;还能促进肿瘤免疫编辑,导致肿瘤细胞产生遗传变异,增强其免疫抵抗能力。
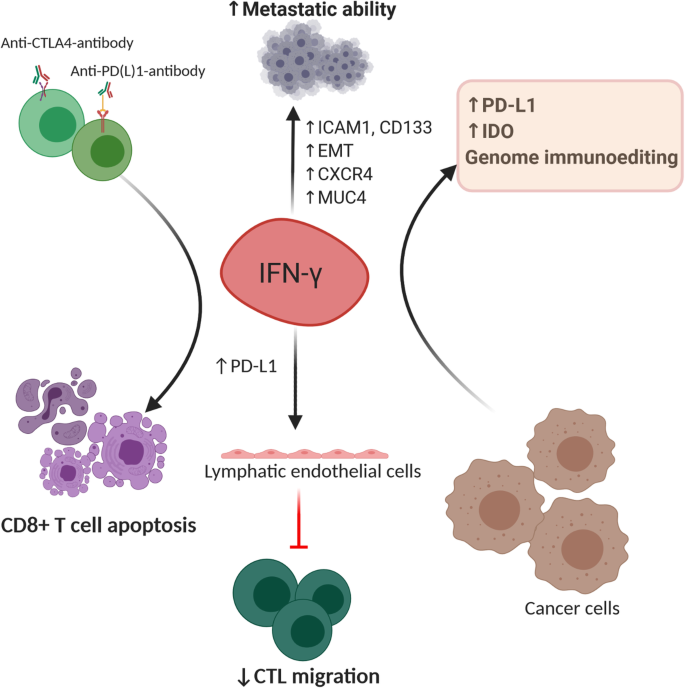
文献未提及具体实验产品,领域常规使用肿瘤转移模型、免疫逃逸检测试剂、基因测序技术等。
4. Biomarker研究及发现成果解析
该综述中涉及的Biomarker主要为干扰素-γ相关基因signature,其作为免疫治疗响应的预测标志物,具有重要的临床转化潜力,为精准肿瘤免疫治疗提供了新的检测指标。
Biomarker定位方面,明确的Biomarker类型为干扰素-γ相关基因表达signature,包括IDO1、CXCL10、CXCL9、HLA-DRA、STAT1、IFNG等基因组成的panel,以及IFNG、CD274、LAG3、CXCL9组成的四基因signature;筛选与验证逻辑为通过对比免疫治疗响应者与非响应者的肿瘤组织基因表达谱,分析干扰素-γ相关基因的表达差异,进而验证其对治疗响应的预测价值,验证过程涵盖转移性黑色素瘤、头颈部鳞癌、胃癌、尿路上皮癌、非小细胞肺癌等多种肿瘤类型。
研究过程详述显示,Biomarker的来源为肿瘤组织样本,验证方法包括基因表达谱芯片、实时荧光定量PCR、免疫组化等;特异性与敏感性数据方面,Ayers等的研究显示,该signature在转移性黑色素瘤、头颈部鳞癌、胃癌患者中可有效区分抗PD-1治疗的响应者与非响应者(文献未明确具体AUC、敏感性及特异性数值,基于研究结论推测),四基因signature在尿路上皮癌和非小细胞肺癌患者中对durvalumab治疗响应的预测准确性较高(文献未明确具体统计学数据)。
核心成果提炼显示,该Biomarker的功能关联为作为免疫检查点抑制剂治疗响应的预测指标,可用于筛选适合免疫治疗的患者,提升治疗的精准性;创新性在于首次系统提出干扰素-γ相关基因signature可作为免疫治疗的预测标志物,明确了干扰素-γ信号通路状态与免疫治疗疗效的关联;统计学结果方面,部分研究显示响应者与非响应者的基因表达水平存在显著差异(P<0.05,样本量因肿瘤类型而异),但具体风险比(HR)、置信区间等数据文献未明确提供。
