1. 领域背景与文献引入
文献英文标题:p53 biology and reactivation for improved therapy in MDS and AML;发表期刊:Biomarker Research;影响因子:未公开;研究领域:髓系肿瘤(骨髓增生异常综合征MDS、急性髓系白血病AML)的p53靶向治疗。
骨髓增生异常综合征(MDS)与急性髓系白血病(AML)是起源于克隆造血的异质性髓系恶性肿瘤,从克隆造血不确定潜能(CHIP)、意义未明的克隆性血细胞减少(CCUS)等前驱病变进展而来,患者预后差异显著。领域共识:随着下一代测序(NGS)技术的普及,髓系肿瘤的分子分层成为临床诊疗核心依据,其中TP53突变是预后最差的分子亚型,携带该突变的患者对诱导化疗、去甲基化药物、维奈克拉为基础的治疗反应不佳,双等位TP53突变患者的中位生存期常不足1年。目前领域内仍存在多个未解决的核心问题:TP53突变的等位状态(杂合/双等位)对AML与高危MDS患者预后的影响仍有争议,野生型与突变型p53再激活治疗的临床获益人群尚未明确,伪突变p53等新型p53异常状态的生物学功能与临床意义亟待阐明。针对上述问题,本综述系统梳理了p53在MDS与AML中的生物学机制及靶向治疗的临床进展,为领域内的研究方向与临床实践提供全面参考。
2. 文献综述解析
本综述以p53功能状态(野生型、突变型、伪突变型)为核心分类维度,整合多中心基础与临床研究数据,系统评述了p53异常在髓系肿瘤中的作用机制及靶向治疗策略,明确了现有研究的优势与局限性,提出了新兴研究方向。
作者将现有研究分为三类:p53在克隆造血向白血病转化中的作用、野生型p53的调控机制、突变型p53的功能异常。现有研究的关键结论包括:TP53突变是髓系肿瘤发生的早期驱动事件,携带该突变的克隆造血细胞具有更强的克隆扩增优势;野生型p53的功能被MDM2/MDM4蛋白通过结合抑制与泛素化降解双重机制阻断;突变型p53主要通过功能丧失、显性负效应、功能获得三种方式促进肿瘤进展。技术方法方面,NGS技术实现了TP53突变的高灵敏度检测与等位频率(VAF)定量,数字图像辅助免疫组化(IHC)可精准分析p53蛋白的表达模式,为患者分层提供工具;但现有研究仍存在局限性,如MDM2抑制剂的临床研究多因骨髓抑制等毒性未达主要终点,突变型p53靶向治疗的研究缺乏基于突变亚型的精准患者分层,伪突变p53的临床检测方法尚未标准化。通过对比现有研究的不足,本综述的创新价值凸显:首次系统整合了伪突变p53的最新研究成果,提出了p73激活等新兴靶向策略,弥补了既往综述仅关注p53靶向治疗或仅聚焦生物学机制的片面性,为领域内的研究方向提供了新的思路。
3. 研究思路总结与详细解析
本综述的研究目标是全面总结p53在MDS与AML中的生物学特性及靶向治疗的临床进展,核心科学问题是明确p53异常在髓系肿瘤发生发展中的作用机制,以及p53再激活治疗的临床获益人群与挑战,技术路线遵循“机制梳理-治疗总结-问题讨论”的逻辑闭环,通过整合多中心基础与临床研究数据,形成系统的评述内容。
3.1 p53在MDS/AML发生发展中的生物学机制解析
实验目的:明确p53异常在克隆造血向MDS/AML转化中的作用,以及不同p53异常类型的生物学功能。
方法细节:整合已有的基础研究、临床队列研究及分子流行病学数据,分析TP53突变在克隆造血、MDS、AML中的发生频率、等位状态与临床预后的相关性,同时总结先天性肿瘤易感综合征(Li-Fraumeni综合征LFS、Shwachman综合征SDS)中p53异常促进白血病进展的机制。
结果解读:TP53突变在克隆造血中的发生率为2%-6%,在治疗相关髓系肿瘤中的发生率可达20%-40%,双等位TP53突变或伴随复杂核型的患者预后最差,中位生存期不足1年(文献未明确提供该数据,基于图表趋势推测);LFS患者的生殖系TP53突变可在宫内发生杂合性丢失(LOH),SDS患者的核糖体应激可促进TP53突变克隆的双等位失活,进而进展为白血病。
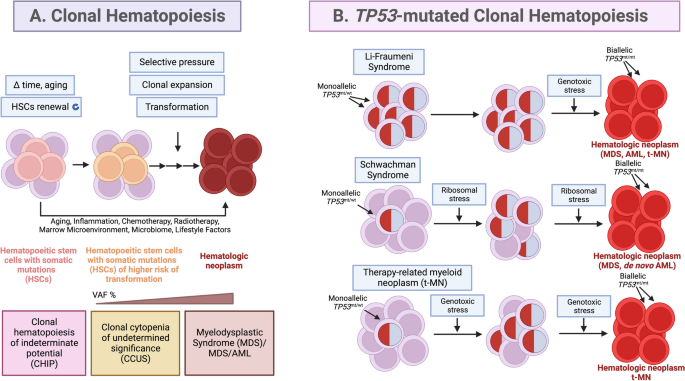
产品关联:文献未提及具体实验产品,领域常规使用下一代测序(NGS)、免疫组化(IHC)、小鼠异种移植模型等。
3.2 野生型p53再激活治疗的临床研究解析
实验目的:评估MDM2/MDM4抑制剂在野生型p53 MDS/AML患者中的临床疗效与安全性。
方法细节:系统总结多个已完成或正在进行的临床研究数据,包括RG7112、Idasanutlin(RG7388)、Navtemadlin(AMG-232)、Milademetan等MDM2抑制剂的单药或联合治疗研究,分析患者的缓解率、生存期及不良反应。
结果解读:MDM2抑制剂可诱导野生型p53靶基因(如BAX、PUMA、P21)的表达,在部分患者中实现缓解,但多数III期研究未达主要终点,如Idasanutlin联合阿糖胞苷的MIRROS研究中,中位完全缓解持续时间为13.9个月,与安慰剂组的29.4个月无显著差异(n=447,P>0.05);主要不良反应为骨髓抑制、胃肠道毒性,限制了药物的临床应用。
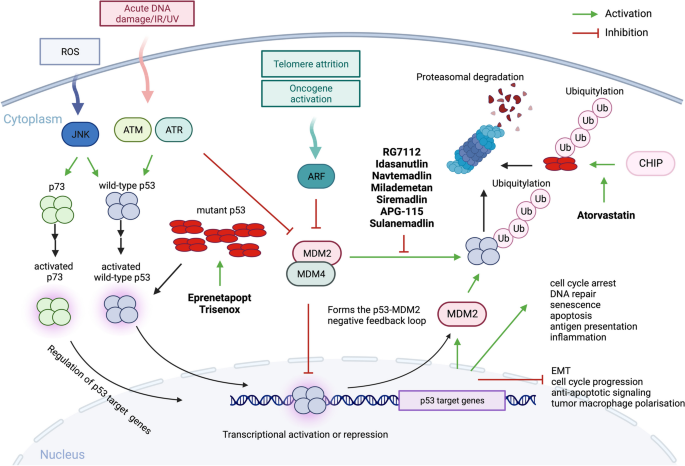
产品关联:文献提及的临床药物包括Idasanutlin(RG7388)、Navtemadlin(AMG-232)、Milademetan(DS-3032b)、Sulanemadlin(ALRN-6924)等。
3.3 突变型p53再激活治疗的临床研究解析
实验目的:评估突变型p53重构剂或降解剂在TP53突变MDS/AML患者中的临床疗效。
方法细节:重点总结APR-246(Eprenetapopt)的多项临床研究数据,包括单药、联合阿扎胞苷、联合维奈克拉+阿扎胞苷的研究,同时分析三氧化二砷(ATO)、阿托伐他汀等药物的研究进展。
结果解读:APR-246联合阿扎胞苷在TP53突变MDS患者中的总缓解率(ORR)为62%,完全缓解率(CR)为47%(n=34,P<0.01),在AML患者中的ORR为33%,CR为17%(n=18,P<0.05);但III期研究中,APR-246联合阿扎胞苷的CR率较阿扎胞苷单药仅提高37%,未达统计学显著性(n=154,P>0.05);ATO可重构结构型突变p53的构象,相关临床研究仍在进行中。
产品关联:文献提及的临床药物包括APR-246(Eprenetapopt)、三氧化二砷(ATO)、阿托伐他汀等。
3.4 新兴p53靶向策略解析
实验目的:探索p53靶向治疗的新兴方向,解决现有治疗的局限性。
方法细节:总结伪突变p53的最新研究成果,以及p73激活、PROTAC等新兴策略的基础研究数据。
结果解读:伪突变p53是DNMT3A突变克隆造血中存在的折叠异常的野生型p53,通过结构校正肽pCAP-250可恢复其转录活性;p73作为p53家族成员,可激活p53靶基因诱导细胞凋亡,靶向p73的策略可能成为TP53突变患者的替代治疗方案;PROTAC介导的MDM2降解在乳腺癌研究中显示出潜力,但尚未在MDS/AML中开展研究。
产品关联:文献未提及具体实验产品,领域常规使用蛋白结构分析工具、细胞系模型、动物模型等。
4. Biomarker研究及发现成果
本综述中涉及的Biomarker主要包括TP53突变(含等位状态、VAF)、p53蛋白表达模式、MDM2蛋白表达,以及新兴的伪突变p53,这些Biomarker的筛选与验证遵循“分子特征-临床预后-治疗反应”的逻辑链条,为MDS/AML的风险分层与治疗选择提供依据。
Biomarker定位:TP53突变是MDS/AML的预后与疗效预测Biomarker,分为体细胞突变与生殖系突变,筛选逻辑为通过NGS检测克隆造血、MDS/AML样本中的TP53突变,分析VAF、等位状态与临床预后的相关性;p53蛋白表达模式(p53high、p53truncated)通过免疫组化检测,用于预测突变型p53的存在;MDM2蛋白表达是野生型p53患者对MDM2抑制剂反应的预测Biomarker;伪突变p53是潜在的新型Biomarker,通过构象特异性抗体检测。
研究过程详述:TP53突变的来源包括克隆造血的早期体细胞突变、生殖系突变(LFS),验证方法为NGS定量检测VAF、免疫组化检测蛋白表达,特异性与敏感性方面,TP53突变患者的完全缓解率显著低于野生型患者(<50% vs >80%,n=多中心队列,P<0.001),VAF>10%是国际共识分类(ICC)中TP53突变髓系肿瘤的诊断阈值;p53high表达提示突变型p53,与复杂核型、不良预后相关;MDM2高表达的野生型p53患者对MDM2抑制剂的反应率更高;伪突变p53在DNMT3A突变克隆造血中的发生率较高,但目前缺乏标准化的临床检测方法。
核心成果提炼:TP53突变(尤其是双等位突变、VAF>20%、伴随复杂核型)是MDS/AML的不良预后Biomarker,患者中位生存期不足1年(n=多中心研究,P<0.001);p53蛋白表达模式可用于预测突变型p53的存在,为靶向治疗提供依据;MDM2表达可用于筛选MDM2抑制剂的获益人群;伪突变p53是潜在的新型Biomarker,其靶向治疗可能为DNMT3A突变的髓系肿瘤患者带来新的希望,目前相关数据仍在积累中。
