1. 领域背景与文献引入
文献英文标题:p63 expression in human tumors and normal tissues: a tissue microarray study on 10,200 tumors;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤生物标志物与临床病理诊断
p53家族转录因子是肿瘤分子生物学研究的核心靶点之一,其中p63作为调控上皮组织分化的关键因子,在鳞状上皮、尿路上皮等正常组织的发育与维持中发挥重要作用。领域共识:p63免疫组化已成为肿瘤病理分类的常用工具,尤其用于区分鳞状细胞癌与腺癌、尿路上皮癌与肾细胞癌等。然而,现有研究中关于p63在肿瘤中表达的数据存在显著冲突,不同研究报道的阳性率差异极大,例如小细胞肺癌中p63阳性率范围为0-77%,尿路上皮癌中为0-100%,这一现象主要由不同研究使用的抗体、免疫组化实验流程及阳性判读标准不统一导致。当前领域的核心空白在于缺乏大规模、标准化条件下的p63表达谱分析,无法为临床诊断提供可靠的参考依据。因此,本研究通过构建包含超万例样本的组织芯片,在统一实验条件下系统分析p63在正常与肿瘤组织中的表达,旨在明确其表达规律及临床价值,为肿瘤病理诊断提供标准化参考。
2. 文献综述解析
作者对领域内现有研究的评述逻辑主要围绕“实验条件异质性导致结果冲突”展开,将现有研究按抗体类型、实验流程、样本量三个维度进行分类总结。
现有研究的关键结论集中于p63在鳞状上皮来源肿瘤中具有较高表达率,可作为该类肿瘤的辅助诊断标志物;部分研究指出p63表达与肿瘤预后相关,如食管鳞状细胞癌中低表达提示不良预后。技术方法优势方面,早期小样本研究初步探索了p63在不同肿瘤中的表达特征,为后续研究提供了方向;但局限性也十分明显,多数研究样本量较小,且缺乏标准化的实验流程与判读标准,导致不同研究结果无法直接比较,甚至出现完全相反的结论,例如部分研究报道子宫内膜癌中p63阳性率较高,而另一些研究则未检测到阳性表达。
通过对比现有研究的“未解决问题”,本研究的创新点在于首次采用包含12620例肿瘤样本(115种肿瘤类型)与76种正常组织的大规模组织芯片,在高度标准化的免疫组化实验条件下进行检测,有效避免了实验异质性带来的结果偏差。同时,本研究系统分析了p63表达与肿瘤起源、临床病理参数及预后的关系,填补了领域内缺乏大规模标准化p63表达谱的空白,为p63的临床应用提供了可靠的依据。
3. 研究思路总结与详细解析
本研究的整体目标是全面绘制p63在人类正常组织与肿瘤组织中的表达谱,明确其表达与肿瘤起源、表型及预后的关联;核心科学问题是解决现有研究中p63表达数据的冲突,明确其作为诊断与预后生物标志物的价值;技术路线遵循“样本构建→标准化检测→结果分析→临床关联”的闭环逻辑,确保研究结果的可靠性与可重复性。
3.1 组织芯片构建与样本收集
实验目的:构建包含多种正常组织与肿瘤类型的组织芯片,为大规模分析p63表达提供样本基础。方法细节:收集来自三家德国医院病理存档的组织样本,其中正常组织芯片包含76种组织类型,每种类型8例样本(共608例);肿瘤组织芯片包含115种肿瘤类型与亚型,共12620例原发性肿瘤样本。所有样本经4%甲醛固定、石蜡包埋后,选取肿瘤细胞占比≥70%的组织块制作组织芯片,每个样本取0.6mm直径的组织点。结果解读:最终10200例肿瘤样本(80.8%)可进行有效评估,非可评估样本均匀分布于各肿瘤类型,无统计学偏倚;正常组织样本均完成有效检测,明确了p63在正常组织中的表达分布。产品关联:文献未提及具体实验产品,领域常规使用组织芯片制作仪、石蜡包埋机、切片机等设备。
3.2 标准化免疫组化检测
实验目的:在统一条件下检测p63在所有样本中的表达水平,避免实验异质性影响结果。方法细节:所有组织芯片切片在同一天进行免疫组化实验,经脱蜡、热诱导抗原修复(121℃,pH7.8缓冲液5分钟)后,加入p63特异性抗体(克隆号7B4,稀释比1:100),37℃孵育60分钟,随后使用EnVision Kit进行显色。结果解读:成功完成所有可评估样本的p63免疫组化检测,明确了p63在不同组织中的表达强度与阳性细胞比例。产品关联:实验所用关键产品:p63单克隆抗体(克隆号7B4)、Agilent的EnVision显色试剂盒。
3.3 结果判读与统计分析
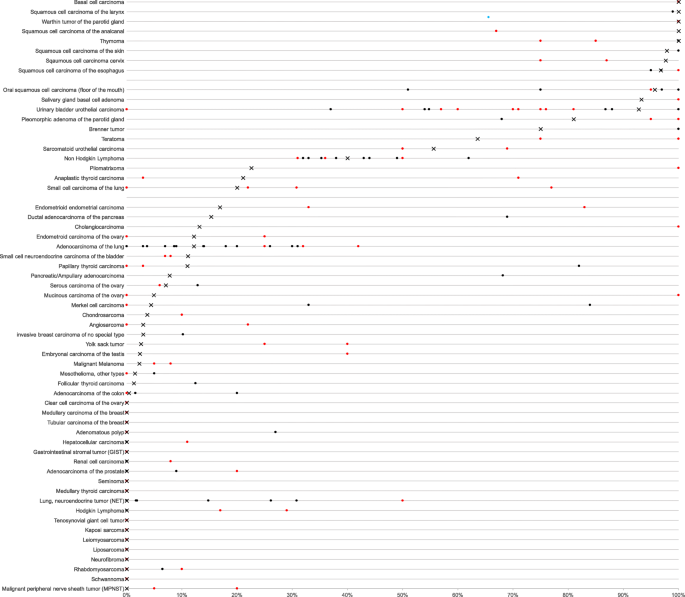
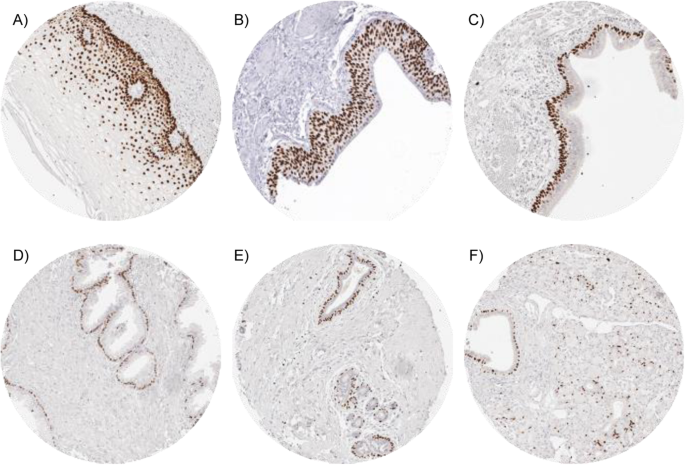
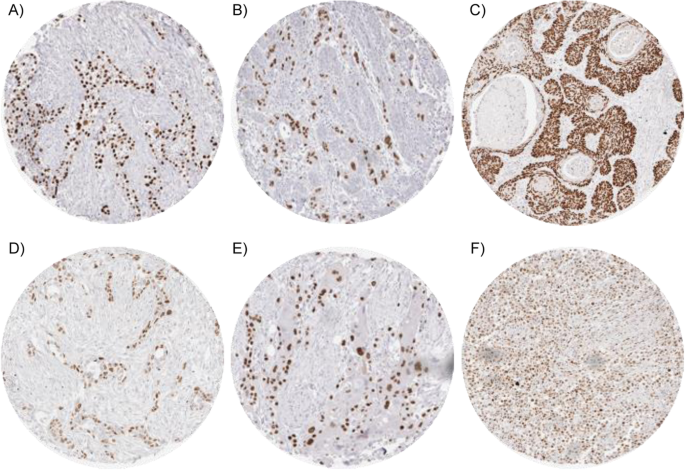
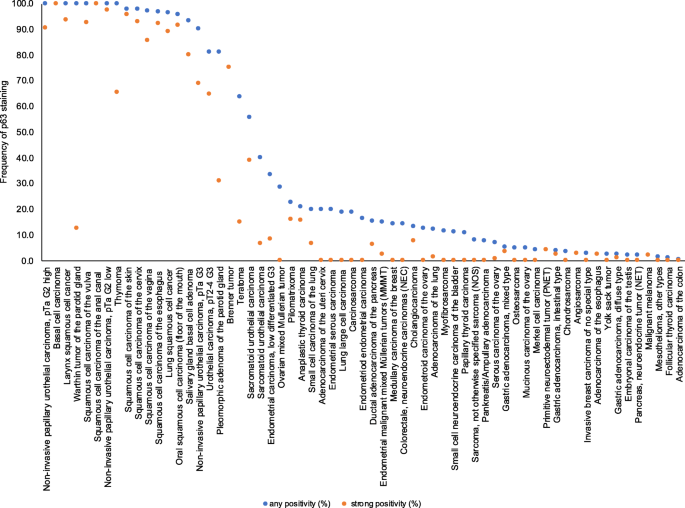
实验目的:系统量化p63表达水平,分析其在不同组织类型中的表达规律。方法细节:对肿瘤样本的p63表达进行半定量判读,评估阳性细胞核比例与染色强度(0、1+、2+、3+),并将结果分为阴性、弱阳性、中度阳性、强阳性四个等级;使用JMP 14软件进行统计分析,通过卡方检验分析p63表达与肿瘤表型的关联,Kaplan-Meier法绘制生存曲线,Log-Rank检验分析预后差异。结果解读:p63在正常组织中主要表达于鳞状上皮、尿路上皮、胸腺上皮、肌上皮细胞等;在肿瘤组织中,61种(53%)肿瘤类型可检测到p63表达,其中鳞状细胞癌(96-100%)、胸腺肿瘤(100%)、尿路上皮癌(81-100%)等阳性率最高。
3.4 临床病理参数关联分析
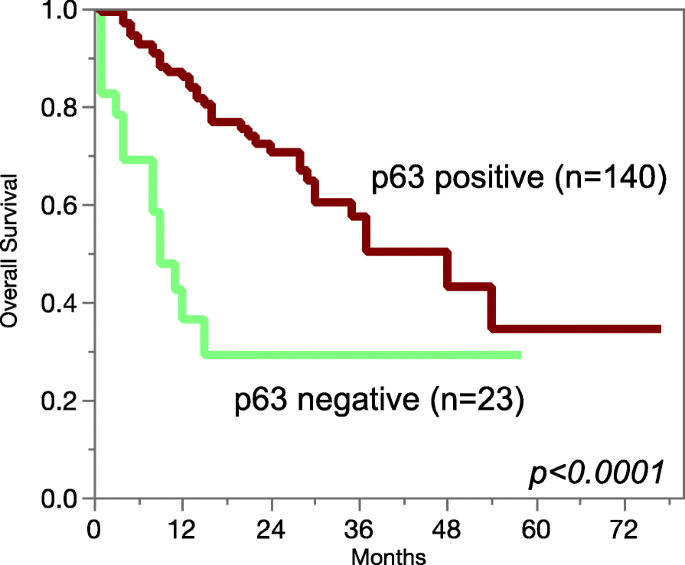
实验目的:明确p63表达与肿瘤表型、预后的关联,探索其临床价值。方法细节:对具有临床病理数据的肿瘤样本(胃癌、胰腺癌、卵巢癌、子宫内膜癌、尿路上皮癌)进行分析,其中尿路上皮癌患者具有随访数据(中位随访14个月)。结果解读:在422例胰腺癌、160例子宫内膜癌、374例卵巢癌中,p63表达与疾病侵袭性参数无关联;在355例胃癌中,4%的样本p63阳性,且与淋巴结转移相关(p=0.0208);在尿路上皮癌中,p63表达缺失或降低与晚期分期、高分级显著相关(p<0.0001),且与不良生存相关(p<0.0001)。
4. Biomarker研究及发现成果
本研究将p63定位为肿瘤诊断与预后生物标志物,通过大规模标准化分析明确了其表达谱与临床关联,为其临床应用提供了可靠依据。
Biomarker定位:p63作为肿瘤诊断与预后生物标志物,筛选逻辑为“正常组织表达谱分析→肿瘤组织表达谱分析→临床病理参数关联”,验证逻辑为通过大规模组织芯片的标准化检测,结合临床数据明确其诊断特异性与预后价值。
研究过程详述:Biomarker来源为人类正常组织与肿瘤组织的石蜡包埋样本;验证方法为免疫组化检测,半定量评估表达水平;特异性方面,p63阳性肿瘤多起源于p63阳性的正常组织,如鳞状上皮来源肿瘤阳性率达96-100%,而起源于p63阴性正常组织的肿瘤多为阴性;敏感性方面,在尿路上皮癌中,p63表达缺失可有效提示晚期病变(敏感性未明确提供,基于图表趋势推测);在355例胃癌中,p63阳性样本的淋巴结转移率更高(p=0.0208,n=355);在254例尿路上皮癌中,p63缺失与不良生存相关(p<0.0001,n=254)。
核心成果提炼:p63作为诊断生物标志物,可有效区分鳞状上皮、尿路上皮等来源的肿瘤与其他类型肿瘤,尤其在不明原发灶转移瘤的诊断中具有价值;作为预后生物标志物,尿路上皮癌中p63表达缺失提示不良预后(风险比未明确提供,基于生存曲线推测HR>2);创新性在于首次通过大规模标准化研究明确了p63在115种肿瘤中的表达谱,解决了现有研究的结果冲突,为其临床应用提供了统一的参考依据。
