1. 领域背景与文献引入
文献英文标题:Kinomic profiling of glioblastoma cells reveals PLCG1 as a target in restricted glucose;发表期刊:Biomarker Research;影响因子:未公开;研究领域:神经肿瘤学(胶质母细胞瘤)
胶质母细胞瘤(GBM)是成人最常见的原发性恶性脑胶质瘤,约占所有原发性恶性脑肿瘤诊断的50%,其治疗一直是神经肿瘤领域的难点。2005年Stupp等提出的手术切除联合同步放化疗及辅助化疗方案,将患者平均生存期延长至14.6个月,2年生存率提升至17%,成为领域标准治疗方案,但患者总体预后仍极差。随着研究深入,肿瘤微环境(如低氧、低营养、低pH值)对GBM细胞信号调控及治疗耐药的作用逐渐受到关注,其中Warburg效应揭示的肿瘤代谢重编程机制,为靶向肿瘤代谢通路提供了理论基础。当前领域研究热点聚焦于肿瘤微环境对激酶信号通路的调控、精准治疗靶点筛选,以及优化体外模型以提高药物研发的临床转化效率,但仍存在核心未解决问题:传统体外培养采用的高葡萄糖条件与体内肿瘤微环境的营养限制状态差异显著,导致体外筛选的药物在临床试验中失败率极高;GBM细胞在低葡萄糖微环境下的激酶活性变化及潜在靶向通路尚不明确。针对这一研究空白,本研究通过激酶组学技术分析低葡萄糖条件下GBM细胞的激酶活性差异,筛选可靶向的关键通路,为优化体外药物筛选模型及开发GBM精准治疗策略提供实验依据。
2. 文献综述解析
作者围绕胶质母细胞瘤治疗困境与肿瘤微环境的调控作用,从治疗现状、激酶组学技术应用、磷脂酶Cγ1(PLCG1)的功能三个维度对领域研究进行系统性评述,明确现有研究的分类逻辑与核心结论。
现有研究的关键结论包括:GBM的不良预后与肿瘤异质性及微环境的多重调控密切相关;激酶组学技术可直接测量激酶的活性状态,避免了基因组等分子替代物的局限性,已被用于肿瘤患者的分层与靶点筛选;PLCG1作为表皮生长因子受体(EGFR)等受体酪氨酸激酶的下游效应分子,参与调控肿瘤细胞增殖信号,是潜在的肿瘤治疗靶点。技术方法优势方面,患者来源异种移植(PDX)模型可最大程度 recapitulate亲本肿瘤的特征,相比长期传代细胞系更具临床相关性;高通量激酶组学平台(如PamStation12)可同时分析上百种激酶底物的磷酸化状态,实现高效靶点筛选。但现有研究仍存在局限性:传统体外培养的高葡萄糖条件无法模拟体内肿瘤微环境的营养限制状态,导致药物筛选结果的临床转化效率低下;EGFR抑制剂等酪氨酸激酶抑制剂因肿瘤细胞的耐药性,在GBM治疗中未取得显著突破。
本研究的创新价值在于,首次在模拟体内生理状态的低葡萄糖条件下,对GBM PDX细胞进行激酶组学分析,发现PLCG1在低葡萄糖条件下的磷酸化水平显著升高,且PLC抑制剂在低葡萄糖环境下对GBM细胞的生长抑制效果远高于高葡萄糖条件,弥补了现有研究未考虑微环境对激酶信号通路影响的不足,为优化体外药物筛选模型、提高GBM治疗靶点的精准性提供了新的实验依据。
3. 研究思路总结与详细解析
本研究以“低葡萄糖微环境对GBM激酶组的调控及潜在治疗靶点筛选”为核心科学问题,采用“细胞模型构建→高通量激酶组分析→差异靶点验证”的闭环技术路线,通过PDX细胞模型模拟体内肿瘤微环境,结合激酶组学与抑制剂功能实验,明确了PLCG1作为低葡萄糖条件下GBM的潜在治疗靶点。
3.1 模拟肿瘤微环境的细胞模型构建
实验目的是建立符合体内肿瘤营养限制状态的细胞培养体系,为后续激酶组分析提供可靠模型。方法细节:选取两株GBM患者来源异种移植(PDX)细胞GBM14和GBM456,分别在标准高葡萄糖(25 mM)和低葡萄糖(2.5 mM)培养基中培养至少3天,培养基采用无血清但含表皮生长因子(EGF)、成纤维细胞生长因子(FGF)和B27的配方,以维持PDX细胞的肿瘤干细胞特征;同时培养正常人星形胶质细胞(NHA)作为正常细胞对照。结果解读:PDX细胞在该培养条件下可最佳模拟亲本肿瘤的生物学特征,低葡萄糖培养基则精准还原了体内肿瘤微环境的营养限制状态,为后续激酶活性分析提供了生理相关的实验模型。实验所用关键产品:Lonza的正常人星形胶质细胞(NHA)、Selleck Chemicals的PLC抑制剂U73122和Raf抑制剂AZ628、Promega的Cell Titer Glo 2.0试剂。
3.2 高通量激酶组分析与差异靶点筛选
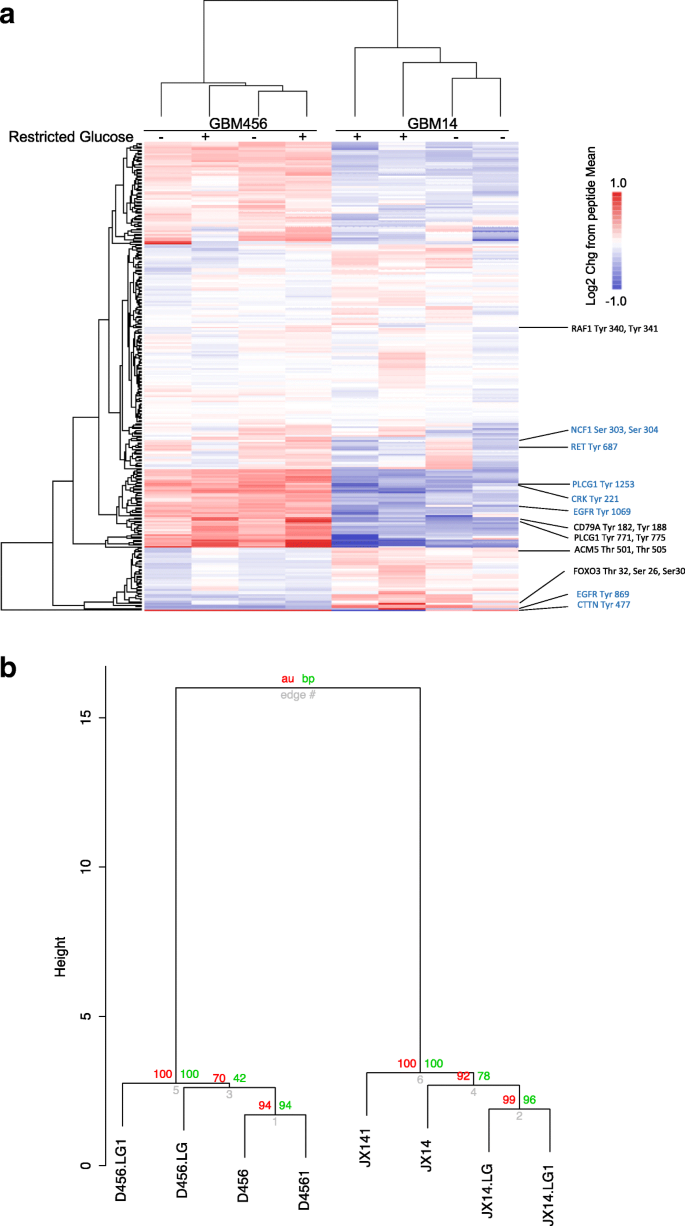
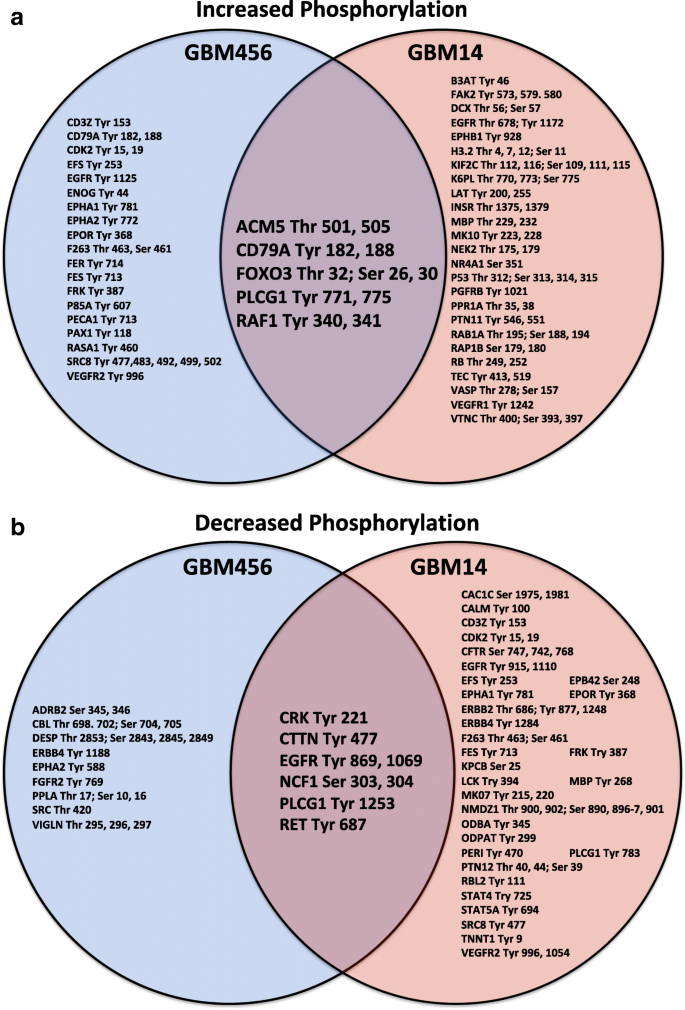
实验目的是检测高/低葡萄糖条件下GBM细胞的激酶活性差异,筛选受微环境调控的关键激酶靶点。方法细节:采用PamStation12平台,对细胞裂解液进行144种酪氨酸和144种丝氨酸/苏氨酸激酶底物肽段的磷酸化水平分析;通过无监督层次聚类分析样本间的激酶组特征差异,结合Venn图筛选两株PDX细胞中共同差异磷酸化的肽段;使用pvclust算法评估聚类结果的统计学强度。结果解读:无监督聚类显示,细胞系来源的激酶组特征差异大于葡萄糖条件的影响,但两株PDX细胞在低葡萄糖条件下均出现PLCG1(Tyr771/775)和Raf-1的底物肽段磷酸化水平显著升高,其中PLCG1肽段的Log2变化值均大于0.5,为最显著的共同差异靶点。
3.3 激酶抑制剂的功能验证
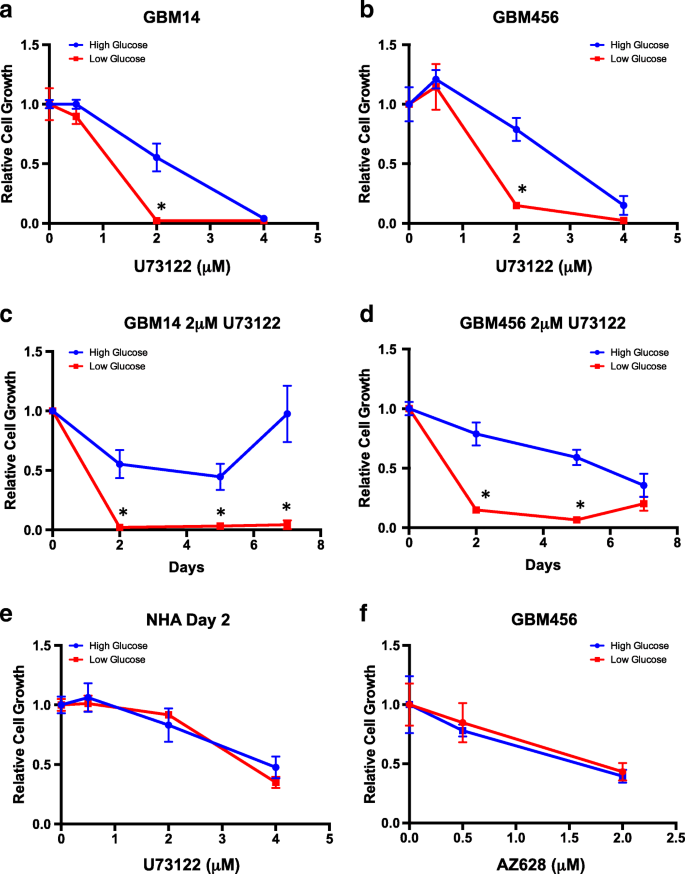
实验目的是验证PLCG1和Raf-1作为低葡萄糖条件下GBM治疗靶点的有效性与特异性。方法细节:在高/低葡萄糖培养的GBM PDX细胞和NHA细胞中,分别加入不同浓度的PLC抑制剂U73122(0.5、2、4 μM)和Raf抑制剂AZ628(0.5、2 μM),培养后使用Cell Titer Glo 2.0试剂检测细胞增殖活性;采用学生t检验分析不同葡萄糖条件下抑制剂效果的统计学差异,实验重复至少3次。结果解读:2 μM的U73122在低葡萄糖条件下对GBM细胞的生长抑制作用显著强于高葡萄糖条件(n=3,P<0.05),而在NHA细胞中未观察到该差异;Raf抑制剂AZ628在两种葡萄糖条件下均显著抑制GBM细胞生长,且效果无明显统计学差异,提示PLCG1的调控作用具有微环境依赖性。
4. Biomarker研究及发现成果
本研究聚焦低葡萄糖微环境下GBM的激酶靶点筛选,将PLCG1定位为GBM适应营养限制微环境的关键功能Biomarker,筛选与验证逻辑为“高通量激酶组筛选→两株PDX细胞交叉验证→抑制剂功能实验验证”,形成完整的证据链。
PLCG1作为Biomarker的来源为GBM PDX细胞的激酶组学分析,验证方法包括高通量底物肽段磷酸化检测与细胞水平的抑制剂功能实验。特异性方面,PLCG1的磷酸化水平升高仅在低葡萄糖条件下的GBM细胞中出现,在正常人星形胶质细胞中无此响应,提示其具有肿瘤细胞与微环境双重特异性;敏感性方面,2 μM的PLC抑制剂U73122在低葡萄糖条件下即可显著抑制GBM细胞生长(n=3,P<0.05),而在高葡萄糖条件下抑制率不足50%,显示出良好的靶点敏感性。
核心成果提炼:PLCG1是GBM细胞适应低葡萄糖微环境的关键激酶靶点,其磷酸化水平升高为GBM细胞在营养限制条件下维持增殖的重要调控机制;PLC抑制剂在低葡萄糖条件下对GBM的生长抑制效果显著增强,提示模拟体内微环境的体外模型可大幅提高药物筛选的精准性;本研究首次揭示了PLCG1作为GBM在营养限制微环境中的潜在治疗靶点,为GBM的精准治疗提供了新方向,同时为优化体外药物筛选模型、提高临床转化效率提供了实验依据。
