1. 领域背景与文献引入
文献英文标题:Single-cell analysis reveals alternations between the aged and young mice prostates;发表期刊:Biomarker Research;影响因子:未公开;研究领域:前列腺衰老与单细胞转录组学
领域共识:衰老是影响所有细胞、组织和器官的普遍过程,男性前列腺通常从40岁左右开始出现增生,进而压迫尿道导致排尿功能障碍,同时显著提升前列腺癌的发病风险。目前前列腺衰老的分子机制尚未完全阐明,成为制约良性前列腺增生、前列腺癌等衰老相关疾病诊疗技术发展的核心瓶颈。单细胞RNA测序技术已成为解析细胞异质性与衰老相关分子变化的重要工具,此前针对前列腺的单细胞研究多聚焦于细胞谱系鉴定或肿瘤微环境分析,但缺乏对前列腺衰老过程中不同细胞类型特异性变化的系统解析。
本研究针对上述研究空白,以年轻(2月龄)和老年(24月龄)C57BL/6J小鼠为模型,通过单细胞RNA测序技术系统对比不同年龄段小鼠前列腺的细胞组成、基因表达及通路变化,旨在揭示前列腺衰老的细胞与分子机制,为衰老相关前列腺疾病的生物标志物筛选与治疗靶点开发提供理论基础。
2. 文献综述解析
作者在综述部分按“前列腺衰老的临床意义→现有研究进展→技术应用局限”的逻辑梳理领域现状:首先明确前列腺增生与癌变的衰老相关性,指出其对老年男性健康的严重影响;随后总结单细胞测序技术在衰老研究中的应用,包括在脑、乳腺等器官的细胞异质性解析成果;最后聚焦前列腺领域,提出现有研究的局限性:缺乏对衰老过程中9种主要前列腺细胞类型的系统差异分析,基底细胞向间质细胞的上皮-间质转化(EMT)在前列腺衰老中的作用未被揭示,免疫细胞的衰老特异性炎症反应机制尚不明确。
现有研究已证实前列腺增生与细胞增殖、氧化应激相关,单细胞测序技术可精准鉴定前列腺上皮细胞亚群,但多数研究未区分年龄因素对细胞组成的影响,且未深入解析细胞间通讯与发育轨迹在衰老中的变化。本研究的创新价值在于:首次系统解析小鼠前列腺9种主要细胞类型的衰老差异基因表达谱,明确基底细胞向间质细胞的EMT转化是前列腺衰老的关键过程,揭示老年小鼠免疫细胞的特异性炎症反应增强,同时发现细胞类型特异性的氧化应激、衰老相关分泌表型(SASP)变化,填补了前列腺衰老单细胞转录组研究的空白。
3. 研究思路总结与详细解析
本研究整体框架为:以年轻与老年小鼠前列腺不同叶组织为样本,通过单细胞RNA测序获取转录组数据,经细胞分群、差异基因分析、功能富集、细胞通讯与拟时序分析解析衰老相关细胞与分子变化,最终结合免疫荧光、蛋白免疫印迹实验验证核心机制。研究逻辑遵循“样本制备→组学检测→生物信息学分析→实验验证”的闭环,核心科学问题是解析前列腺衰老过程中细胞异质性变化的分子机制及关键细胞间相互作用。
3.1 实验样本制备与单细胞测序
实验目的:获取年轻与老年小鼠前列腺的高质量单细胞转录组数据,为细胞异质性解析提供基础。
方法细节:选取2月龄(年轻组)和24月龄(老年组)C57BL/6J雄性小鼠各2只,分离前列腺前叶(AP)与腹/背/侧叶(VDLP)组织,采用Miltenyi Biotec组织消化液37℃孵育15分钟消化组织,经40μm细胞滤网过滤后制备单细胞悬液;使用MobiDrop单细胞试剂盒构建文库,通过Illumina NovaSeq 6000平台进行测序。
结果解读:共获得68214个高质量单细胞,其中老年组27460个、年轻组40754个;通过UMAP算法分群鉴定出9种主要细胞类型,包括管腔细胞(n=27153)、基底细胞(n=10204)、间质细胞(n=17590)、内皮细胞、淋巴管内皮细胞、髓系细胞、T细胞、B细胞、浆细胞。老年小鼠间质细胞与免疫细胞的相对比例显著升高,管腔细胞在年轻小鼠中占主导地位(校正P<0.01)。
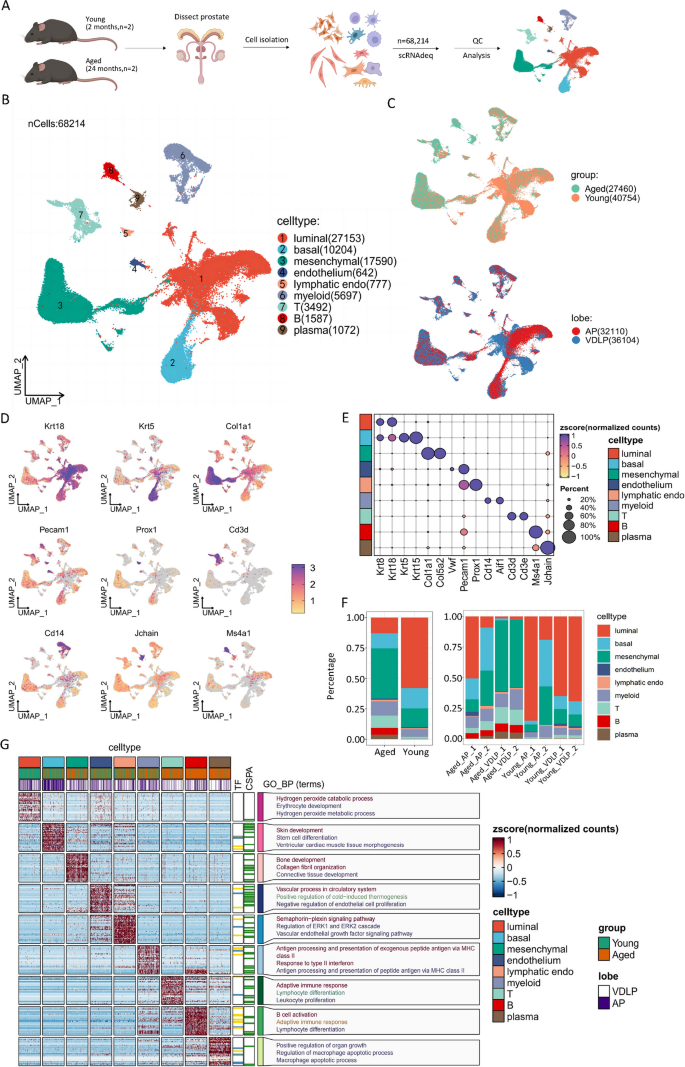
产品关联:实验所用关键产品:Miltenyi Biotec的组织储存缓冲液(货号130–100-008)、组织消化液(货号130–110-203),Pricella的胎牛血清(货号164210–50),Corning的40-µm细胞滤网(货号CLS431750),Sigma的牛血清白蛋白(货号A1933),MobiDrop的Chip A Single Cell Kit v2.0(货号S050100201)、Illumina NovaSeq 6000测序系统。
3.2 差异基因分析与衰老相关通路富集
实验目的:鉴定不同细胞类型中衰老相关的差异表达基因(DEGs),解析其调控的生物学通路。
方法细节:使用Seurat软件的FindMarkers函数筛选DEGs,阈值设置为校正P值<0.01、|log2倍数变化|>1.5;通过clusterProfiler进行GO功能富集分析,利用MSigDB Hallmark基因集计算衰老相关通路的基因集得分。
结果解读:几乎所有细胞类型中Spink1基因显著下调,老年小鼠Ly6a基因表达普遍升高;GO富集显示上皮细胞、间质细胞和髓系细胞的上调基因与“细胞衰老”“细胞因子介导的信号通路”“氧化应激反应”相关,T细胞上调基因与“病毒反应”“细胞质翻译”相关。老年组ROS信号通路得分在间质细胞、内皮细胞和免疫细胞中显著升高,管腔细胞中显著降低;SASP基因集得分在几乎所有主要细胞类型中显著升高,尤其是管腔细胞、基底细胞和间质细胞;再生基因集得分在间质细胞、内皮细胞和淋巴管内皮细胞中显著升高,管腔细胞和基底细胞中显著降低(校正P<0.01)。
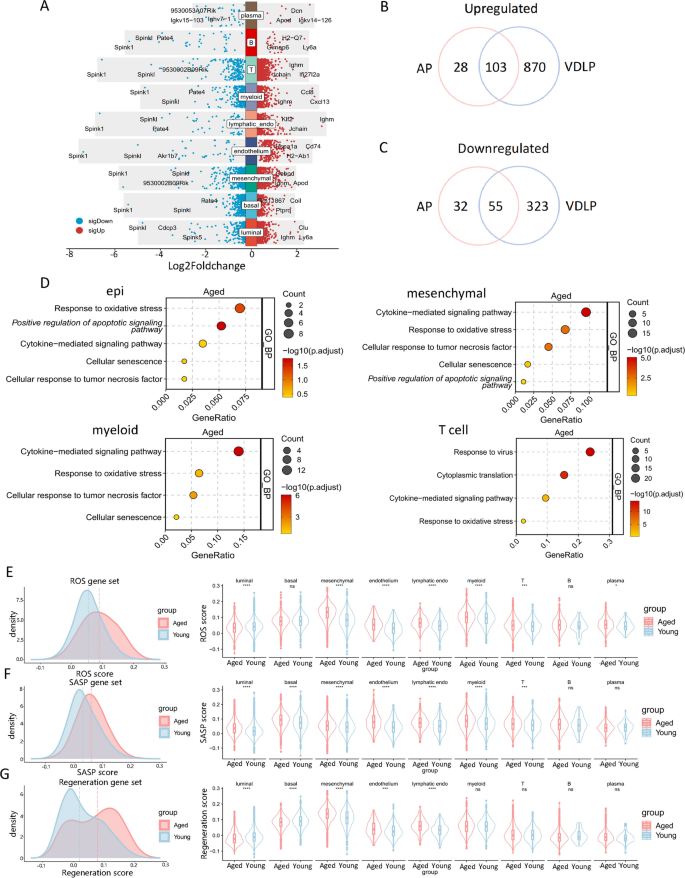
产品关联:文献未提及具体实验产品,领域常规使用qRT-PCR、蛋白免疫印迹等技术验证差异基因表达。
3.3 上皮细胞亚群异质性与发育轨迹分析
实验目的:解析上皮细胞的亚群组成及衰老对其的影响,明确上皮细胞的发育分化轨迹。
方法细节:通过tSNE分析将上皮细胞分为8个亚群(5个管腔细胞亚群、2个基底细胞亚群、1个增殖细胞亚群),利用Monocle软件进行拟时序分析,同时检测各亚群的慢性炎症、ROS得分及转录因子表达变化。
结果解读:老年小鼠基底_Krt15high亚群比例增加,VP管腔细胞、基底_Krt15low和增殖细胞比例降低;拟时序分析显示所有上皮细胞亚群均来源于基底细胞,基底细胞先分化为管腔祖细胞,再进一步分化为不同叶的上皮细胞。老年组上皮细胞中Ifitm3、Ighm、Ly6a基因上调,Spink1基因下调;慢性炎症得分在VP管腔细胞、LP管腔细胞和增殖亚群中升高,ROS得分在VP管腔细胞中升高、ADP管腔细胞等亚群中降低。转录因子分析显示Btf3、Gata3在多个亚群上调,Atf3、Egr1、Fosb在几乎所有亚群下调,Klf6在VP、LP管腔细胞等亚群中显著下调(校正P<0.01)。
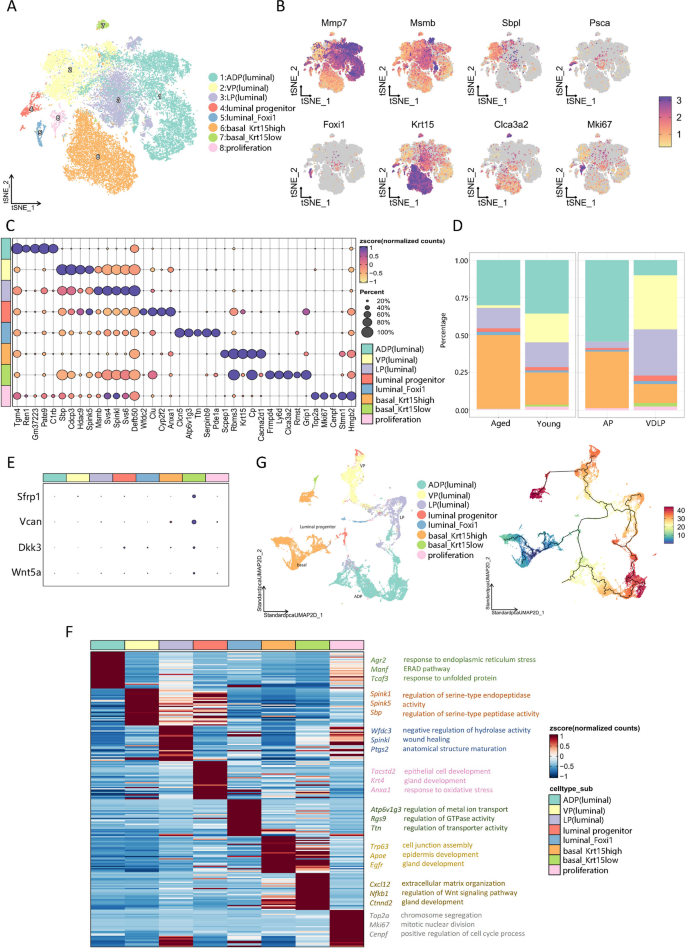
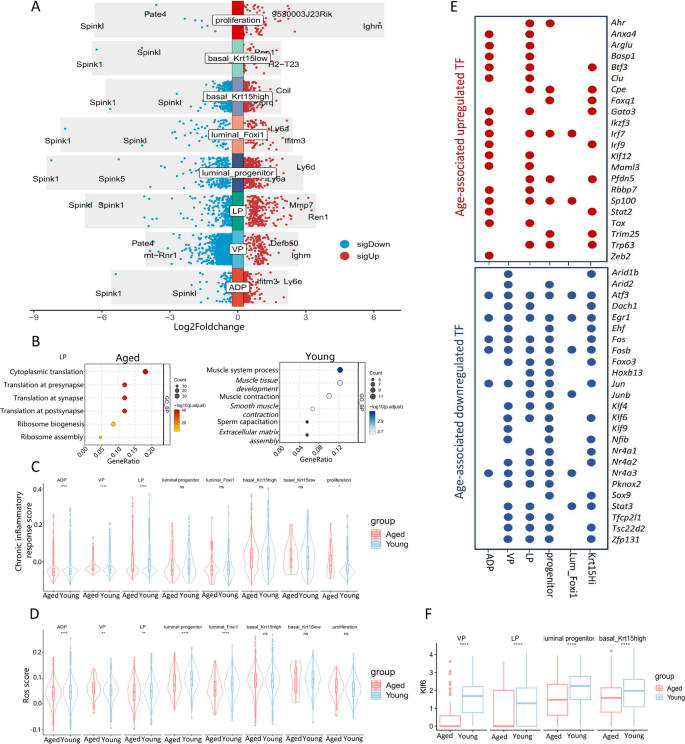
产品关联:实验所用关键产品:免疫荧光染色使用Proteintech的CK5抗体(货号66727–1-lg)、CDH1抗体(货号20874–1-AP)、VIM抗体(货号60330–1-Ig),Abcam的CD14抗体(货号ab182032)。
3.4 间质细胞亚群分析与EMT机制验证
实验目的:解析间质细胞的亚群异质性及衰老对其的影响,验证基底细胞向间质细胞的EMT转化机制。
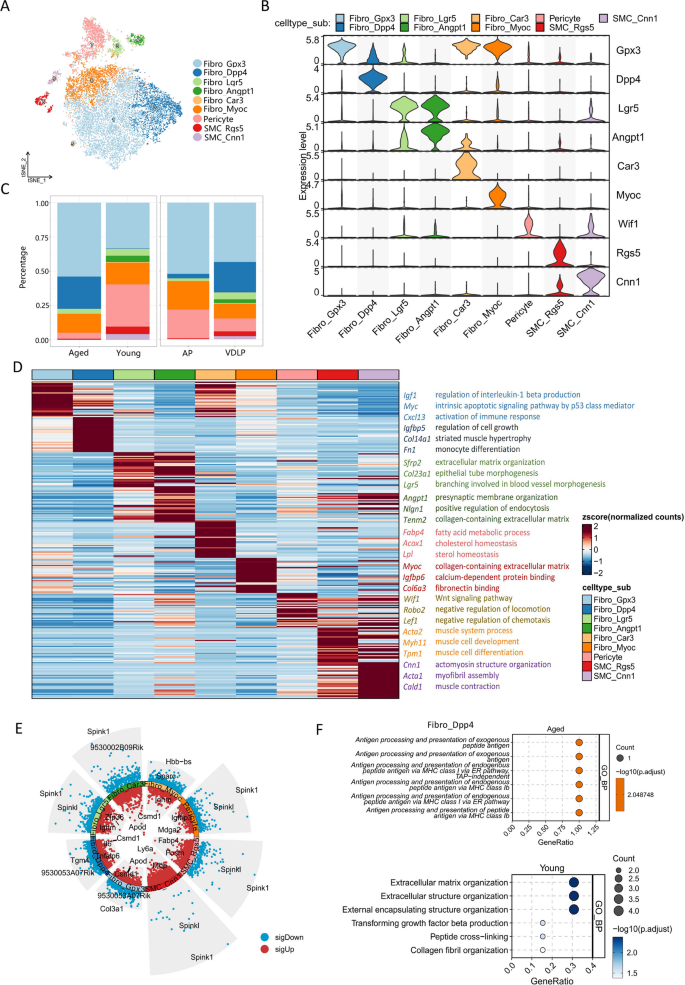
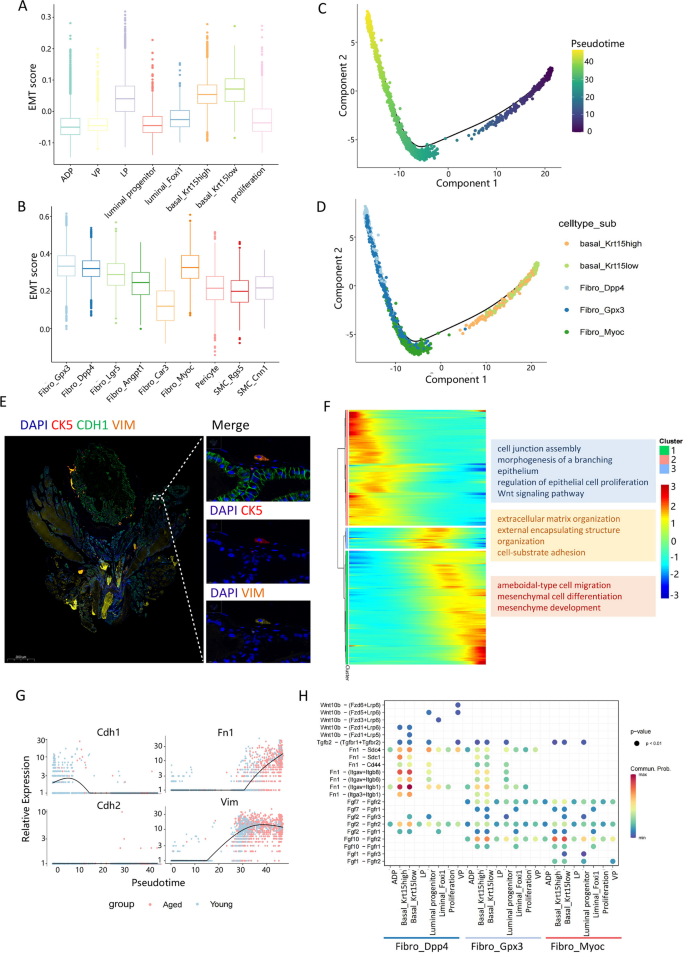
方法细节:通过tSNE分析将间质细胞分为9个亚群(6个成纤维细胞亚群、2个平滑肌细胞亚群、1个周细胞亚群),计算各亚群的EMT得分,利用Monocle进行拟时序分析,同时通过免疫荧光、蛋白免疫印迹验证EMT相关标记物的表达变化。
结果解读:老年小鼠Fibro_Dpp4和Fibro_Gpx3成纤维细胞亚群比例增加,Fibro_Angpt1亚群比例降低;老年组整体EMT得分显著高于年轻组,基底细胞与Fibro_Gpx3、Fibro_Dpp4、Fibro_Myoc亚群的EMT得分较高。拟时序分析显示基底_Krt15low亚群(主要存在于年轻小鼠)可分化为Fibro_Dpp4亚群(主要存在于老年小鼠),Cdh1表达随拟时序逐渐降低,Fn1和Vim表达逐渐升高;免疫荧光结果显示老年小鼠基底细胞失去Cdh1表达并获得Vim表达,证实EMT过程的存在(校正P<0.01)。
产品关联:实验所用关键产品:蛋白免疫印迹使用RIPA裂解液、BCA蛋白定量试剂盒、ECL发光试剂,免疫荧光使用Powerful Biology的EDTA抗原修复缓冲液(货号B0035)。
3.5 免疫细胞亚群分析与细胞通讯解析
实验目的:解析免疫细胞的亚群异质性及衰老对其的影响,明确免疫细胞与上皮/间质细胞的通讯机制。
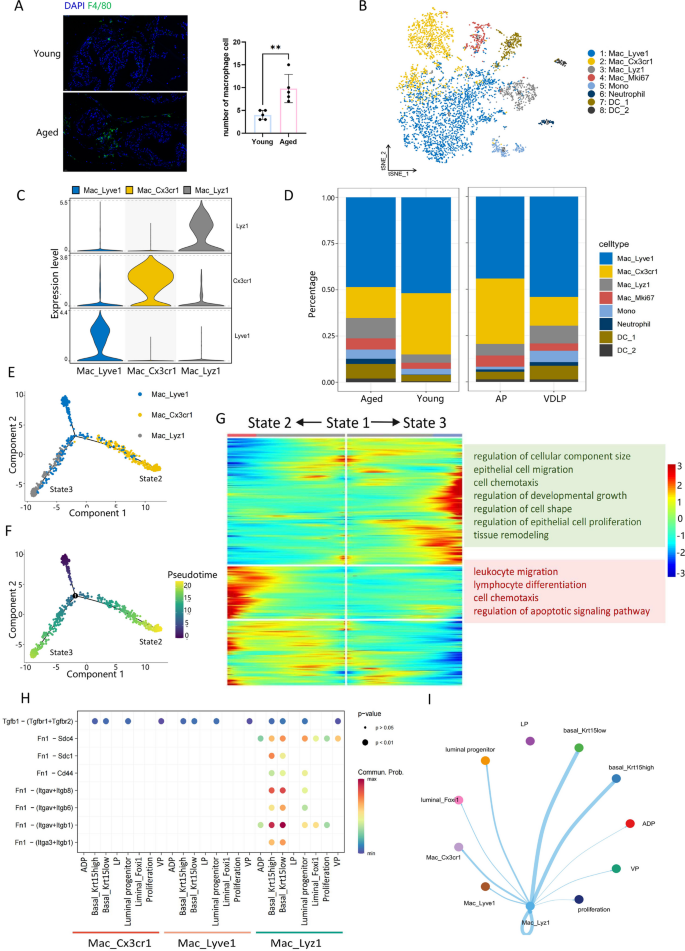
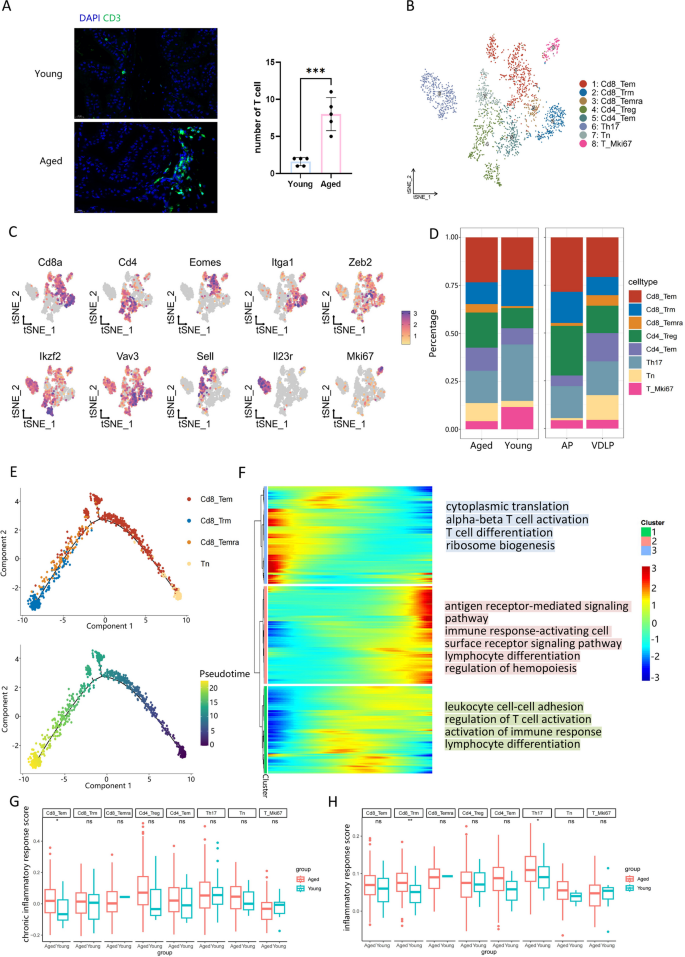
方法细节:通过tSNE分析将髓系细胞分为7个亚群、T细胞分为8个亚群,利用CellChat软件分析细胞间通讯,检测各亚群的炎症反应得分变化。
结果解读:老年小鼠Mac_Lyz1巨噬细胞亚群比例显著增加,该亚群通过Fn1-(Itgav + Itga1)配体-受体对与基底细胞相互作用,可能参与调控EMT过程;T细胞中Cd4_Treg亚群比例在老年小鼠中更高,老年小鼠T细胞的慢性炎症和炎症反应得分普遍升高,其中Cd8_Tem和Cd8_Trm亚群的得分变化具有统计学意义(校正P<0.01)。
产品关联:文献未提及具体实验产品,领域常规使用流式细胞术、免疫组化等技术验证免疫细胞亚群。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究涉及的Biomarker包括细胞比例标记物(间质细胞、免疫细胞比例)、基因标记物(Ly6a、Spink1、Csmd1)、通路标记物(ROS、SASP、EMT得分)。筛选与验证逻辑为:通过单细胞RNA测序筛选衰老相关差异细胞比例与基因,结合功能富集、拟时序分析解析其生物学功能,最终通过免疫荧光、蛋白免疫印迹实验验证核心标记物的表达变化。
研究过程详述
Biomarker来源为年轻与老年小鼠前列腺的单细胞转录组数据及组织样本。验证方法包括:单细胞测序的差异基因分析、GO功能富集、拟时序分析,免疫荧光验证EMT标记物(Cdh1、Vim)的表达定位,蛋白免疫印迹验证EMT相关蛋白的表达水平。特异性与敏感性方面,Ly6a在老年小鼠几乎所有主要细胞类型中上调,Spink1在几乎所有细胞类型中下调(n=68214,校正P<0.01);间质细胞比例在老年组显著增加,管腔细胞比例显著降低(文献未提供ROC曲线数据)。
核心成果提炼
Ly6a可作为前列腺衰老的潜在分子标志物,其上调与干细胞自我更新、免疫反应调控相关;Spink1下调可能与前列腺增生相关,或在前列腺癌发展中发挥双向调控作用;Csmd1在老年小鼠Fibro_Dpp4和Fibro_Gpx3成纤维细胞亚群中上调,可能参与前列腺疾病的发生发展。基底细胞向间质细胞的EMT转化是前列腺衰老的核心机制,Mac_Lyz1巨噬细胞通过Fn1信号通路参与调控该过程。统计学结果显示,所有差异均为校正P<0.01,样本量为4只小鼠(2年轻、2老年),共68214个单细胞。本研究发现的Biomarker为衰老相关前列腺疾病的早期诊断与靶向治疗提供了新的候选靶点。
