1. 领域背景与文献引入
文献英文标题:High expression of RNA-binding motif protein 3 in esophageal and gastric adenocarcinoma correlates with intestinal metaplasia-associated tumours and independently predicts a reduced risk of recurrence and death;发表期刊:Biomarker Research;影响因子:未公开;研究领域:上消化道腺癌生物标志物与预后研究
领域共识:食管癌是全球第八大常见癌症及第六大癌症死因,胃腺癌曾为全球最常见癌症,目前位列第四大常见癌症及第二大癌症死因,两类癌症患者多因症状隐匿导致诊断延迟,多数病例确诊时已处于晚期,预后极差,因此亟需鉴定新的预后生物标志物以优化患者临床管理。现有研究显示RNA结合基序蛋白3(RBM3)在乳腺癌、卵巢癌、前列腺癌等多种癌症中,高核表达与良好临床病理特征及延长生存期相关,其机制可能涉及调控DNA完整性修复、减弱肿瘤干细胞特性,但RBM3在上消化道腺癌中的表达模式及预后意义尚未见报道。针对这一研究空白,本研究旨在通过连续队列分析,明确RBM3在未经放化疗的食管、胃食管结合部及胃腺癌中的表达特征、临床病理关联及独立预后价值,为上消化道腺癌的预后分层提供新的生物标志物依据。
2. 文献综述解析
本研究的文献综述部分以“RBM3在恶性肿瘤中的预后价值及机制”为核心评述逻辑,按癌种分类梳理现有研究结论,同时明确上消化道腺癌领域的研究空白。现有研究显示,RBM3在卵巢癌中高表达与顺铂敏感性及良好预后相关,在结直肠癌、乳腺癌、前列腺癌、恶性黑色素瘤等癌种中,高核表达均被证实为独立的良好预后因素,技术方法上多采用免疫组化结合组织微阵列的大样本分析,具有样本代表性强、检测效率高的优势,部分研究还探索了RBM3的调控机制,如参与DNA完整性修复、减弱肿瘤干细胞特性等。但现有研究仍存在局限性,一是缺乏上消化道腺癌这一高发癌种的相关数据,二是RBM3与癌前病变(如肠化生)的关联未被探索,其在上消化道腺癌中的表达模式及预后意义完全未知。通过对比现有研究的未解决问题,本研究的创新价值凸显:首次在未经放化疗的上消化道腺癌连续队列中开展研究,同时分析RBM3在正常组织、癌前病变、原发肿瘤及转移灶中的表达差异,明确其与肠化生相关肿瘤的关联,并验证其作为独立预后标志物的价值,填补了RBM3在上消化道腺癌领域的研究空白,为该癌种的预后分层提供了新的分子依据。
3. 研究思路总结与详细解析
本研究的整体研究框架为:以“RBM3在上消化道腺癌中的表达模式及预后价值”为核心科学问题,通过“研究队列构建→组织微阵列制备→免疫组化检测→表达差异分析→临床病理关联→生存预后验证”的技术路线,验证RBM3作为上消化道腺癌预后生物标志物的价值,形成完整的研究闭环。
3.1 研究队列构建与组织微阵列制备
本环节的实验目的是建立具有代表性的上消化道腺癌研究队列,并构建标准化组织微阵列以实现高效的多组织样本检测。方法细节为纳入2006年1月至2010年12月瑞典隆德和马尔默大学医院手术治疗的175例食管及胃腺癌患者,经病理复检最终纳入173例未经放化疗的原发肿瘤患者,同时收集配对的正常鳞状上皮(n=53)、胃黏膜(n=117)、肠化生组织(n=61)及淋巴结转移灶(n=71)样本,采用半自动阵列仪构建组织微阵列,每个原发肿瘤取2个1mm组织芯,转移灶、癌前病变及正常组织按对应标准取芯。结果解读为成功构建包含多类型组织的标准化微阵列,原发肿瘤样本可评估率达98.9%,转移灶达94.7%,组织芯间无明显异质性,确保了后续检测的可靠性。实验所用关键产品:Atlas Antibodies AB的抗RBM3单克隆抗体(货号AAb030038)、DAKO的Autostainer Plus免疫组化染色系统、Ventana BenchMark ULTRA系统的Ki67单克隆抗体(克隆号MIB1)。
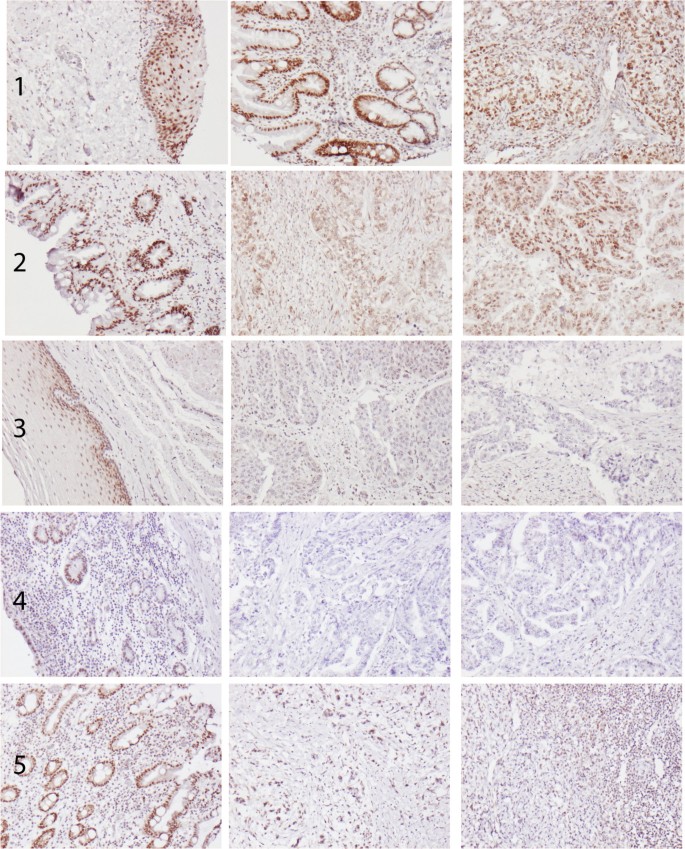
3.2 RBM3表达的免疫组化(IHC)检测与表达差异分析
本环节的实验目的是系统分析RBM3在不同组织类型中的表达特征及与临床病理参数的关联。方法细节为采用免疫组化技术检测组织微阵列中RBM3的表达,由两名独立盲法观察者评估核RBM3表达的细胞比例及染色强度,计算综合核评分,同时检测Ki67表达以评估肿瘤增殖水平,采用Mann Whitney U检验分析RBM3表达与临床病理参数的关联。结果解读为正常鳞状上皮和肠化生组织中RBM3表达显著高于正常胃黏膜、原发肿瘤及转移灶(n=53/61/117,P<0.001),原发肿瘤与转移灶中RBM3表达无显著差异;有肠化生背景的原发肿瘤及转移灶中RBM3表达显著高于无肠化生者(P<0.001),且RBM3表达随肿瘤分期进展显著降低(P=0.006);原发肿瘤中RBM3表达与Ki67增殖水平无显著关联,但转移灶中高RBM3表达与增殖水平升高呈正相关。
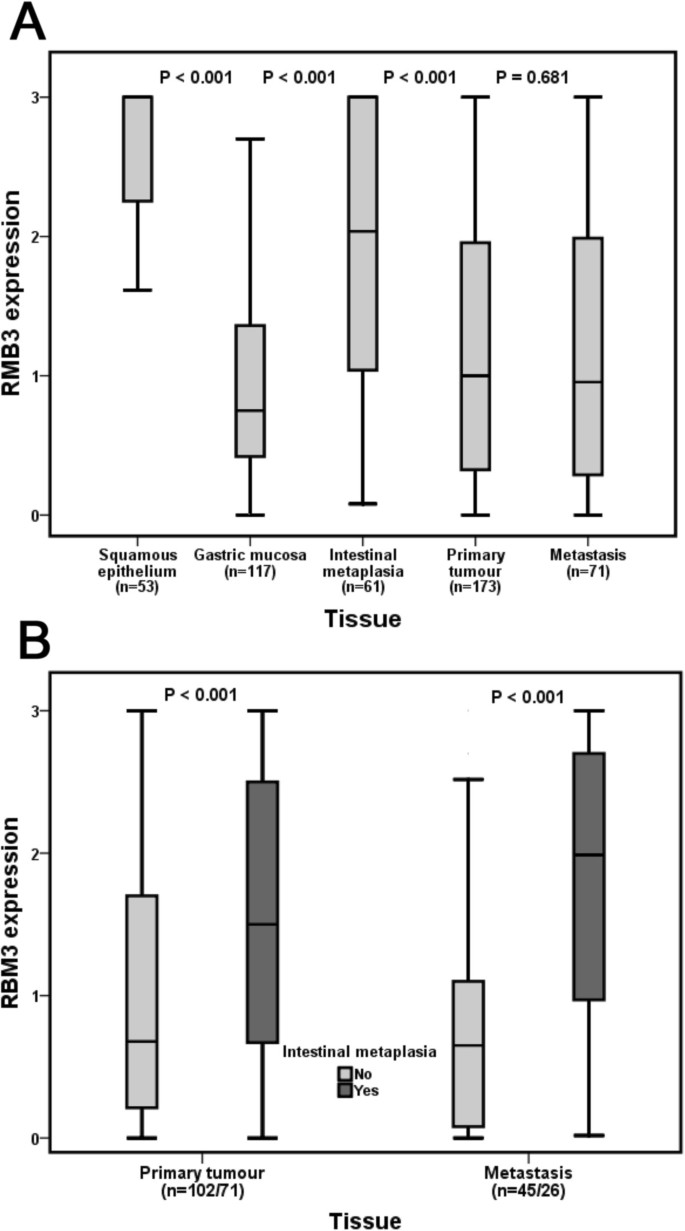
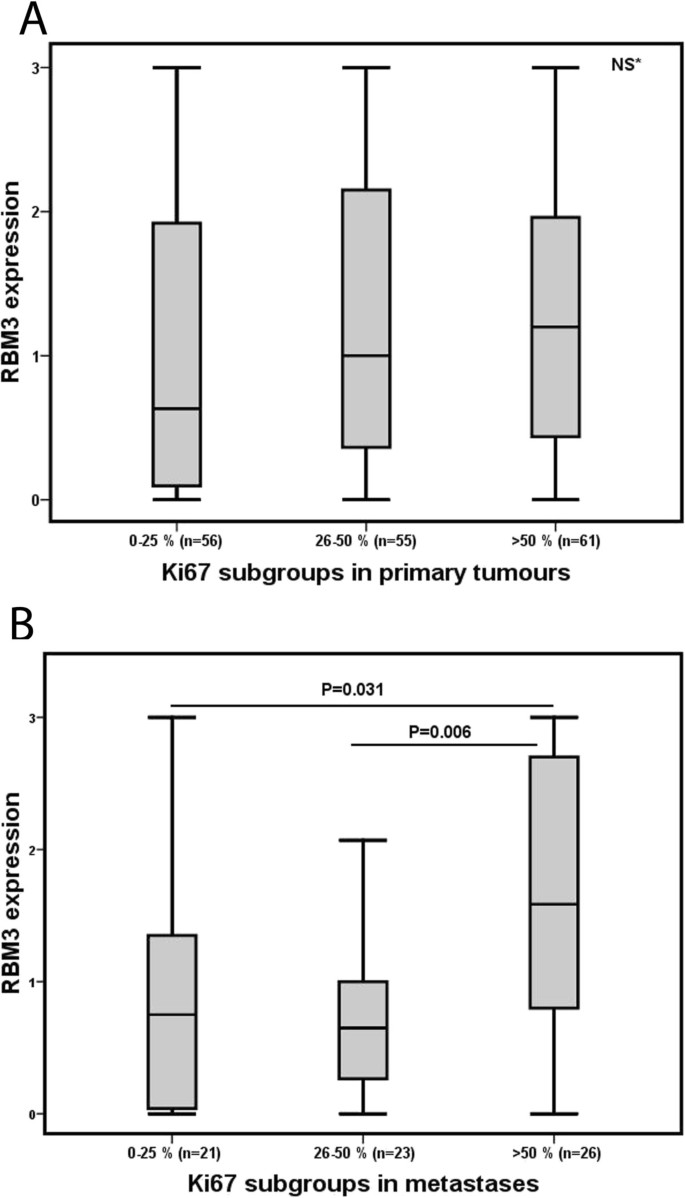
3.3 生存预后分析与独立预后价值验证
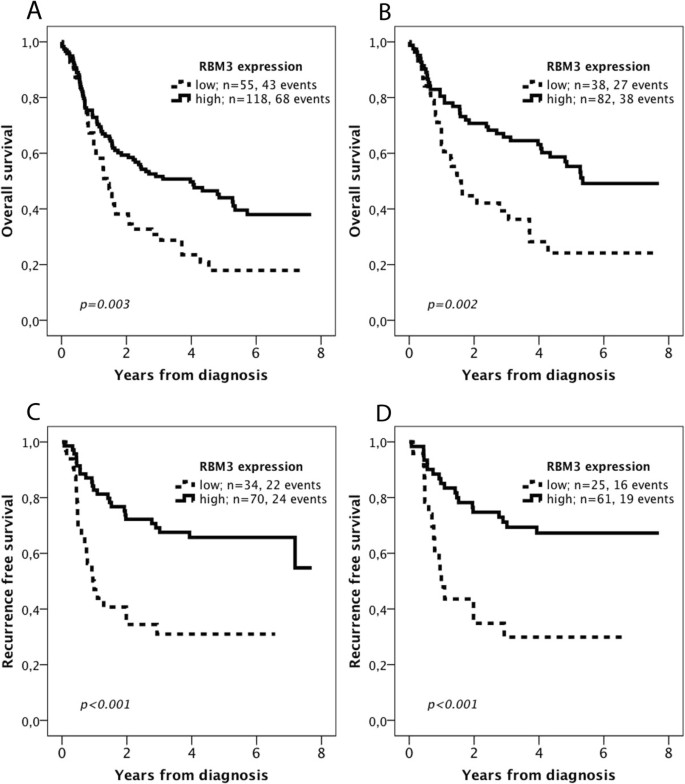
本环节的实验目的是验证RBM3表达对患者生存期的预测价值及独立性。方法细节为通过分类回归树分析确定RBM3表达的预后截断值,采用Kaplan-Meier法绘制生存曲线并比较组间差异,通过Cox比例风险模型在未调整及调整年龄、性别、肿瘤分期等混杂因素后,评估RBM3表达对总生存期(OS)及无复发生存期(RFS)的独立影响。结果解读为低RBM3表达与根治性切除(R0)患者更短OS相关(风险比HR=2.19,95%CI 1.33-3.61,n=173,P=0.002),与根治性治疗且无远处转移患者更短RFS相关(HR=3.21,95%CI 1.64-6.30,P=0.001);调整混杂因素后,RBM3表达仍为独立的预后因素,OS的HR为1.95(95%CI 1.17-3.25,P=0.010),RFS的HR为3.02(95%CI 1.45-6.29,P=0.003)。文献未提及具体统计分析产品,领域常规使用IBM SPSS Statistics类统计软件。
4. Biomarker研究及发现成果
本研究鉴定的核心Biomarker为RNA结合基序蛋白3(RBM3),其高表达可作为上消化道腺癌的独立预后良好标志物,且与肠化生相关肿瘤密切关联,为上消化道腺癌的预后分层提供了新的分子依据。
Biomarker定位方面,RBM3属于核定位的RNA结合蛋白,本研究基于其在其他癌种中的预后价值,首次在上消化道腺癌队列中开展验证,筛选与验证逻辑为:先通过组织微阵列免疫组化检测RBM3在正常组织、癌前病变、原发肿瘤及转移灶中的表达,分析其与肠化生背景的关联,再通过临床病理关联分析明确其与肿瘤分期的关系,最后通过生存分析验证其独立预后价值,形成完整的“表达特征-临床关联-预后验证”逻辑链条。
研究过程详述:样本来源为173例上消化道腺癌患者的原发肿瘤组织,及配对的正常鳞状上皮(n=53)、正常胃黏膜(n=117)、肠化生组织(n=61)、淋巴结转移灶(n=71);验证方法为免疫组化染色评估核RBM3的综合表达评分;特异性表现为,有肠化生背景的原发肿瘤及转移灶中RBM3表达显著高于无肠化生者(P<0.001),且RBM3表达随肿瘤分期进展显著降低(P=0.006);敏感性方面,低RBM3表达可有效预测患者不良预后,在R0切除患者中,总生存期的风险比为2.19(95%CI 1.33-3.61,P=0.002),无复发生存期的风险比为3.21(95%CI 1.64-6.30,P=0.001),调整混杂因素后仍保持显著的独立预测价值。
核心成果提炼:RBM3高表达与上消化道腺癌的肠化生背景密切相关,提示其可能参与上消化道腺癌的肠型发生通路;同时,RBM3高表达是上消化道腺癌独立的预后良好标志物,可预测患者更低的复发及死亡风险;本研究的创新性在于首次在上消化道腺癌中报道RBM3的表达特征及预后价值,明确其与肠化生相关肿瘤的关联,填补了该领域的研究空白;所有关键结论均有显著统计学结果支持,样本量覆盖173例原发肿瘤患者,平均随访时间达5.2年,研究结果具有较高的可靠性。
