1. 领域背景与文献引入
文献英文标题:Genome-wide mapping of FOXM1 binding reveals co-binding with estrogen receptor alpha in breast cancer cells;发表期刊:Genome Biology;影响因子:未公开;研究领域:乳腺癌转录调控与肿瘤生物学
叉头框转录因子FOXM1是细胞周期的关键调控因子,参与G1/S期转换、G2/M期进展、有丝分裂纺锤体组装等核心过程,其缺失会导致有丝分裂灾难和细胞周期停滞。领域共识:FOXM1在乳腺癌、结直肠癌等多种实体瘤中过表达,与肿瘤侵袭、转移、不良预后密切相关,是潜在的肿瘤治疗靶点。在乳腺癌中,约70%的病例为雌激素受体α(ERα)阳性,内分泌治疗是这类患者的一线治疗方案,但约30%的患者会出现原发性或继发性耐药,成为临床治疗的核心难题。现有研究显示,FOXM1的表达与ERα活性密切相关,FOXM1是ERα的直接靶基因,其高表达与ERα阳性乳腺癌患者的内分泌耐药、不良预后相关,但FOXM1与ERα在基因组层面的共结合模式,以及FOXM1调控ERα转录活性的具体机制尚未完全阐明,这一研究空白限制了对FOXM1在ERα阳性乳腺癌中功能的理解,也阻碍了针对FOXM1的靶向治疗策略的开发。本研究旨在通过全基因组染色质免疫共沉淀(ChIP)结合高通量测序技术,揭示FOXM1在ERα阳性和阴性乳腺癌细胞中的结合模式,明确FOXM1与ERα的相互作用机制,为ERα阳性乳腺癌的预后评估和治疗提供新的靶点和理论依据。
2. 文献综述解析
作者围绕FOXM1的细胞周期调控功能、FOXM1在肿瘤中的异常表达及临床意义、FOXM1与ERα的转录调控关联三个维度对现有研究进行评述。
现有研究已证实FOXM1是细胞周期的核心调控因子,通过调控CCNB1、CDC25B等细胞周期相关基因的表达,促进细胞增殖和有丝分裂;在肿瘤领域,FOXM1在乳腺癌、结直肠癌等多种癌症中过表达,与肿瘤分期、侵袭性、不良预后呈正相关,且其过表达与乳腺癌的HER2状态、内分泌耐药相关。技术方法上,早期研究多采用定量PCR、免疫印迹等技术分析FOXM1的表达和转录调控,部分研究通过染色质免疫共沉淀技术分析单个或少数基因的结合位点,但缺乏全基因组层面的系统分析,无法揭示FOXM1在不同ERα状态乳腺癌细胞中的结合模式差异。现有研究的局限性在于,仅发现FOXM1与ERα在转录层面的相互调控,未明确两者在基因组层面的共结合机制,也不清楚FOXM1如何调控ERα的转录活性。
本研究的创新价值在于,首次通过全基因组染色质免疫共沉淀结合高通量测序技术,绘制了FOXM1在ERα阳性和阴性乳腺癌细胞中的结合图谱,发现FOXM1与ERα的广泛共结合现象,揭示了FOXM1通过招募共激活因子CARM1调控ERα转录活性的分子机制,同时明确了FOXM1结合模式的细胞系特异性,为理解FOXM1在ERα阳性乳腺癌中的功能提供了全基因组层面的证据。
3. 研究思路总结与详细解析
本研究的整体研究目标是揭示FOXM1在不同ERα状态乳腺癌细胞中的全基因组结合模式,阐明FOXM1与ERα的相互作用机制及功能意义;核心科学问题包括FOXM1如何与ERα协同调控基因转录、FOXM1的结合模式是否依赖ERα状态、FOXM1调控的基因是否与乳腺癌患者预后相关;技术路线遵循“全基因组定位→分子机制验证→功能与临床意义分析”的闭环逻辑,通过染色质免疫共沉淀结合高通量测序、分子生物学实验、临床数据分析等多层面验证研究假设。
3.1 ERα阳性乳腺癌细胞中FOXM1全基因组结合位点分析
实验目的是系统绘制ERα阳性MCF7细胞中FOXM1的全基因组结合位点,明确其调控的生物学通路和潜在的协同作用因子。方法细节:采用染色质免疫共沉淀结合高通量测序技术,在MCF7细胞中进行4个生物学重复的FOXM1染色质免疫共沉淀实验,对测序数据进行分析,识别FOXM1的结合位点,通过功能注释、基序富集分析明确其调控的通路和潜在的结合基序,同时与已发表的ERα、FOXA1染色质免疫共沉淀数据集进行重叠分析。结果解读:全基因组分析显示,MCF7细胞中FOXM1共检测到21029个离散结合事件,其中约9%的结合位点位于启动子区域,主要调控细胞周期、有丝分裂等通路的基因(如CCNB1、CDC25B),约85%的结合位点位于基因间和内含子区域;功能注释分析显示,FOXM1结合位点富集的生物学过程包括细胞增殖、M期调控、类固醇激素刺激应答等;基序富集分析显示,FOXM1结合区域富集了叉头框、亮氨酸拉链、核受体家族等基序,其中ERα结合基序显著富集;与已发表的ERα染色质免疫共沉淀数据集重叠分析显示,约80%的FOXM1结合位点与ERα结合位点重叠,约71%的FOXM1结合位点与FOXA1结合位点重叠,提示FOXM1与ERα、FOXA1存在协同结合。
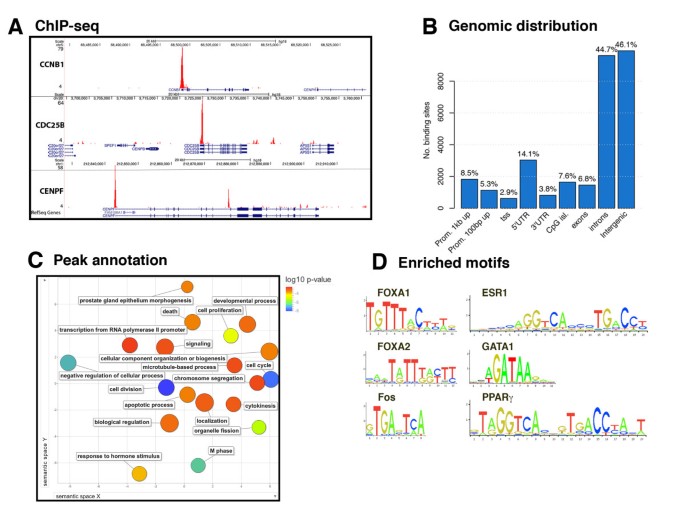
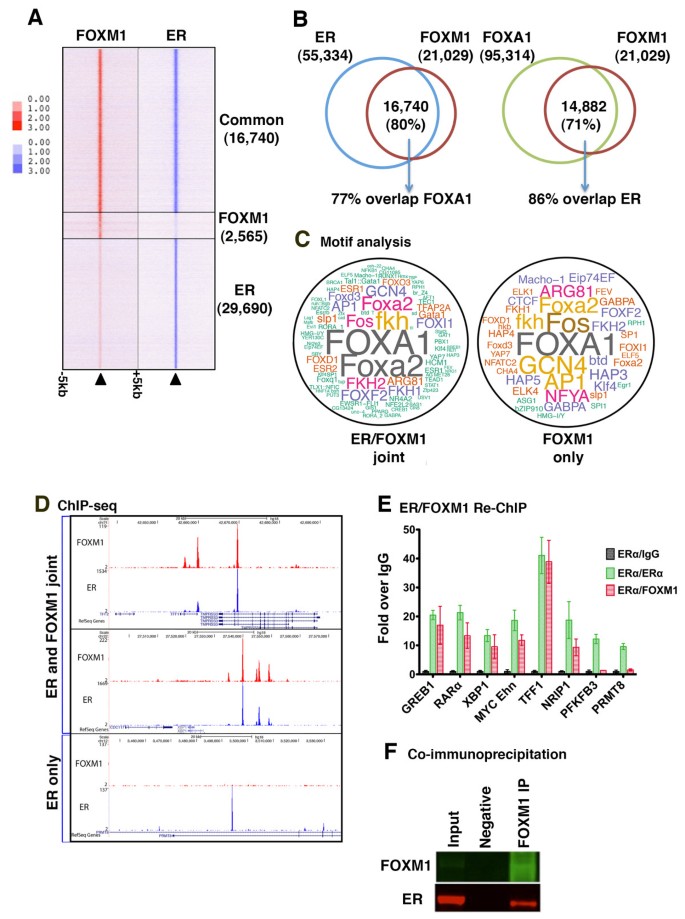
实验所用关键产品:Santa Cruz的FOXM1抗体(货号sc-502)、ERα抗体(货号sc-543),Illumina高通量测序平台。
3.2 FOXM1与ERα的共结合验证及相互作用机制
实验目的是验证FOXM1与ERα是否同时结合在同一染色质位点,以及ERα对FOXM1结合的调控作用。方法细节:采用Re-ChIP实验,先对MCF7细胞进行ERα染色质免疫共沉淀,再对沉淀产物进行FOXM1染色质免疫共沉淀,通过定量PCR验证共结合位点;采用免疫共沉淀(Co-IP)实验验证FOXM1与ERα的直接相互作用;用雌激素受体拮抗剂氟维司群(10nM)处理MCF7细胞3小时,通过免疫印迹检测ERα和FOXM1的蛋白水平,通过染色质免疫共沉淀结合定量PCR检测FOXM1在共结合位点和非共结合位点的结合变化;用siRNA敲低FOXM1,检测ERα的蛋白水平和结合位点的结合变化。结果解读:Re-ChIP实验结果显示,在共结合位点(如GREB1、RARα区域),FOXM1和ERα可同时结合在同一染色质位点,而在仅ERα结合的位点(如PRMT8区域)未检测到FOXM1的共结合;免疫共沉淀实验显示FOXM1与ERα存在直接相互作用;氟维司群处理后,ERα蛋白水平显著降低,FOXM1蛋白和转录水平无变化,FOXM1在共结合位点的结合显著降低(P<0.05),但在ERα非结合位点(如PLK1启动子)的结合无显著变化;siRNA敲低FOXM1后,ERα蛋白水平无显著变化,ERα在其结合位点的结合也无显著变化,提示FOXM1的招募依赖ERα,但FOXM1不影响ERα的染色质结合。

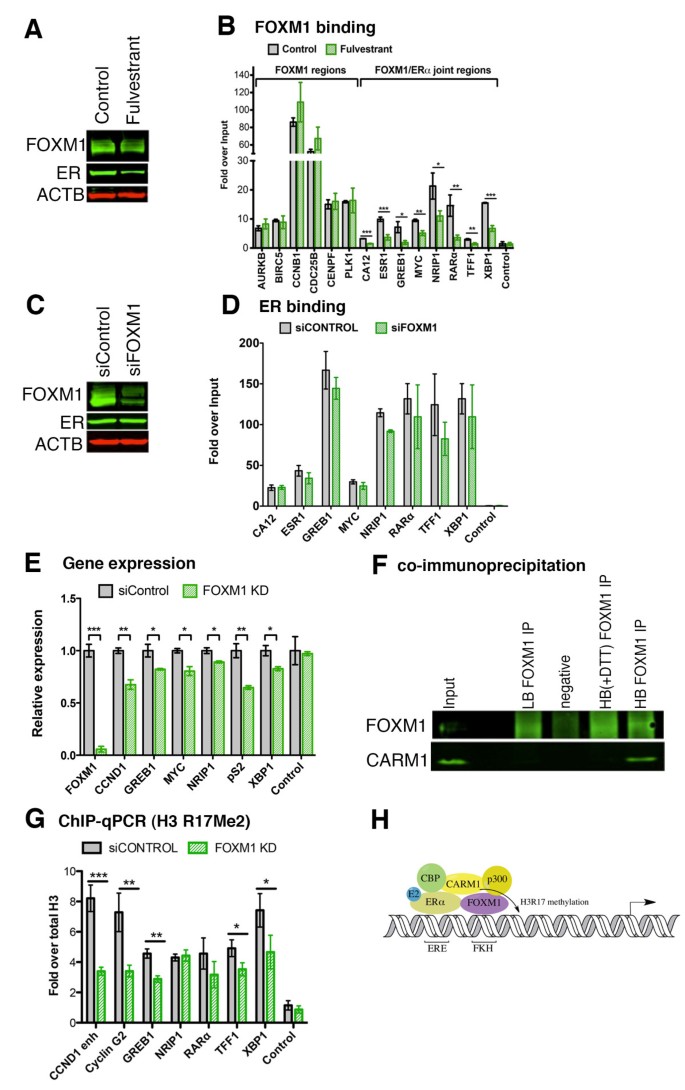
实验所用关键产品:Santa Cruz的FOXM1抗体(货号sc-502)、ERα抗体(货号sc-543),Dharmacon的FOXM1 siRNA,氟维司群(Sigma)。
3.3 FOXM1通过CARM1调控ERα转录活性的机制
实验目的是探究FOXM1调控ERα转录活性的分子机制。方法细节:通过蛋白质组学筛选FOXM1的相互作用蛋白,聚焦共激活因子CARM1;采用免疫共沉淀实验验证FOXM1与CARM1的直接相互作用;用siRNA敲低FOXM1,通过染色质免疫共沉淀结合定量PCR检测共结合位点的组蛋白H3精氨酸17甲基化水平(CARM1的催化产物)。结果解读:免疫共沉淀实验证实FOXM1与CARM1存在直接相互作用;敲低FOXM1后,共结合位点的组蛋白H3精氨酸17甲基化水平显著降低,提示FOXM1通过招募CARM1到ERα结合位点,促进组蛋白甲基化,从而调控ERα的转录活性。

实验所用关键产品:Santa Cruz的FOXM1抗体(货号sc-502)、CARM1抗体(货号sc-5421),Novus的组蛋白H3精氨酸17甲基化抗体(货号NB21-1132)。
3.4 ERα阴性乳腺癌细胞中FOXM1结合模式的差异分析
实验目的是对比ERα阳性和阴性乳腺癌细胞中FOXM1的结合模式,明确ERα状态对FOXM1结合的影响。方法细节:在ERα阴性MDA-MB-231细胞中进行2个生物学重复的FOXM1染色质免疫共沉淀结合高通量测序实验,分析FOXM1的结合位点分布,并与MCF7细胞的结合位点进行对比;同时在另外3种ERα阳性细胞系(T47D、ZR-751)和2种ERα阴性细胞系(MDA-MB-453、MCF10A)中,通过染色质免疫共沉淀结合定量PCR验证FOXM1在共结合位点和非共结合位点的结合。结果解读:MDA-MB-231细胞中FOXM1的结合位点与MCF7细胞的重叠仅为14%,其中约52%的共同结合位点位于ERα非结合区域;基因组分布显示,MDA-MB-231细胞中FOXM1约31%的结合位点位于启动子区域,约13%位于5"UTR,而MCF7细胞中仅约9%位于启动子区域,约2%位于5"UTR;在其他ERα阳性细胞系中,FOXM1可结合在ERα结合位点,而在ERα阴性细胞系中则无法结合,提示FOXM1的结合模式具有细胞系特异性,依赖ERα状态。
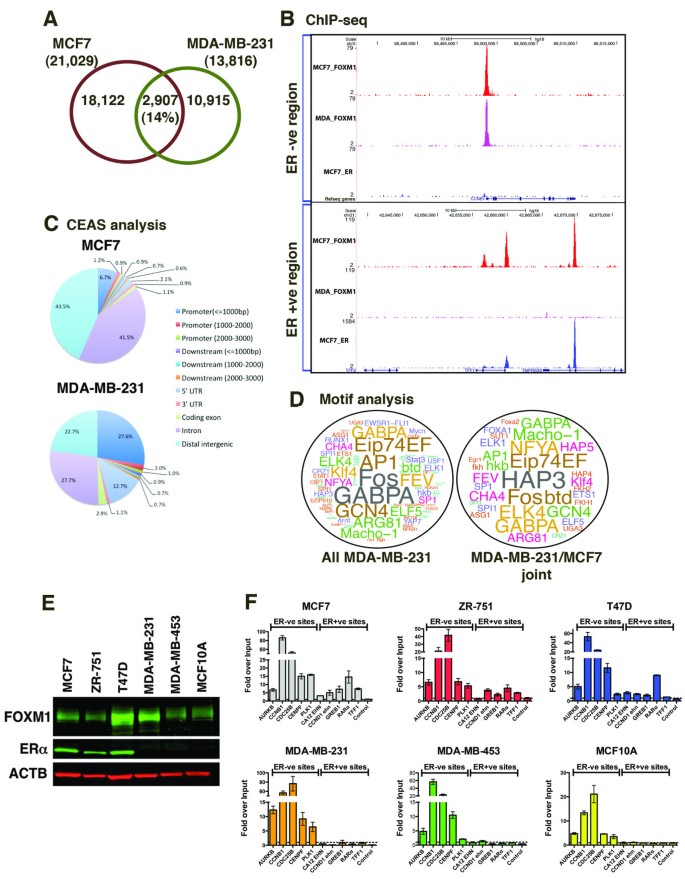
实验所用关键产品:Santa Cruz的FOXM1抗体(货号sc-502),Illumina高通量测序平台。
3.5 硫链丝菌素抑制FOXM1的功能验证及临床意义
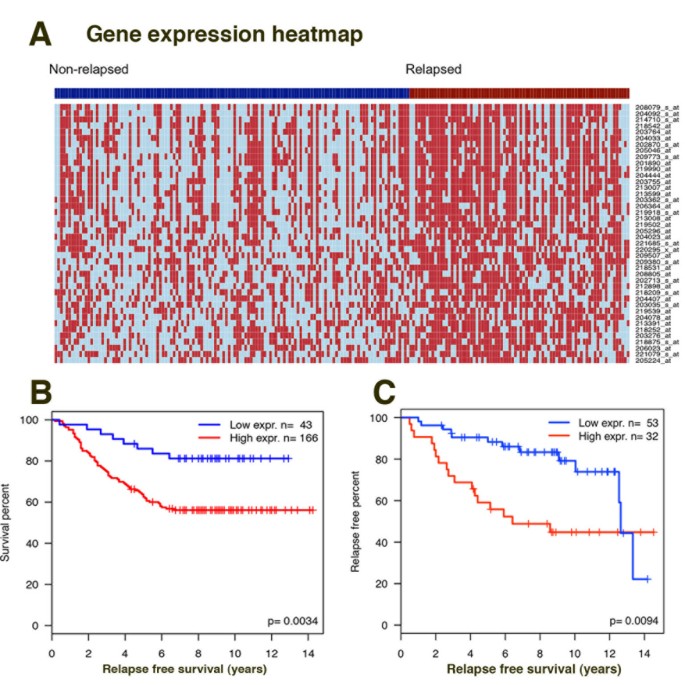
实验目的是验证FOXM1的功能,以及其调控的基因与乳腺癌患者预后的关联。方法细节:用硫链丝菌素(10μM)处理MCF7细胞4小时,通过染色质免疫共沉淀结合高通量测序检测FOXM1结合位点的变化;处理6小时后,通过基因表达芯片检测基因表达变化;通过基因集富集分析、生存分析,将差异结合位点和差异表达基因与乳腺癌患者的临床预后数据关联。结果解读:硫链丝菌素处理后,共检测到1902个差异结合位点,其中约76%的位点FOXM1结合降低,这些位点富集的通路包括类固醇激素信号通路、FGFR信号通路;基因表达芯片显示,处理后有2322个差异表达基因,其中ERα信号通路显著富集;将硫链丝菌素下调的、与FOXM1结合位点距离转录起始位点(TSS)±50kb以内的基因与209例ERα阳性乳腺癌患者的生存数据关联,发现38个基因的高表达与患者的不良预后显著相关(P<10^-6),Kaplan-Meier生存分析显示,该基因签名的高表达与患者复发时间缩短显著相关(P<0.0034),在独立数据集(n=209)中也得到验证(P=0.0094),提示FOXM1调控的基因具有临床预后价值。
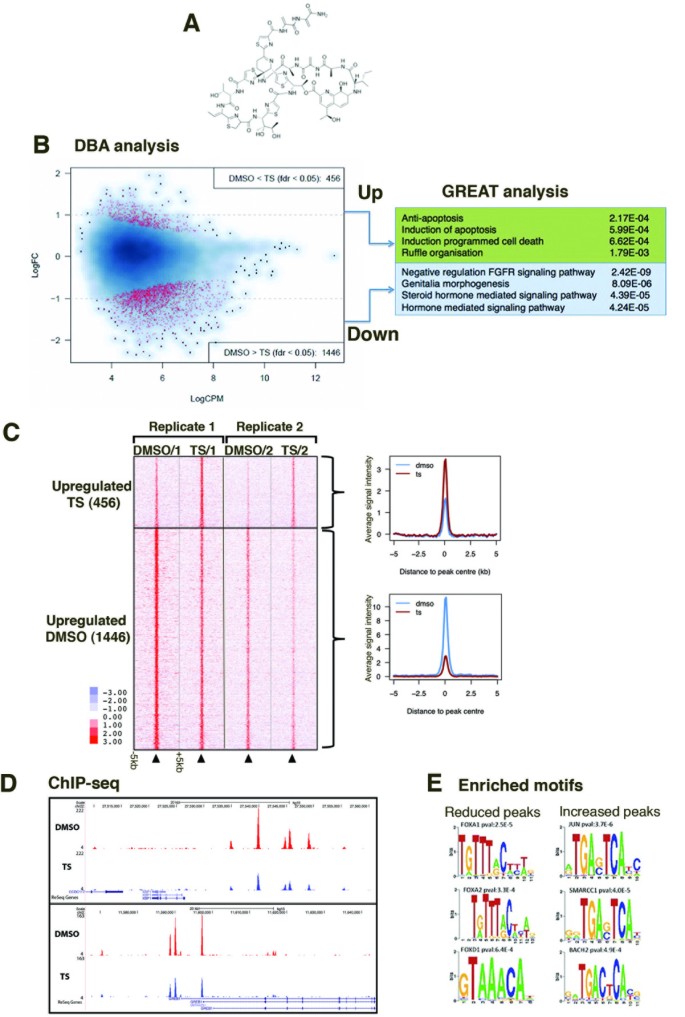
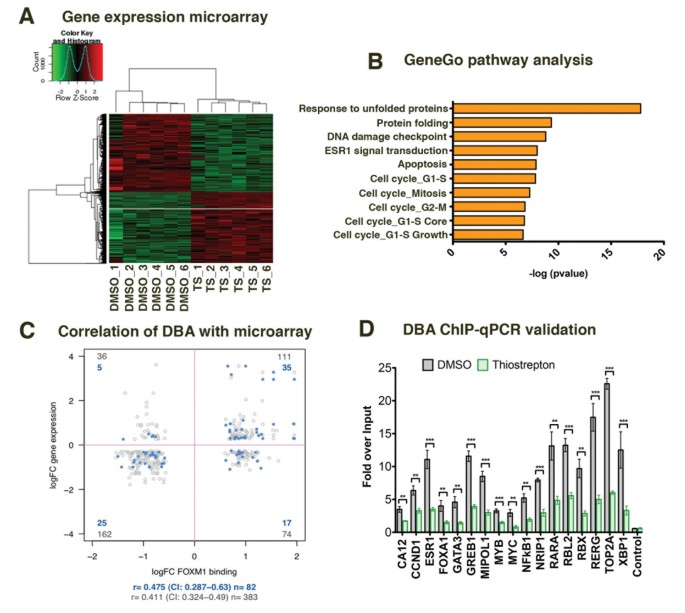
实验所用关键产品:硫链丝菌素(Sigma),Illumina Human HT12 version 4基因表达芯片。
4. Biomarker研究及发现成果
本研究发现的Biomarker是由38个FOXM1调控的基因组成的基因签名,其筛选逻辑为硫链丝菌素处理后下调的基因→与FOXM1结合位点距离转录起始位点(TSS)±50kb以内→在ERα阳性乳腺癌患者数据集中与不良预后显著相关。
研究过程详述:该基因签名的基因来源为MCF7细胞经硫链丝菌素处理后的差异表达基因,通过染色质免疫共沉淀结合高通量测序确认这些基因的调控区域存在FOXM1结合位点;验证方法包括基因表达芯片、染色质免疫共沉淀结合定量PCR、Kaplan-Meier生存分析;在209例ERα阳性乳腺癌患者中,该基因签名的高表达与患者的复发时间缩短显著相关(Kaplan-Meier分析P<0.0034),在独立的ERα阳性乳腺癌患者数据集(n=209)中,该基因签名的高表达同样与不良预后显著相关(P=0.0094),提示其具有较好的特异性和敏感性。
核心成果提炼:该基因签名可作为ERα阳性乳腺癌患者的预后生物标志物,其高表达提示患者复发风险高、预后差;本研究首次揭示了FOXM1通过与ERα共结合、招募CARM1调控ERα转录活性的机制,明确了FOXM1调控的基因签名与ERα阳性乳腺癌患者预后的关联,为ERα阳性乳腺癌的预后评估提供了新的生物标志物,同时为针对FOXM1的靶向治疗提供了理论依据,具有重要的临床转化价值。
